-
某探究小组同学研究金属铝与稀盐酸的反应速率受外界因素影响的情况.
实验药品:5%盐酸、10%盐酸、质量相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50.0mL,金属用量均为9.0g.
(1)写出铝与盐酸反应的化学方程式______.
(2)该小组设计了如下影响反应速率因素的实验(温度控制为25℃和35℃).请你根据实验目的帮助该小组完成以下实验设计表(用量:酸均为50.0mL、铝为9.0g过量):
(3)根据实验①和③得到的结论是______.实验目的 实验
编号温度 金属铝
形态盐酸浓度 1.实验①和②探究盐酸浓度对该反应速率的影响;
2.实验①和③探究温度对该反应速率的影响;
3.实验①和④探究金属颗粒大小(铝片、铝粉)对该反应速率的影响.① 25˚C 铝片 10% ② ③ ④ 九年级化学解答题中等难度题查看答案及解析
-
某研究性学习小组同学探究影响镁与稀硫酸反应速率的因素.
药品:5%硫酸、10%硫酸、质量相同的镁片和镁粉(表面氧化膜都已除去);
(1)该小组设计了影响反应速率因素(温度控制为25℃和35℃).请你根据实验目的帮助该小组完成以下设计表格(用量:5%硫酸、10%硫酸用量每次均为5.0mL,镁片和镁粉的用量均为0.5g).
(2)根据②和④得到结论是______.实验目的 编号 温度 镁的形态 硫酸浓度 1、①和②硫酸浓度对该反应速率影响
2、①和③温度对该反应速率影响;
3、②和④镁与酸的接触面积对该反应速率影响① 镁片 ② 25˚C 5% ③ 镁片 ④ 25˚C 5% 九年级化学解答题中等难度题查看答案及解析
-
化学兴趣小组的同学们用下列药品探究影响金属与酸反应速率的因素.
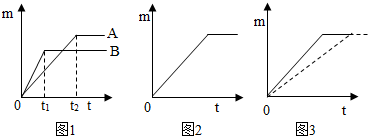
药品:锌片、铁片、镁片、5%的稀盐酸、20%的稀盐酸.
(一)不同金属与酸反应的快慢不同
取质量相等的上述两种金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图1所示.
(1)线A、B对应的金属分别为______、______.
结论:金属______,与盐酸反应的速率越快.
(二)金属与不同溶质质量分数的盐酸反应的快慢不同取质量相等的锌片,分别放入5%、20%的足量稀盐酸中.5%的稀盐酸与锌片反应生成氢气的质量(m)与反应时间(t)的关系曲线如图2所示.
(2)请在该图上补画出20%的稀盐酸与锌片反应m与 t的关系曲线.
结论:盐酸______,与金属反应的速率越快.
(三)温度对金属与盐酸反应速率也有影响
取质量相等的同种金属,分别放入溶质质量分数相同的20℃、50℃的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图3所示.
(3)请在该关系曲线图上标出相应的温度.
结论:温度______,金属与盐酸反应的速率越快.
若你还能提出别的合理影响因素,请仿照上述例子简述实验方法和结论并画出生成氢气的质量(m)与反应时间(t)的关系曲线.______.(本题奖励4分,总分不超过60分)九年级化学解答题中等难度题查看答案及解析
-
化学兴趣小组的同学们用下列药品探究影响金属与酸反应速率的因素.
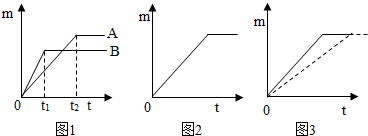
药品:锌片、铁片、镁片、5%的稀盐酸、20%的稀盐酸.
(一)不同金属与酸反应的快慢不同
取质量相等的上述两种金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图1所示.
(1)线A、B对应的金属分别为______、______.
结论:金属______,与盐酸反应的速率越快.
(二)金属与不同溶质质量分数的盐酸反应的快慢不同取质量相等的锌片,分别放入5%、20%的足量稀盐酸中.5%的稀盐酸与锌片反应生成氢气的质量(m)与反应时间(t)的关系曲线如图2所示.
(2)请在该图上补画出20%的稀盐酸与锌片反应m与 t的关系曲线.
结论:盐酸______,与金属反应的速率越快.
(三)温度对金属与盐酸反应速率也有影响
取质量相等的同种金属,分别放入溶质质量分数相同的20℃、50℃的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图3所示.
(3)请在该关系曲线图上标出相应的温度.
结论:温度______,金属与盐酸反应的速率越快.
若你还能提出别的合理影响因素,请仿照上述例子简述实验方法和结论并画出生成氢气的质量(m)与反应时间(t)的关系曲线.______.(本题奖励4分,总分不超过60分)九年级化学解答题中等难度题查看答案及解析
-
课外探究时,某兴趣小组同学选择了“金属和酸反应快慢与什么因素有关”课题.
(1)其他条件相同,同种金属与不同质量分数的盐酸反应,反应的快慢不同.取质量相等的铝片,分别放入5%、20%的足量稀盐酸中,实验表明盐酸浓度越大,反应速率越快.如图1中Ⅰ、Ⅱ、Ⅲ是三位同学记录实验生成氢气的质量(m)与反应时间(t)的关系曲线,其中正确的是 .
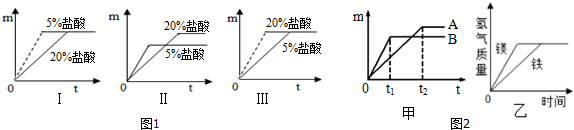
(2)其他条件相同,不同金属与相同质量分数的盐酸反应,反应的快慢不同.取质量相等的镁片、锌片、铁片中的两种金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图甲所示.则曲线A对应的金属与稀盐酸反应后生成的盐的名称是 .
(3)有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图乙所示.下列结果可能的是 (填序号).
①反应后镁有剩余 ②反应后铁有剩余
③反应后稀硫酸有剩余 ④反应后稀盐酸有剩余
⑤剩余铁的和镁的质量相等 ⑥消耗的稀硫酸和稀盐酸质量相等.
九年级化学探究题中等难度题查看答案及解析
-
(2005•广州)实验室现有下列药品:盐酸(5%)、硫酸(5%);大小相同的镁片、铝片、铁片;铁粉、铝粉、铁粉.某同学为了比较金属与酸的反应,按下图所示的实验方案进行实验.
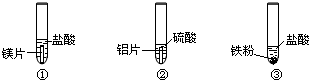
从实验开始到反应5分钟,所观察到的现象记录如下:
该同学根据上述实验现象得出结论:金属与酸反应的剧烈程度按镁、铁、铝的顺序减弱.编号 ① ② ③ 现象 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 金属表面慢慢有少量无色气泡冒出.反应到5分钟时,铝片还在冒气泡 铁粉中不断有无色气泡冒出.气泡的量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡
你认为该同学的结论是否合理(填“合理”或“不合理)______,如果有不合理的地方,请你在上述设计的基础上完善该实验,在下图中填写所需的化学药品;如果合理,可以不填.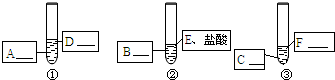
九年级化学解答题中等难度题查看答案及解析
-
实验室现有下列药品:盐酸(5%)、硫酸(5%);大小相同的镁片、铝片、铁片;铁粉、铝粉.某同学为了比较金属与酸的反应,按下图所示的实验方案进行实验.
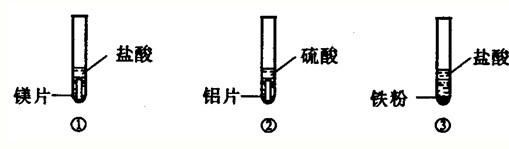
从实验开始到反应5分钟,所观察到的现象记录如下:
(1)写出实验③中的化学反应方程式______.编号 ① ② ③ 现象 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 金属表面慢慢有少量无色气泡冒出.反应到5分钟时,铝片还在冒气泡 铁粉中不断有无色气泡冒出.气泡的量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡
(2)该同学根据上述实验现象得出结论:金属与酸反应的剧烈程度按镁、铁、铝的顺序减弱.你认为该同学的结论是否合理(填“合理”或“不合理)______,如果有不合理的地方,请你在上述设计的基础上完善该实验,在图中填写所需的化学药品;如果合理,可以不填.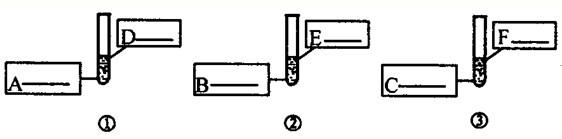
九年级化学解答题中等难度题查看答案及解析
-
实验室现有下列药品:盐酸(5%)、硫酸(5%);大小相同的镁片、铝片、铁片;铁粉、铝粉、铁粉.某同学为了比较金属与酸的反应,按下图所示的实验方案进行实验.
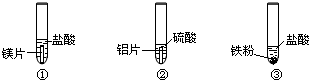
从实验开始到反应5分钟,所观察到的现象记录如下:
该同学根据上述实验现象得出结论:金属与酸反应的剧烈程度按镁、铁、铝的顺序减弱.编号 ① ② ③ 现象 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 金属表面慢慢有少量无色气泡冒出.反应到5分钟时,铝片还在冒气泡 铁粉中不断有无色气泡冒出.气泡的量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡
你认为该同学的结论是否合理(填“合理”或“不合理)______,如果有不合理的地方,请你在上述设计的基础上完善该实验,在下图中填写所需的化学药品;如果合理,可以不填.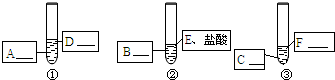
九年级化学解答题中等难度题查看答案及解析
-
实验室现有下列药品:盐酸(5%)、硫酸(5%);大小相同的镁片、铝片、铁片;铁粉、铝粉、铁粉.某同学为了比较金属与酸的反应,按下图所示的实验方案进行实验.
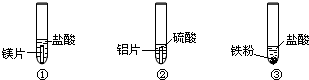
从实验开始到反应5分钟,所观察到的现象记录如下:
该同学根据上述实验现象得出结论:金属与酸反应的剧烈程度按镁、铁、铝的顺序减弱.编号 ① ② ③ 现象 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 金属表面慢慢有少量无色气泡冒出.反应到5分钟时,铝片还在冒气泡 铁粉中不断有无色气泡冒出.气泡的量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡
你认为该同学的结论是否合理(填“合理”或“不合理)______,如果有不合理的地方,请你在上述设计的基础上完善该实验,在下图中填写所需的化学药品;如果合理,可以不填.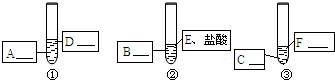
九年级化学解答题中等难度题查看答案及解析
-
为了探究金属与酸的反应,某兴趣小组进行了以下实验:
(1)A小组研究影响金属与酸反应剧烈程度的因素,如图时20℃时相同质量的铁粉、铁片、铝片分别与足量稀盐酸完全反应,产生氢气的质量与时间的关系图。

由此分析,归纳出影响金属与酸反应速率的因素有:金属的种类、_____和_____。
(2)金属铬(Cr)越来越受到人们的关注,B小组对Cr、Al、Cu的金属活动性顺序进行了探究,过程如下:
(提出假设)对三种金属的活动性顺序提出假设
a.Al>Cr>Cu b.Cr>Al>Cu c._____
(设计实验)同温下,取大小相同的金属薄片,分别投入到等体积、等浓度的足量稀盐酸中,观察现象,记录如下:
金属
Cr
Al
Cu
现象
反应缓慢,金属逐渐溶解
反应激烈,金属迅速溶解
无明显现象
(实验条件)实验前,打磨三种金属发生的是_____(填“物理”或“化学”)变化;上述实验使用等浓度的盐酸溶液的理由是_____。
(得出结论)原假设中正确的是_____(填假设中a、b或c),写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式_____。
九年级化学科学探究题困难题查看答案及解析