-
氯碱工业的反应原理是电解NaCl水溶液,下列物质不可能是氯碱工业产品的是( )
A.Na2CO3 B.Cl2 C.H2 D.NaOH
九年级化学单选题简单题查看答案及解析
-
氯碱工业的反应原理是电解NaCl水溶液,下列物质不可能是氯碱工业产品的是( )
A.Na2C03 B.Cl2 C.H2 D.NaOH
九年级化学选择题中等难度题查看答案及解析
-
氯碱工业的反应原理是电解饱和食盐水,下列物质不可能是氯碱工业产品的是
A.H2 B.Cl2 C.Na2CO3 D.NaOH
九年级化学选择题中等难度题查看答案及解析
-
氯碱工业的反应原理是电解饱和食盐水,下列物质不可能是氯碱工业产品的是( )
A. H2 B. Cl2 C. Na2CO3 D. NaOH
九年级化学单选题中等难度题查看答案及解析
-
氯碱工业的反应原理是电解饱和食盐水,下列物质不可能是氯碱工业产品的是( )
A.H2
B.Cl2
C.Na2CO3
D.NaOH九年级化学选择题中等难度题查看答案及解析
-
氯碱工业是最基本的化学工业之一,是指工业上用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品。反应原理是:
2NaCl + 2H2O
2NaOH + Cl2↑ + H2↑
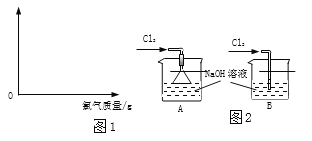
(1)工业上电解浓度为26.5%的饱和工业盐水200t,则生产氯气的质量是多少_____?(精确到0.1)
(2)取电解生产的氯气71g,通入到一定浓度的NaOH溶液中制备漂白液(主要成分为盐NaClO),反应原理为:Cl2 + 2NaOH = NaClO + NaCl + H2O。请在图1坐标中画出相应的曲线图(纵坐标为盐的质量,请设定具体物质,并标出曲线中必要的数据_____)。
(3)图2是实验室制备漂白液的部分装置。最好选用的装置是_____(填序号),理由_____。
九年级化学计算题困难题查看答案及解析
-
“氯碱工业”是我国目前化学工业的重要支柱之一,它的主要原理是电解饱和食盐水,其化学方程式为xNaCl+2H2O
xNaOH+H2↑+Cl2↑.在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g.已知:20℃时,NaC1的溶解度为36g.
请分析并计算回答:
(1)运用质量守恒定律可知上述反应中x= .
(2)通过计算,上述过程中同时产生H2的质量为 g.
(3)计算电解后剩余溶液中NaC1的质量分数(写出详细的计算过程,结果精确到0.1%).
九年级化学计算题极难题查看答案及解析
-
氯碱工业是指用电解饱和NaCl溶液的方法来抽取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,电解饱和NaCl溶液的化学方程式为:
,请计算:
(1)烧碱中三种元素的质量比m(Na):m(O): m(H)= 。
(2)用这种方法制备40t烧碱,需要NaCl的质量为 。
(3)若用25%的NaCl溶液按照上述方法电解并制取40t烧碱,完全电解后所得溶液的质量分数。( 假设生成的烧碱全溶,计算时若除不尽保留到1%) .
九年级化学计算题中等难度题查看答案及解析
-
(10分)“氯碱工业”是我国目前化学工业的重要支柱之一,它的主要原理是电解饱和食盐水,其化学方程式为: x NaCl+ 2 H2O
x NaOH+ H2↑+ Cl2↑。在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g。(已知:20℃时,NaC1的溶解度为36g)请分析并计算回答:
(1)运用质量守恒定律可知上述反应中x= 。
(2)通过计算,上述过程中同时产生H2的质量为 g。
(3)计算电解后剩余溶液中NaC1的质量分数(写出详细的计算过程,结果精确到0.1%)。
九年级化学计算题困难题查看答案及解析
-
某氯碱化工厂以电解食盐水产生化工原料氢氧化钠(反应原理为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑).若电解含氯化钠23.4t的食盐水,理论上可得到多少氢氧化钠?
九年级化学解答题中等难度题查看答案及解析