-
某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备绿矾(FeSO4·xH2O),工艺流程如下图所示::
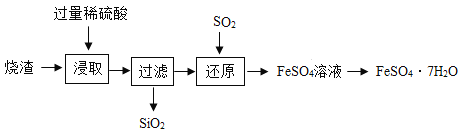
资料1: SiO2不溶于水,也不与稀硫酸反应;
资料2: +2价的铁元素容易被空气中的氧气氧化。
(1)“浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式为:FeO+ H2SO4= FeSO4+ H2O、_________,为提高“浸取”步骤的反应速率,除了采取“搅拌”和“使用催化剂”外,还可采取的具体措施有________(写1条)。
(2)“浸取”、“过滤”步骤后,滤液中的溶质有_________。
(3)“还原”转化的化学反应原理为:SO2+Fe2(SO4)3+2H2O=2FeSO4+2H2SO4,该步骤的主要目的是______。
(4)FeSO4溶液经过蒸发浓缩、______________、过滤、洗涤、低温干燥后得到FeSO4·xH2O晶体;低温干燥的目的是______________。
(5)以上结晶过程最好在氮气环境中进行,氮气的作用是___________。
-
绿矾(FeSO4·7H2O)是一种重要的食品添加剂。某工厂产生的炉渣主要含有FeO和Fe2O3,还有一定量的SiO2(SiO2不溶于水、不与稀硫酸反应)。实验室以此炉渣制备绿矾的流程如下:
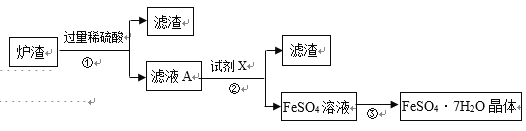
(1)步骤①实验时需用到的玻璃仪器是___________、玻璃棒和烧杯。该过程发生反应的化学方程式为:①FeO+H2SO4=FeSO4+H2O,②__________________。
(2)滤液A中含有的溶质有FeSO4、_______________。
(3)加入试剂X的目的是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。
①若试剂X是SO2,转化原理为SO2+Fe2(SO4)3+2H2O=2FeSO4+2Y,则Y的化学式是__________。
②若试剂X是Fe,转化原理为Fe+ Fe2(SO4)3=3FeSO4。测得反应后溶液的pH明显增大,其原因是__________________。
(4)步骤③的操作是蒸发浓缩、___________、过滤,即得到绿矾晶体。
-
某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备七水合硫酸亚铁晶体(FeSO4 ·7H2O),其工艺流程如下:
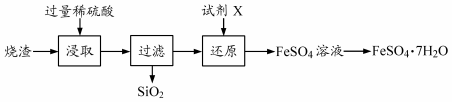
查阅资料:SiO2不溶于水,也不与稀硫酸反应。
(1)“浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式分别为
FeO+H2SO4=FeSO4+ H2O 、________________。
(2)为提高“浸取”步骤的反应速率,可采取的具体措施有______________(写2条,不考虑“搅拌”和 “使用催化剂”)。
(3)“还原”步骤的日的是将Fe抖转化为Fe2+,试剂X可用SO2或Fe。
①若试剂X是SO2,转化原理为SO2+Fe2 (SO4)3+2Y =2FeSO4+2H2SO4,则Y的化学式是_________。
②若试剂X是Fe,转化原理为Fe+Fe2 (SO4)3=3FeSO4。测得“还原”后溶液的pH明显增大,其原因是______ 。
-
某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备七水合硫酸亚铁晶体(FeSO4 ·7H2O),其工艺流程如下:
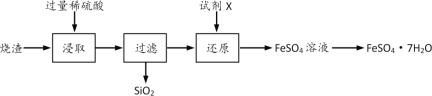
查阅资料:SiO2不溶于水,也不与稀硫酸反应。
⑴ “浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式分别为FeO+H2SO4=FeSO4+H2O、__________________。
⑵ 过滤用到的玻璃仪器有______________。
⑶ “还原”步骤是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。
① 若试剂X是SO2,转化原理为SO2+Fe2(SO4)3+2H2O=2FeSO4+2Y,则Y的化学式是:____________。
② 若试剂X是Fe,转化原理的化学方程式为______________________。
测得“还原”后溶液的pH明显增大,其原因是______________________。
-
某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备七水合硫酸亚铁晶体(FeSO4•7H2O),其工艺流程如下:
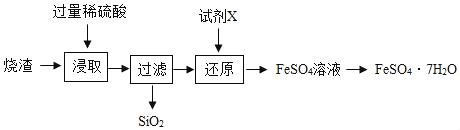
查阅资料:SiO2不溶于水,也不与稀硫酸反应。
(1)“浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式分别为FeO+H2SO4=FeSO4+H2O、________________________________。
(2)为提高“浸取”步骤的反应速率,可采取的具体措施有___________________(写2条,不考虑“搅拌”和“使用催化剂”)。
(3)“还原”步骤的目的是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。
①若试剂X是SO2,转化原理为SO2+Fe2 (SO4)3+2Y═2FeSO4+2H2SO4,则Y的化学式是________。
②若试剂X是Fe,转化原理为Fe+Fe2 (SO4)3=3FeSO4.测得“还原”后溶液的pH明显增大,其原因是__________________________________。
-
某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备七水合硫酸亚铁晶体(FeSO4•7H2O),其工艺流程如下:
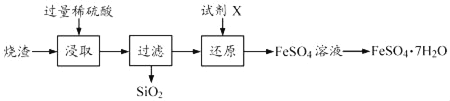
查阅资料:SiO2不溶于水,也不与稀硫酸反应。
(1)“浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式分别为FeO+H2SO4=FeSO4+H2O、_____。
(2)为提高“浸取”步骤的反应速率,可采取的具体措施有_____(写1条,不考虑“搅拌”和“使用催化剂”)。
(3)“过滤”操作需要使用的玻璃仪器有烧杯、玻璃棒和_____,“过滤”后得到的滤液中的溶质有_____(填化学式)。
(4)“还原”步骤的目的是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。
①若试剂X是SO2,转化原理为SO2+Fe2 (SO4)3+2Y═2FeSO4+2H2SO4,则Y的化学式是_____。
②若试剂X是Fe,转化原理为Fe+Fe2 (SO4)3═3FeSO4.测得“还原”后溶液的pH明显增大,其原因是_____。
-
某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制七水合硫酸亚铁晶体(FeSO4•7H2O),其工艺流程如下:
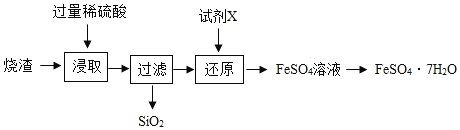
查阅资料:SiO2不溶于水,也不与稀硫酸反应。
(1)“浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式分别为FeO+H2SO4=FeSO4+H2O、________。
(2)为提高“浸取”步骤的反应速率,可采取的具体措施有________(写一条,不考虑“搅拌”和“使用催化剂”)。
(3)“还原”步骤的目的是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。若试剂X是Fe,转化原理为Fe+Fe2(SO4)3=3FeSO4。测得“还原”后溶液的pH明显增大,其原因是________。
(4)由FeSO4溶液得到FeSO4•7H2O的过程中包含蒸发、________等操作,其中蒸发操作中所需的玻璃仪器有酒精灯、________。
-
某工厂产生的废渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备氧化铁,流程如下图所示。

已知: SiO2既不溶于水,也不能与酸反应.双氧水能将Fe2+转化为Fe3+。
(1)在“酸溶”步骤中,FeO、Fe2O3和稀硫酸反应的化学方程式分别为:  、_______。
、_______。
(2)滤液Ⅰ中的溶质除FeSO4外,还有______(用化学式表示)。
(3)氨水在调节pH时会与硫酸反应,其化学反应方程式为_____。
(4)滤液Ⅱ中的盐可用作_______。
(5)氢氧化铁在加热条件下很容易分解产生氧化铁,化学反应方程式为_____。
-
某工厂生产的烧渣(主要含有FeO、Fe2O3和SiO2),可用于制备七水合硫酸亚铁晶体(FeSO4•7H2O),其工艺流程如下:
(资料:SiO2不溶于水,也不与稀硫酸反应。)
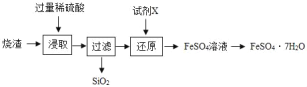
(1)“浸取”步骤中,发生反应的化学方程式有_____,Fe2O3+3H2SO4=Fe2(SO4)3+3H2O。
(2)为提高“浸取”步骤的反应速率,可采取的具体措施有_____(写1条,不考虑“搅拌”、“使用催化剂”)
(3)“还原”的目的是将Fe3+转化为Fe2+.写出“还原”过程中反应的化学反应方程式_____。
(4)该工艺中可循环利用的物质是_____。
-
某工厂生产的烧渣(主要含有FeO、Fe2O3和SiO2),可用于制备七水合硫酸亚铁晶体(FeSO4·7H2O),其工艺流程如下:
(资料:SiO2不溶于水,也不与稀硫酸反应。)

(1)“浸取”步骤中,发生反应的化学方程式有_________、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O。
(2)为提高“浸取”步骤的反应速率,可采取的具体措施有_________________(写1条,不考虑“搅拌”、“使用催化剂”)
(3)“还原”的目的是将Fe3+转化为Fe2+。写出“还原”过程中反应的化学反应方程式________________。
(4)该工艺中可循环利用的物质是__________________。









