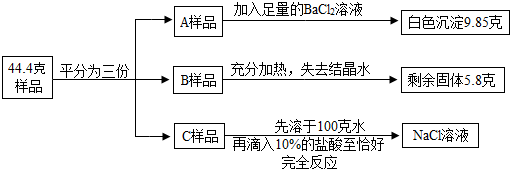
(1)将A样品与BaCl2溶液反应生成的白色沉淀分离出来的方法是______.
(2)A样品中与BaCl2溶液反应的Na2CO3的质量是______克.
(3)B样品中含有结晶水的质量是______克.
(4)化学式Na2CO3•nH2O中n是多少?
(5)对C样品的操作结束后,所得NaCl溶液的溶质质量分数是多少?(精确到0.01%)
九年级化学解答题中等难度题

九年级化学解答题中等难度题

九年级化学解答题中等难度题查看答案及解析
将质量为44.4克含有少量NaCl 的纯碱晶体(Na2CO3•nH2O)样品,平均分成A、B、C三份,进行如图实验(Na2CO3受热不分解)。
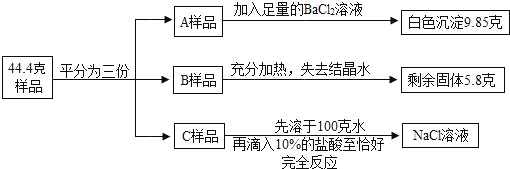
(1)将A样品与BaCl2溶液反应生成的白色沉淀分离出来的方法是_____。
(2)A样品中与BaCl2溶液反应的Na2CO3的质量是_____克。
(3)B样品中含有结晶水的质量是_____克。
(4)化学式Na2CO3•nH2O中n是_____
(5)对C样品的操作结束后,所得NaCl溶液的溶质质量分数是多少_____?(精确到0.01%)
九年级化学计算题中等难度题查看答案及解析
为测定某含有少量NaCl的纯碱晶体(Na2CO3•nH2O)样品的组成,做了如下实验:

根据实验数据进行计算,写出计算过程。
(1)样品中含有结晶水的质量是 克。
(2)原混合物中NaCl与纯碱晶体(Na2CO3•nH2O)的质量比 。
(3)化学式Na2CO3• nH2O中n= 。
九年级化学计算题极难题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
纯碱产品中常含有少量的氯化钠杂质,在实验室中取50g纯碱样品,平均分成五份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为30g),每次充分反应后都进行称量,得到的实验数据如表:
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 10 | 10 | 10 | 10 | 10 |
| 电子天平的示数/g | 137.8 | a | 153.4 | 161.2 | 171.2 |
(1)a的值为_____。
(2)计算纯碱样品中碳酸钠的质量_____。
(3)计算所用稀盐酸的溶质质量分数_____。
九年级化学计算题困难题查看答案及解析
工业上侯氏制碱法得到的纯碱产品中常含有少量的氯化钠杂质,化验员要对每批次的纯碱产品进行检验.在实验室中取27g纯碱样品,平均分成五份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后都进行称量,得到的实验数据如下表: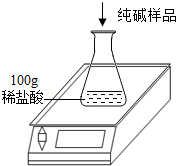
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 电子天平的示数/g | 163.2 | 166.4 | 169.6 | 175 | 180.4 |
(1)第一次加入纯碱样品充分反应后,生成二氧化碳的质量是________g.
(2)计算纯碱样品中碳酸钠的质量分数是多少?(计算结果精确到0.1%)
(3)计算所用稀盐酸的质量分数是多少?
九年级化学计算题困难题查看答案及解析
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 电子天平的示数/g | 163.2 | 166.4 | 169.6 | 175 | 180.4 |
九年级化学解答题中等难度题查看答案及解析
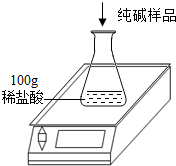
工业上侯氏制碱法得到的纯碱产品中常含有少量的氯化钠杂质,化验员要对每批次的纯碱产品进行检验.在实验室中取27g纯碱样品,平均分成五份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后都进行称量,得到的实验数据如下表: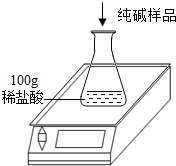
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 电子天平的示数/g | 163.2 | 166.4 | 169.6 | 175 | 180.4 |
(1)第一次加入纯碱样品充分反应后,生成二氧化碳的质量是________g.
(2)计算纯碱样品中碳酸钠的质量分数是多少?(计算结果精确到0.1%)
(3)计算所用稀盐酸的质量分数是多少?
九年级化学计算题困难题查看答案及解析
(8分)工业上侯氏制碱法制得的纯碱产品中常含有少量的氯化钠杂质,化验员要对每批次的纯碱产品进行检验。在实验室中取27g纯碱样品,平均分成五份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后都进行称量,得到的实验数据如下表:
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 电子天平的示数/g | 163.2 | 166.4 | 169.6 | 175 | 180.4 |
(1)第一次加入纯碱样品充分反应后,生成二氧化碳的质量是 g。
(2)第 次加入纯碱样品后恰好与100g稀盐酸完全反应,此时共反应纯碱样品 g。
(3)计算纯碱样品中碳酸钠的质量分数是多少?(计算结果精确到0.1%)
九年级化学计算题中等难度题查看答案及解析
某化工厂生产的纯碱中含有少量NaCl杂质,其产品包装袋上标有:碳酸钠≥96%.为了证实该产品中碳酸钠的含量,某同学取12g该样品放入烧杯中,称得烧杯和样品总质量为132.0g再把100g稀盐酸平均分成4次加入烧杯中,每次充分反应后烧杯和剩余物总质量如下:(每次反应产生的CO2气体都全部从烧杯中逸出)
| 加入稀盐酸次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸质量/g | 25 | 25 | 25 | 25 |
| 充分反应后烧杯和剩余物总质量/g | 155.2 | 178.4 | 202.6 | 227.6 |
请你根据表中数据分析:①第1次充分反应后产生的CO2气体质量是 ________ g
②该产品中碳酸钠的质量分数是多少?该产品是否合格?(计算后回答,计算结果精确到0.1%)
九年级化学计算题困难题查看答案及解析