-
阅读下面科普短文。
日常生活中,很多人会用冰箱来保存一些吃剩的菜肴,隔一天甚至几天再吃。储存后菜肴中亚硝酸盐含量的变化引发人们的关注。
亚硝酸盐是一类化合物的总称,主要指亚硝酸钠(NaNO2),它是白色或淡黄色粉末,有咸味,易溶于水。蔬菜中一般都含有硝酸盐,含量较高的是茎叶类蔬菜、其次是根茎类蔬菜、然后是瓜类蔬菜,它们在煮熟后如果久置,硝酸盐就会被分解为亚硝酸盐。
实验人员准备了烧熟的蔬菜、牛肉,分别在常温和4℃冷藏条件下保存,48 h内测得亚硝酸盐含量,如下表所示。
时间变化
12 h
24 h
48 h
常温白菜/(mg/kg)
0.057
0.089
0.18
4℃白菜/(mg/kg)
0.037
0.057
0.057
常温胡萝卜/(mg/kg)
0.057
0.073
0.10
4℃胡萝卜/(mg/kg)
0.057
0.057
0.073
常温牛肉(mg/kg)
0.089
0.087
0.18
4℃牛肉(mg/kg)
0.067
0.089
0.089
实验结果表明,48 h内三种菜肴中亚硝酸盐含量均小于国家标准(肉类为3mg/kg、蔬菜为4mg/kg)。
亚硝酸盐本身并无致癌效应,它在胃中酸性环境下,易与氨基酸的分解产物发生反应,产生致癌物。当摄入维生素C时可以阻止致癌物产生。
人体对亚硝酸盐的一次性安全摄入量为每千克体重0.2mg。有数据显示,人体摄入的亚硝酸盐主要来自蔬菜。如果你体重50kg,即使一次性吃2.5kg蔬菜也是安全的。因此,将亚硝酸盐摄入量控制在安全范围内不会对人体造成危害。
依据文章内容,回答下列问题。
(1)亚硝酸钠的物理性质有______________________(写出一条)。
(2)煮熟蔬菜中的亚硝酸盐是由______________转化生成的。
(3)体重50kg的人对亚硝酸盐的一次性安全摄入量为_________mg。
(4)亚硝酸盐产生致癌物的原因是________________________。
(5)下列有关说法正确的是_________。
A.烧熟的白菜在常温储存时的亚硝酸盐含量高于4℃冷藏条件
B.常温储存条件下,烧熟的胡萝卜中的亚硝酸盐含量随存放时间呈增加趋势
C.适量吃富含维生素C的新鲜蔬菜水果,有利于抑制致癌物的产生
D.隔夜菜中因为富含亚硝酸盐,所以不能食用
九年级化学简答题简单题查看答案及解析
-
泡菜是我国北方人民广泛喜爱的一种菜肴,但在腌制过程中,由于一些硝酸盐还原菌的作用,会产生一定量的亚硝酸盐.某校自然科学课外研究小组为了了解泡菜在腌制过程中亚硝酸盐含量变化及其高峰期出现的时间,以及泡菜在加热煮熟状态下亚硝酸盐含量变化的情况进行了如下实验:
(1)选1、2、3号容量相同的泡菜坛,分别加入0.6kg的新鲜莲花菜;
(2)再在坛中加满煮沸过的质量分数为10%的NaCl溶液;
(3)封坛前分别测量各坛中液体未加热和煮沸后亚硝酸盐的含量;
(4)用水封坛,放在15~20°C环境中;
(5)以后每隔4天测量一次,直至泡菜腌熟能够食用为止,周期约为15天.所得数据见表1和表2.
表1 泡菜腌制过程中亚硝酸盐含量的变化(未加热)
表2 未加热和加热情况下亚硝酸盐含量的对比亚硝酸盐含量(mg/kg)
时间1号坛 2号坛 3号坛 封坛前 0.15 0.15 0.15 第4天 0.6 0.2 0.8 第8天 0.2 0.1 0.6 第12天 0.1 0.05 0.2 第16天 0.1 0.05 0.2
请根据上述情况,回答下列问题:亚硝酸盐含量(mg/kg)
时间未加热 加热煮沸后 1号坛 2号坛 3号坛 1号坛 2号坛 3号坛 封坛前 0.15 0.15 0.15 0.15 0.15 0.15 第4天 0.6 0.2 0.8 0.6 0.2 0.8 第8天 0.2 0.1 0.6 0.2 0.1 0.6 第12天 0.1 0.05 0.2 0.1 0.05 0.2 第16天 0.1 0.05 0.2 0.1 0.05 0.2
(1)在该项研究中,要取同样处置的3只坛的目的是什么?
(2)请根据表1中的数据,以时间为横坐标、亚硝酸盐含量为纵坐标,绘制3只坛内亚硝酸盐含量随时间变化的趋势图.
(3)根据曲线及表1、表2中的数据,你可以推理出什么结论?
(4)该项研究的设计存在着一个较明显的缺陷,你认为是什么?九年级化学解答题中等难度题查看答案及解析
-
阅读下面科普短文。
日常生活中,我们常饮用桶装水。网上盛传“千沸水”(指反复多次烧开的水)中含有大量亚硝酸盐,摄入一定量可导致中毒;此外,亚硝酸盐在人体内还能形成强致癌性物质-亚硝胺,饮用会致癌。这是真的吗?
水中亚硝酸盐主要来源于微生物的还原作用,适宜的温度会使水中的微生物增多,微生物释放出的还原酶可将水中的硝酸盐还原成亚硝酸盐。
童贵忠、董智军等人对微生物检测的实验:
取15种桶装水与饮水机装配好,分别测使用过程(动态)中不同时段水桶内的水样。取13种桶装水(不与饮水机装配)静态放置进行检测。检测结果如下表:
样品类别
动态实验样品(72小时)
静态实验样品(1个月)
数量
15
13
微生物超标数
14
2
微生物超标率/%
93.0
15.4
解释:使用过程中,随桶中水量的减少,空气进入水桶中也会带入许多空气中的微生物。加热时,桶内水温会达到微生物大量繁殖的适宜温度。
加热次数对亚硝酸盐含量是否有影响呢?我国在《GB 19298-2003瓶(桶)装饮用水卫生标准》中对亚硝酸盐(以NO2﹣计)的含量规定为小于5 μg/L。
邹伶俐、张雪娇等人的实验:
取新鲜的桶装水放置在饮水机上,测定36 h内反复加热(共计181次)的水样,亚硝酸盐含量(以NO2﹣计)检测结果如下表:
加热时间/h
含量/μg/L
0
0.67
1
0.73
3
1.12
6
1.23
12
1.81
24
2.44
36
3.53
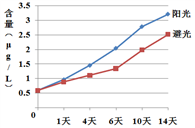
取检验合格的14桶桶装水分两组(每组7份)静态放置,进行存放环境检测,亚硝酸盐含量(以NO2﹣计)检测结果如图。
人在日常生活中主要摄取亚硝酸盐的途径是蔬菜,通过人体唾液的转化,间接进入人体的亚硝酸盐含量最高在300 mg/kg,人并没有因为食用蔬菜而导致亚硝酸盐中毒,由此可知“千沸水”中的亚硝酸盐不足以使人中毒。没有明确证据证明亚硝酸盐能致癌,在正确使用饮水机的前提下,“千沸水”不会致癌。反复煮沸的水,只是活性降低了,不易被人体细胞吸收。
依据文章内容,回答下列问题。
(1)水中亚硝酸盐主要来源于______。
(2)在使用过程中,桶装水内微生物的增多与大量繁殖与______有关。
(3)你认为“千沸水”可以饮用吗?说明理由______。
(4)依据图,静态放置时,影响桶装水中亚硝酸盐含量的因素有______。
(5)请你结合文章和生活实际,谈谈饮用桶装水时的注意问题______。
九年级化学简答题中等难度题查看答案及解析
-
阅读下面科普短文。
很多人畏甲醛如虎、谈甲醛色变,甚至希望生活在“零甲醛”的世界里,你真的了解甲醛吗?甲醛常温下易溶于水,其水溶液具有防腐杀菌功能,35% ~ 40%的甲醛水溶液俗称福尔马林,可用来浸制生物标本,给种子消毒等,但不能用于保鲜虾仁、鱿鱼等食品。在纺织品加工过程中,向助剂中添加甲醛,能防皱、防缩、防褪色等,但穿着或使用时会释放甲醛。《国家纺织产 品基本安全技术规范》(GB 18401-2010)规定纺织品甲醛最大残留量如下表:
项目
A类
B类
C类
甲醛含量(mg/kg)
20
75
300
甲醛可用于生产脲醛树脂、酚醛树脂、三聚氰胺-甲醛树脂等胶黏剂。这些胶黏剂生产工艺简单、性能良好、价格低廉,广泛应用于装修材料,但会缓慢释放出甲醛。我国室内空气质量标准(GB/T 18883-2002)规定,甲醛1小时均值浓度不得超过0. 10 mg/m3。下图是3个房子在7个时间点测定的甲醛均值浓度。
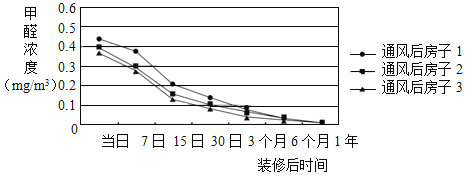
甲醛还能用于合成有机材料,这些材料性能优良,在工业机械、汽车制造、电子电器、日常用品等领域有广泛应用。现在你对甲醛一定有了新的认识!
依据文章内容回答下列问题。
(1)甲醛的物理性质有________________ (写出一条即可)。
(2)按照国家标准,B类衣服中甲醛的含量不得超过____________mg/kg。
(3)装修后的房子通风6个月,甲醛含量___________ (填“符合”或“不符合”)国家标准。
(4)下列说法正确的是____________ (填序号) 。
A通风换气可降低室内甲醛含量
B甲醛是防腐剂,但不能用于食品保鲜
C甲醛有百害而无一利,应禁用甲醛
九年级化学科普阅读题简单题查看答案及解析
-
阅读下面科普短文:
雾霾给我们的生活带来了很多困扰,柴静的一部纪录片《穹顶之下》引发了人们对于雾霾形成机理的关注,汽车尾气排放是产生雾霾的因素之一.
科学分析表明,汽车尾气中含有多种污染物,如固体悬浮微粒、一氧化碳、二氧化碳、碳氢化合物、氮氧化合物(NOx)等.目前最有效的汽车尾气治理方法是在发动机排气系统中加装催化转化器,在催化剂的作用下发生一系列反应,使CO、NOx、碳氢化合物三种有害物质较快地转化为对人体无害的CO2、N2和水蒸气(H2O),因此这种催化剂被称为三效催化剂(TWC).
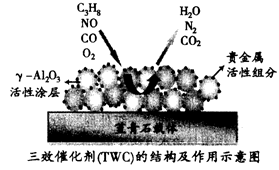
TWC通常是以贵金属铂、铑、钯为活性组分,它们是三效催化剂中其催化作用的主体.制作TWC时,将贵金属通过浸渍的方法分散在大比表面积的γ﹣Al2O3活性涂层上(“比表面积”指单位质量物料所具有的总面积),并将γ﹣Al2O3涂附在熔点达1350℃的堇青石载体上.
由此可见,催化转换器是安装在汽车排气系统中最重要的机外净化装置
依据文章内容,回答下列问题:
(1)堇青石的熔点是1350℃,该性质属于__(填“物理”或“化学”)性质
(2)三效催化剂主要由三部分组成,分别是γ﹣Al2O3活性涂层、__和___
(3)在催化转化器中发生一系列反应,其中一步是:一氧化氮和一氧化碳反应生成二氧化碳和空气中含量最多的气体,该反应的文字表达式为____
(4)机动车发动机排气系统中加装催化剂转化器的作用是____
九年级化学填空题简单题查看答案及解析
-
阅读下面科普短文。
雾霾给我们的生活带来了很多困扰,柴静的一部纪录片《穹顶之下》引发了人们对于雾霾形成机理的关注,汽车尾气排放是产生雾霾的因素之一。
科学分析表明,汽车尾气中含有多种污染物,如固体悬浮微粒、一氧化碳、碳氢化合物、氮氧化合物(NOx)等。目前有效的尾气治理方法是在汽车发动机排气系统中加装催化转化器,在催化剂的作用下发生一系列反应,使CO、碳氢化合物、NOx三种有害物质较快地转化为对人体无害的CO2 , N2和水蒸气(H2O),因此这种催化剂被称为三效催化剂(TWC)。
'I'WC通常是以贵金属铂、锗、把为活性组分,它们是三效催化剂中起催化作用的主体。制作TWC时,将贵金属通过浸渍的方法分散在比表面积较大的
一Al2O3活性涂层上黑(“比表面积”指单位质量物料所具有的总面积),并将
一Al2O3涂附在熔点达13500C董青石载体上。由此可见,催化转化器是安装在汽车排气系统中最重要的机外净化装置。
依据文章内容,回答下列问题:
(1)荃青石的熔点是13500C,该性质属于 (填“物理”或“化学”)性质。
(2)三效催化剂主要由三部分组成,分别是
一Al2O3活性涂层、 和
(3)在催化转化器中发生了一系列反应,其中的一步是:一氧化氮和一氧化碳反应生成了二氧化碳和空气中含量最多的气体,该反应的文字表达式为 。
(4)机动车发动机排气系统中加装催化转化器的作用是 。
(5)科学家一直积极致力于开发新型的活性组分,如采用Mn、Fe、Cu等金属为主要活性组分来取代贵金属,你认为该研发的优势是 。
九年级化学填空题中等难度题查看答案及解析
-
阅读下面科普短文:
亚硝酸盐广泛存在于自然环境和我们的生活中。在粮食、豆类,蔬菜、肉类、蛋类等食物中,都可以检测出一定量的亚硝酸盐,蔬菜中一般都含有硝酸盐,含量高的是茎叶类蔬菜、其次是根茎类蔬、然后是瓜类蔬菜,它们在煮熟后如果久置,硝酸盐就会被分解为亚硝酸盐。
大剂量的亚硝酸盐能够将人体内血红素中的铁元素由+2价氧化为+3价,从而使其失去携氧能力,引起全身组织缺氧,即产生亚硝酸盐中毒。当体内+3价铁血红蛋白达到20%-40%就会出现缺氧症状,达到70%以上可导致死亡。
亚硝酸盐控制在安全范围内使用,是不会对身体造成危害的,而且它对预防致命的肉毒梭菌中毒具有不可替代的作用。我国和许多国家都批准把亚硝酸盐作为食品添加剂以防止食品腐败,改进肉类颜色。亚硝酸盐与肌肉中的乳酸作用会产生亚硝胺,亚硝胺不稳定易分解产生一氧化氮,一氧化氮与肌红蛋白结合产生红色的亚硝基肌红蛋白,使肉制品产生稳定的红色。
为了测定煮熟后的蔬菜中亚硝酸盐含量,研究人员选用白菜进行了测定,实验1温度为20℃,实验2温度为13℃,实验中分别取放置2、4、6、8、10、12、24小时的熟白菜汁3滴,滴入1滴稀硫酸,再滴入2滴0.03%高锰酸钾溶液,若溶液的紫红色褪去,表示含有亚硝酸盐,实验记录见表:
时间/h
2
4
6
8
10
12
24
实验1
不褪色
不褪色
不褪色
由稍褪色到褪色且速度逐渐加快
实验2
不褪色
不褪色
不褪色
不褪色
不褪色
褪色且速度加快
依据文章内容,回答下列问题:
(1)高锰酸钾溶液中的溶质是______。(填化学式)
(2)亚硝酸盐使人体中毒的原因______。
(3)下列有关亚硝酸盐的说法正确的是______。(填字母序号)
A 煮熟蔬菜中的硝酸盐会被逐渐分解为亚硝酸盐
B 温度越低,熟蔬菜中亚硝酸盐产生的速率越快
C 亚硝酸盐与肌肉中的乳酸作用产生亚硝胺发生的是化学变化
D 我国规定食品中禁止添加亚硝酸盐
(4)根据实验现象,你对一次吃不完的熟蔬菜的建议是______。
九年级化学科普阅读题困难题查看答案及解析
-
阅读下面科普短文。
最近关于水果打蜡的报道很多,引发了许多疑问。
问题1:水果能打蜡吗?
根据中国《食品添加剂使用卫生标准》,允许使用规定的、适量的食用蜡对鲜水果进行处理。食用蜡原料主要来自于动植物,如蜂蜡、棕榈蜡等,蜂蜡中的主要成分为十六烷酸(C16H32O2)与三十烷醇(C30H62O)形成的脂类。人体少量接触食用蜡不会产生危害,偶尔食用也可排出体外。
问题2:为什么给水果打蜡?
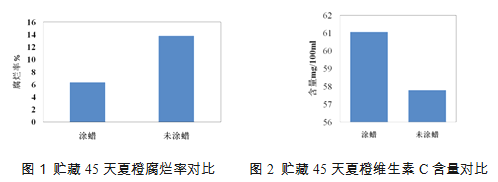
给水果打蜡最主要的目的是为了保鲜。下图是农科院王日葵等人对夏橙的研究结果。
问题3:如何分辨水果是否打了工业蜡?
用工业蜡加工水果,其中的重金属成分对人体会造成伤害。下面提供几种分辨方法。一是看,工业蜡多含有染色剂,使用湿纸巾擦拭水果表面,如有较重的颜色可能是工业蜡;二是闻,经工业蜡处理的水果会发出轻微的刺鼻味;三是刮,经工业蜡处理的水果用手指甲或水果刀一刮,会看到一层白色的蜡状物。
问题4:打蜡的水果如何清洗?
热水清洗:蜡遇热会熔化,把打蜡水果放到热水中,水中浮起一层蜡。
食盐洗:食盐的小颗粒能增强摩擦,也可以杀菌消毒。
另外,建议购买时令水果,少购买反季节及长途运输的水果,以减少买到打蜡水果的几率。
依据文章内容,回答下列问题。
(1)给水果打蜡的主要目的是______。
(2)研究人员对夏橙的研究,得出的结论是______。
(3)根据热水清洗,可以得出蜡的物理性质有______。
(4)C16H32O2与C30H62O两种物质具有的相同点是______。
九年级化学简答题简单题查看答案及解析
-
阅读下面科普短文。
葡萄是深受人们喜爱的水果之一。但由于葡萄果皮薄、果肉柔软,难以保存。葡萄的保鲜方法很多,常用的有冰温高湿保鲜法、SO2保鲜法等。
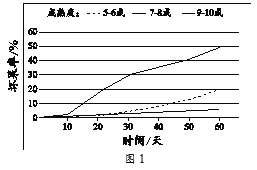
冰温高湿保鲜法。在贮藏过程中,葡萄中的糖(C6H12O6)、VC(C6H8O6)、水份等含量会因温度和湿度的波动而变化。将葡萄贮藏在其冻结点(0℃以下)的范围内、湿度保持在90%以上,能使其生理活性降至最低,从而达到保鲜的目的。采摘时的成熟度对葡萄的保鲜也有一定影响。研究人员以巨峰葡萄为研究对象,将温度和湿度控制在-1.5℃和95%,观察其坏果率(如图1)。
SO2保鲜法。SO2气体对葡萄贮藏中常见的真菌有抑制作用,还能降低葡萄的呼吸强度。但SO2使用时间过长,会对葡萄造成漂白伤害。
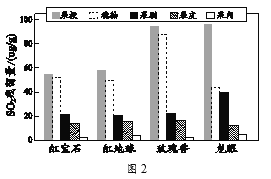
表1不同葡萄品种出现漂白伤害的时间(0℃)
红宝石
红地球
玫瑰香
龙眼
时间(天)
24
32
58
72
贮藏过程中,SO2会通过不同路径进入葡萄果肉。依据图2果皮中SO2的残留量明显高于果肉,推测出“果皮到果肉”是一条路径。
葡萄的保鲜方法很多,不同地区可根据当地气候、葡萄品种等因素,选择适宜的保鲜方法。
依据文章内容,回答下列问题。
(1)葡萄不易保存的原因是______(答1条即可)。
(2)葡萄中含有丰富的葡萄糖(C6H12O6)和VC(C6H8O6),两种物质中氧元素含量较高的是______。
(3)依据图1分析,将温度和湿度控制在-1.5℃和95%的条件下,影响巨峰葡萄坏果率的因素有______。
(4)由表1可知,在0℃贮藏60天不出现漂白伤害的葡萄品种为______。
(5)结合图2推测SO2进入果肉的另一路径是______(填序号,下同)。
A 穗轴→果梗→果刷→果肉
B 果刷→果梗→穗轴→果肉
C 果梗→穗轴→果刷→果肉
(6)下列说法不正确的是______。
ASO2对葡萄的贮藏有益无害
B葡萄的保鲜效果与温度、湿度无关
C葡萄的保鲜效果与葡萄品种有关
九年级化学科普阅读题中等难度题查看答案及解析
-
阅读下面科普短文。
牙膏是我们日常口腔清洁的必需品。依据添加剂的成分和含量不同,可将牙膏分为高磨擦剂含量牙膏和低磨擦剂含量牙膏,其主要数据如下表。
磨擦剂
保湿剂
香精
发泡剂
增稠剂
其他添加剂
高磨擦剂
含量牙膏
40%-50%
10%-30%
0.8%-1.8%
1.5%-3.0%
1%-2%
0.3%-6%
低磨擦剂
含量牙膏
15%-25%
35%-65%
0.85%-1.5%
1.0%-2.5%
0.2%-0.9%
0.3%-6%
其中,清洁牙齿主要通过磨擦剂来实现。其磨擦性取决于磨擦剂的形状、大小、硬度和含量。常见的磨擦剂有碳酸钙、二氧化硅和氢氧化铝[Al(OH)3]等。碳酸钙具有较高的磨擦性,硬度大,储量丰富,一般用来做经济型牙膏。二氧化硅的磨擦性较低,在使用过程中易于保护牙龈,适于老人及牙齿受损的人群。氢氧化铝分为普通氢氧化铝和球形氢氧化铝(如图1、2),它们具有白度高、光泽好等优点,但球形氢氧化铝的表面更加光滑,其生产工艺流程如图
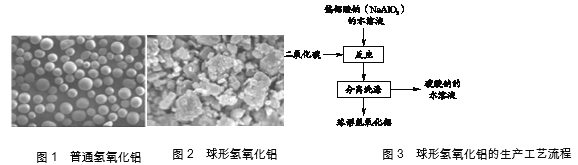
在实际生产中,通常会选用多种磨擦剂混合使用。例如,用二氧化硅和碳酸钙混合使用,既能保留牙膏对牙菌斑、牙结石的清洁效果,又可以避免其对牙齿的磨损。依据文章内容回答下列问题。
(1)碳酸钙中含有的非金属元素共______种。
(2)“高磨擦剂含量牙膏”的成分中,含量一定高于“低磨擦剂含量牙膏”的是______。
(3)影响磨擦剂磨擦性的因素有______。
(4)适用于老人及牙齿受损人群的磨擦剂是______。
(5)球形氢氧化铝的生产工艺流程中,反应物除NaAlO2外,还有______。
(6)下列说法正确的是______(填序号)。
A.通常多种磨擦剂混合使用比单独使用效果好
B.普通氢氧化铝比球形氢氧化铝对牙齿的磨损更小
C.选取磨擦剂时,除考虑磨擦性,还需考虑原料的成本
九年级化学填空题中等难度题查看答案及解析