-
⑴ 工业废料石膏(CaSO4•2H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下研究。
高纯CaO的制备
【资料卡】
Ⅰ.石膏(CaSO4•2H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅱ.无水硫酸铜遇水变成蓝色的硫酸铜晶体。
Ⅲ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊,还能被高锰酸钾溶液氧化而除去。
甲同学用如下装置制备CaO并验证石膏与焦炭高温反应的其他产物。
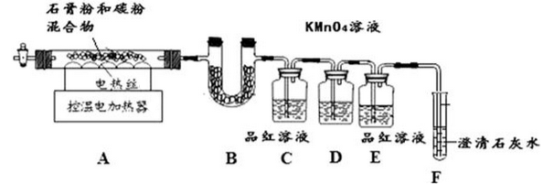
实验过程中发现:B中无水硫酸铜变蓝,__________________现象证明有SO2生成,装置D的作用________________,当观察到_____________现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:___________________。
⑵ 铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
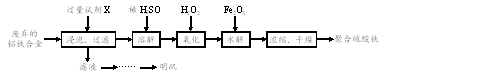
① 浸泡、过滤过程中加入过量的试剂X目的是_______。试剂X是一种常见的强碱,明矾是一种硫酸盐,化学式为KAl(SO4)2·12H2O。
② 聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型混凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
a 最适合作为混凝剂聚合硫酸铁的洗涤液为__________,选择该洗涤液的优点_______、_________。
b 请用含y的代数式表示x的数值:x =________。
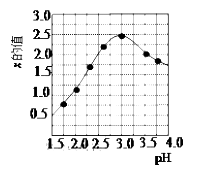
c 水解过程中,溶液的pH与x的关系如下图所示。溶液的pH=3.0时聚合硫酸铁中x的数值达到最大值。加入试剂 Fe2O3目的是__________。
-
工业废料石膏(CaSO4•2H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下系列研究。
一、高纯CaO的制备
【资料一】
Ⅰ.石膏(CaSO4•2H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅱ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊。
甲同学用如图1装置制备CaO并验证石膏与焦炭高温反应的其他产物。
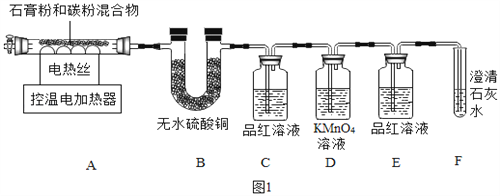
实验过程中发现:B中无水硫酸铜变蓝;C中产生__现象证明有SO2生成;装置__中无明显变化和装置F中__现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:____。
二、硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如图2:
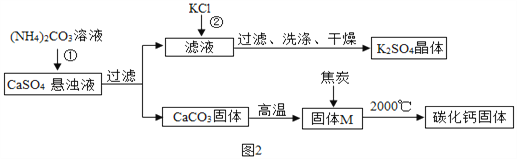
【资料二】CaO与C在高温下反应生成碳化钙(化学式为CaCx)和CO。
(1)反应①的化学方程式为___。证明固体M中不含CaCO3的方法是____(写出实验的方法、现象)。
(2)反应②的化学方程式为(NH4)2SO4+2KCl═K2SO4↓+2NH4Cl,该反应能析出K2SO4晶体的原因是__。
三、假设上述流程中制得的碳化钙(化学式为CaCx)固体中只含杂质CaO,乙小组同学为测定CaCx中x的值进行如下实验。
【资料三】CaCx在空气中灼烧生成CaO和CO2。
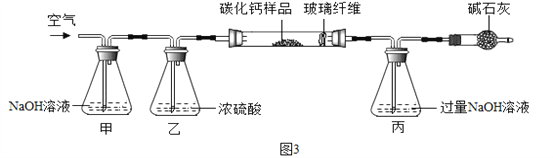
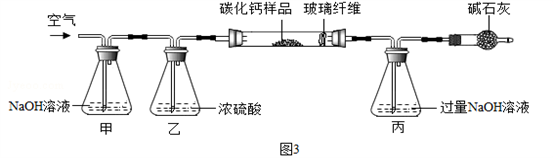
步骤一:称取3.76g样品于图3所示石英管中(测定装置图如图3,夹持及加热装置省略),反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气,测得丙溶液的质量比反应前增重了4.4g。(玻璃纤维可防止固体粉末进入导管)
步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、干燥等操作得到碳酸钙固体6克。试回答下列问题:
(1)装置甲的作用是__。反应完全后继续缓缓通入空气的目的是__。
(2)根据步骤一、二计算该样品中钙、碳、氧的质量比为___,
计算确定CaCx的化学式(请写出计算过程)______________。
(3)若碳酸钙未能完全干燥,则会导致CaCX中的x的值____(填“偏大”、“偏小”、“无影响”)。
-
工业废料石膏(CaSO4•2H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下系列研究。
一、高纯CaO的制备
【资料一】
Ⅰ.石膏(CaSO4•2H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅱ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊。
甲同学用如图1装置制备CaO并验证石膏与焦炭高温反应的其他产物。
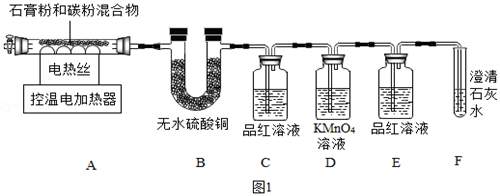
实验过程中发现:B中无水硫酸铜变蓝;C中产生__现象证明有SO2生成;装置__中无明显变化和装置F中__现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:____。
二、硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如图2:
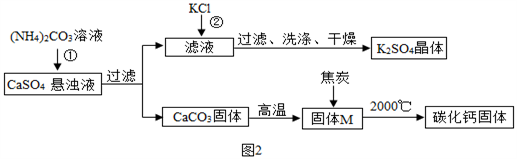
【资料二】CaO与C在高温下反应生成碳化钙(化学式为CaCx)和CO。
(1)反应①的化学方程式为___。证明固体M中不含CaCO3的方法是____(写出实验的方法、现象)。
(2)反应②的化学方程式为(NH4)2SO4+2KCl═K2SO4↓+2NH4Cl,该反应能析出K2SO4晶体的原因是__。
三、假设上述流程中制得的碳化钙(化学式为CaCx)固体中只含杂质CaO,乙小组同学为测定CaCx中x的值进行如下实验。
【资料三】CaCx在空气中灼烧生成CaO和CO2。
步骤一:称取3.76g样品于图3所示石英管中(测定装置图如图3,夹持及加热装置省略),反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气,测得丙溶液的质量比反应前增重了4.4g。(玻璃纤维可防止固体粉末进入导管)
步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、干燥等操作得到碳酸钙固体6克。试回答下列问题:
(1)装置甲的作用是__。反应完全后继续缓缓通入空气的目的是__。
(2)根据步骤一、二计算该样品中钙、碳、氧的质量比为___,
计算确定CaCx的化学式(请写出计算过程)______________。
(3)若碳酸钙未能完全干燥,则会导致CaCX中的x的值____(填“偏大”、“偏小”、“无影响”)。
-
工业废料石膏(CaSO4•2H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下系列研究。
一.高纯CaO的制备
【资料一】
Ⅰ.无水硫酸铜遇水变成蓝色的硫酸铜晶体。
Ⅱ.石膏(CaSO4•2H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅲ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊,还能被高锰酸钾溶液氧化而除去。
甲同学用如下装置制备CaO并验证石膏与焦炭高温反应的其他产物。
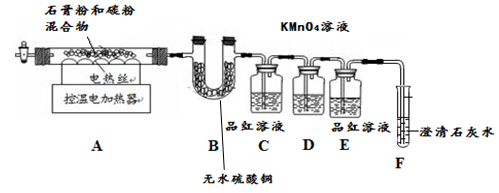
实验过程中发现:B中无水硫酸铜变蓝,C中产生_____________现象证明有SO2生成,装置_____中无明显变化和装置F中_____________现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:___________________。
二.硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如下:
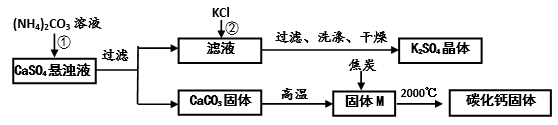
【资料二】氧化钙与焦炭在高温下反应生成碳化钙和一氧化碳。
(1)反应①的化学方程式为__________________________。证明固体M中不含CaCO3的方法是____________________________(写出实验的方法、现象)。
(2)反应②的化学方程式为(NH4)2SO4 + 2KCl ═ K2SO4↓+ 2NH4Cl,该反应能析出K2SO4晶体的原因是_____________________________________。
(3)假设上述流程中制得的碳化钙(化学式为CaCx)固体中只含杂质CaO,乙小组同学为测定CaCx中x的值进行如下实验。
【资料三】碳化钙在空气中灼烧生成氧化钙和二氧化碳气体。
步骤一:称取3.76g样品于下图所示石英管中(测定装置图如下,夹持及加热装置省略),反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气,测得丙溶液的质量比反应前增重了4.4g。(玻璃纤维可防止固体粉末进入导管)
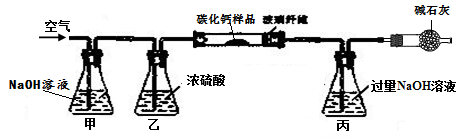
步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、干燥等操作得到碳酸钙固体6克。试回答下列问题:
①装置甲的作用是_______。反应完全后继续缓缓通入空气的目的是_________。
②根据步骤一、二计算该样品中钙、碳、氧的质量比为______________,计算确定CaCx的化学式(请写出计算过程)________。
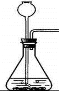
③应用:丙同学经查阅资料知道实验室常用电石(主要成分为碳化钙)与水反应制取乙炔气体(发生装置如图)。经实验发现,电石与水反应非常剧烈,为控制反应的速度以得到平稳的气流,下列改进方法可行的是______。
A.改长颈漏斗为分液漏斗或注射器 B.将电石研成粉末
C.将锥形瓶置于冰水浴中 D.用饱和食盐水代替水(电石与氯化钠不反应)
-
工业废料石膏(CaSO4•2H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下系列研究。
一.高纯CaO的制备
【资料一】
Ⅰ.无水硫酸铜遇水变成蓝色的硫酸铜晶体。
Ⅱ.石膏(CaSO4•2H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅲ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊,还能被高锰酸钾溶液氧化而除去。
甲同学用如下装置制备CaO并验证石膏与焦炭高温反应的其他产物。
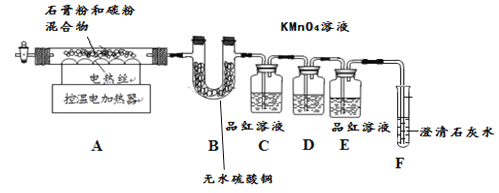
实验过程中发现:B中无水硫酸铜变蓝,C中产生_____________现象证明有SO2生成,装置_____中无明显变化和装置F中_____________现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:___________________。
二.硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如下:
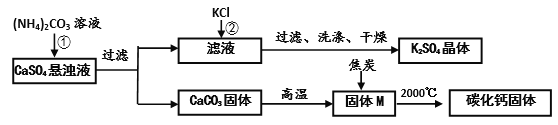
【资料二】氧化钙与焦炭在高温下反应生成碳化钙和一氧化碳。
(1)反应①的化学方程式为________________。证明固体M中不含CaCO3的方法是____________________(写出实验的方法、现象)。
(2)反应②的化学方程式为(NH4)2SO4 + 2KCl ═ K2SO4↓+ 2NH4Cl,该反应能析出K2SO4晶体的原因是_______________。
(3)假设上述流程中制得的碳化钙(化学式为CaCx)固体中只含杂质CaO,乙小组同学为测定CaCx中x的值进行如下实验。
【资料三】碳化钙在空气中灼烧生成氧化钙和二氧化碳气体。
步骤一:称取3.76g样品于下图所示石英管中(测定装置图如下,夹持及加热装置省略),反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气,测得丙溶液的质量比反应前增重了4.4g。(玻璃纤维可防止固体粉末进入导管)
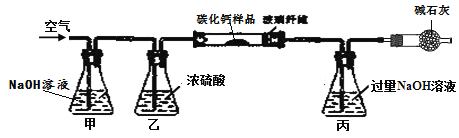
步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、干燥等操作得到碳酸钙固体6克。试回答下列问题:
①装置甲的作用是_______。反应完全后继续缓缓通入空气的目的是_________。
②根据步骤一、二计算该样品中钙、碳、氧的质量比为______________,计算确定CaCx的化学式(请写出计算过程)________。
③应用:丙同学经查阅资料知道实验室常用电石(主要成分为碳化钙)与水反应制取乙炔气体(发生装置如图)。经实验发现,电石与水反应非常剧烈,为控制反应的速度以得到平稳的气流,下列改进方法可行的是______。
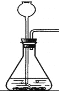
A.改长颈漏斗为分液漏斗或注射器 B.将电石研成粉末
C.将锥形瓶置于冰水浴中 D.用饱和食盐水代替水(电石与氯化钠不反应)
-
工业废料石膏 可以“变废为宝”,用于生产氧化钙、硫酸钾、电石等。某研究性学习小组展开了如下系列研究:
可以“变废为宝”,用于生产氧化钙、硫酸钾、电石等。某研究性学习小组展开了如下系列研究:
一、高纯CaO的制备
(资料一)
Ⅰ 无水硫酸铜遇水变成蓝色的硫酸铜晶体。
无水硫酸铜遇水变成蓝色的硫酸铜晶体。
Ⅱ 石膏
石膏 与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅲ 能使品红溶液褪色,也能使澄清石灰水变浑浊,还能被高锰酸钾溶液氧化而除去。
能使品红溶液褪色,也能使澄清石灰水变浑浊,还能被高锰酸钾溶液氧化而除去。
甲同学用如下装置制备CaO并验证石膏与焦炭高温反应的其他产物。
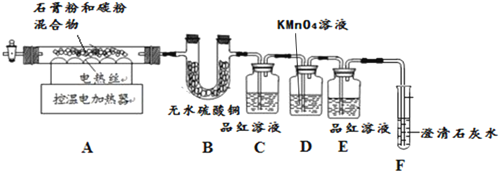
实验过程中发现:B中无水硫酸铜变蓝,说明有______生成;C中产生溶液褪色现象证明有 生成;装置______中无明显变化和装置F中______现象证明有
生成;装置______中无明显变化和装置F中______现象证明有 生成。写出石膏与碳粉在高温条件下反应的化学方程式:______。
生成。写出石膏与碳粉在高温条件下反应的化学方程式:______。
二、硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如下:
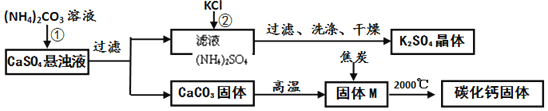
(资料二)常温下, 能溶于水,温度升高,溶解度变大;
能溶于水,温度升高,溶解度变大;
氧化钙与焦炭在高温下反应生成碳化钙和一氧化碳。
 反应
反应 的化学方程式为______。证明固体M中不含
的化学方程式为______。证明固体M中不含 的方法是______
的方法是______ 写出实验的方法、现象
写出实验的方法、现象 。
。
 反应
反应 的化学方程式为
的化学方程式为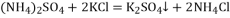 ,为得到纯净的硫酸钾晶体,洗涤反应
,为得到纯净的硫酸钾晶体,洗涤反应 所得晶体是必不可少的步骤。但工业上不用水而用饱和
所得晶体是必不可少的步骤。但工业上不用水而用饱和 溶液洗涤反应
溶液洗涤反应 所得晶体,其目的是______。
所得晶体,其目的是______。
三、研究 加热分解的产物
加热分解的产物
 工业废料
工业废料 中含有
中含有 ,为了测定
,为了测定 和
和 的质量比x:y,实验小组利用如下图所示的装置
的质量比x:y,实验小组利用如下图所示的装置 夹持仪器省略
夹持仪器省略 进行实验:
进行实验:
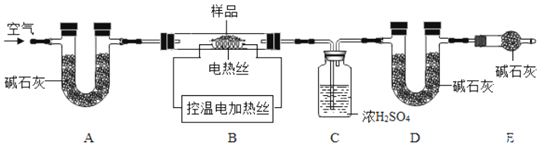
(资料三)碱石灰为固体氢氧化钠和氧化钙的混合物。可吸收水蒸气或二氧化碳。
 实验前首先要______,再装入样品。装置A的作用是______。
实验前首先要______,再装入样品。装置A的作用是______。
 已知
已知 在
在 生成
生成 ,
, 时
时 开始分解;
开始分解; 在
在 时分解完全。现控制B装置温度
时分解完全。现控制B装置温度 进行实验并采集了如下数据:
进行实验并采集了如下数据:
 反应前玻璃管与样品的质量m1g
反应前玻璃管与样品的质量m1g  反应后玻璃管中固体的质量为m2g
反应后玻璃管中固体的质量为m2g
 装置C实验后增重m3g
装置C实验后增重m3g  装置D实验后增重m4g
装置D实验后增重m4g
某同学选用c、d数据组合求出x:y的值,若无装置E,则实验测定结果将______ 填“偏大”、“偏小”或“无影响”
填“偏大”、“偏小”或“无影响” 。
。
 受热会逐步失去结晶水。
受热会逐步失去结晶水。
取纯净 固体
固体 ,放在
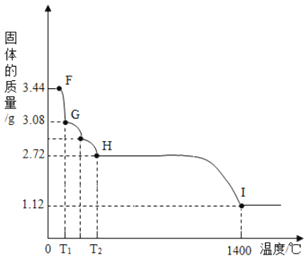
,放在 的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示。
的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示。 点固体的化学式是______。请写出计算过程。
点固体的化学式是______。请写出计算过程。
-
化工生产上通常将石膏(CaSO4)转化为硫酸钾肥料和氯化钙,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下是该转化的流程图。
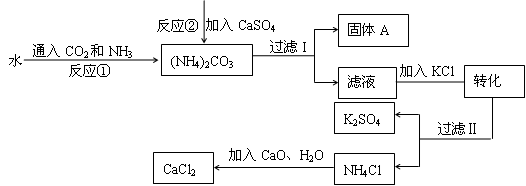
回答下列问题:
(1)写出反应①的化学方程式。
(2)过滤I操作所得固体中,出CaSO4外还含有________(填化学式)等物质。
(3)过滤I操作所得滤液是溶液(NH4)2SO4。检验滤液中是否还含有CO32—的方法是________。
(4)已知不同温度下K2SO4的溶解度如下表:
| 温度(℃) | 0 | 20 | 60 |
| 溶解度(g) | 7.4 | 11.1 | 18.2 |
60℃时K2SO4的饱和溶液591g冷却到0℃,可析出K2SO4固体________g。
-
某烟气脱硫的工艺不仅能消除SO2,还能将其转化为石膏(CaSO4•2H2O)等产品,实现“变废为宝”。(提示SO2化学性质与CO2相似)主要物质转化关系如图。
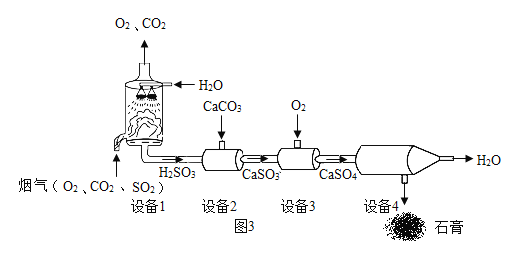
(1)设备4中经过_____操作,将水和石膏固体进行分离。
(2)设备1的作用是通过喷淋水脱去烟气中的SO2,该反应的化学方程式为_____。该处水采用喷淋而不是自由流下的目的是_____。
(3)若将二氧化硫气体通入紫色的石蕊溶液中,猜想可能出现的现象是_____。
(4)脱硫工艺流程中,可以循环利用的物质是_____。
-
某烟气脱硫的工艺不仅能消除SO2,还能将其转化为石膏(CaSO4•2H2O)等产品,实现“变废为宝”。(提示SO2化学性质与CO2相似)主要物质转化关系如图。
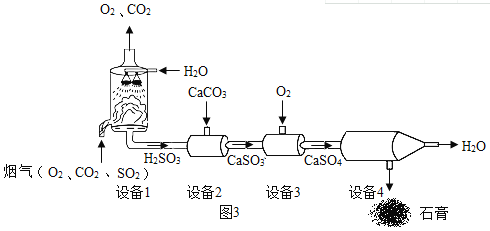
(1)设备4中经过_____操作,将水和石膏固体进行分离。
(2)设备1的作用是通过喷淋水脱去烟气中的SO2,该反应的化学方程式为_____。该处水采用喷淋而不是自由流下的目的是_____。
(3)若将二氧化硫气体通入紫色的石蕊溶液中,猜想可能出现的现象是_____。
(4)脱硫工艺流程中,可以循环利用的物质是_____。
-
某烟气脱硫的工艺不仅能消除SO2,还能将其转化为石膏(CaSO4•2H2O)等产品,实现“变废为宝”.主要物质关系如图:
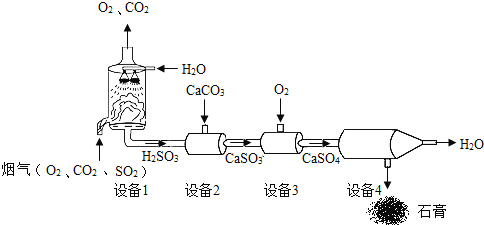
(1)设备1中,通过喷淋水脱去烟气中的SO2,该反应的化学方程式为 ______ .
(2)设备2中,加入CaCO3的目的是将H2SO3转化为 ______ .
(3)设备3中,反应前后化合价发生改变的元素是 ______ .
(4)流程中能循环利用的物质是 ______ .



















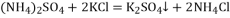 ,为得到纯净的硫酸钾晶体,洗涤反应
,为得到纯净的硫酸钾晶体,洗涤反应




