-
创新发展材料技术可推动人类社会进步。
(1)碱式碳酸铝镁[AlaMgb(OH)c(CO3)·xH2O]既可以用作抗酸药,也常用于制作阻燃材料其化学式中的a、b、c、d需满足的代数关系式为_________________________________。
(2)城市建没需要大量的钢材、水泥、玻璃等建筑材料,水泥和玻璃属于_______________材料,钢筋混凝土属于_____________________材料。
(3)纳米TiO2是一种性能优良的光催化剂,可将其制成环保涂料涂覆于建筑物表面,利用光催化作用产生的活性氧(O3)和雨水使空气中的SO2转化为H2SO4,并吸附在催化剂表面,从而改善城市空气质量。写出上述过程中发生反应的化学方程式_______。
九年级化学填空题困难题查看答案及解析
-
化学能帮助我们更好地认识物质世界、改善生活。
(1)创新发展材料技术可推动人类社会进步。
①石墨烯可用作太阳能电池的电极,这里主要利用了石墨烯的____性;
②2019年1月3日,嫦娥四号成功着陆在月球背面,所用的SiC颗粒增强铝基材料具有重量轻、高刚度、高耐磨、耐冲击等特点,该材料属于____(填字母);
a金属材料 b复合材料 c有机高分子材料
③高铁信息传输系统中使用的光导纤维,其主要成分是____(填字母);
a铜 b石墨 c二氧化硅
④基础工程建设中常用到水泥、玻璃、钢材等。钢材中添加铬、镍等元素的目的是__。
(2)紫薯营养丰富,具有特殊的保健功能。下表是100 g紫薯粉的营养成分含量表:
营养成分
含量
营养成分
含量
营养成分
含量
水分
9.9 g
淀粉
82.5 g
蛋白质
4.8 g
脂肪
0.2 g
铁元素
1.10 mg
钙元素
23.00 mg
硒元素
0.02 mg
其他
……
①紫薯中能为人体提供能量的营养物质为脂肪、淀粉和____;
②以上营养成分中____(填元素符号)是人体中含有的微量元素,____(填元素符号)摄入不足,会导致骨质疏松、佝偻病;
③在酶的作用下,淀粉先水解为葡萄糖,葡萄糖再转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式____。
九年级化学简答题简单题查看答案及解析
-
人类的生产生活离不开金属材料。
(1)铜和铁一样也可以生锈,铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3],是铜与空气中的氧气、水和________(填化学式)共同作用的结果。
(2)向铜锈中加入过量稀硫酸,固体逐渐溶解,得到蓝色硫酸铜溶液,从蓝色溶液中回收铜的过程如下:
 第
第①向蓝色溶液中加入过量铁粉,发生反应的化学方程式是_________________________;
②操作a是________。
九年级化学填空题简单题查看答案及解析
-
为纪念化学学科所取得的成就以及对人类文明的贡献,联合国将2011年定为“国际化学年”.请回答有关问题:
(1)材料的发展推动社会的进步,材料技术和应用与化学科学的发展密切相关,下列材料属于合成材料的是________(填序号)
a.不锈钢 b.聚乙烯塑料 c.高强度陶瓷 d.钢筋混凝土
(2)化学科学为防治环境污染发挥重大作用.例如,用纳米级的某种氧化物做催化剂,使汽车尾气中的两种有毒气体CO与NO反应转化为两种无毒气体,其中一种是空气中含量最多的气体.这两种气体是________和________.
(3)化学电源在生产、生活、科研中应用十分广泛.例如,银锌纽扣电池的反应原Zn+Ag2O+H2OZn(OH)2+2Ag理是:,该电池在使用时________能转化为电能.
(4)化肥的发明和使用,大大提高了全球的粮食产量,其中“合成氨技术”、“尿素生产技术”等功不可没,在加热、加压条件下,二氧化碳和氨气(NH3)反应生成尿素[CO(NH2)2]和水,该反应的化学方程式是________.九年级化学填空题中等难度题查看答案及解析
-
为纪念化学学科所取得的成就以及对人类文明的贡献,联合国将2011年定为“国际化学年”.请回答有关问题:
(1)材料的发展推动社会的进步,材料技术和应用与化学科学的发展密切相关,下列材料属于合成材料的是________(填序号)
a.不锈钢 b.聚乙烯塑料 c.高强度陶瓷 d.钢筋混凝土
(2)化学科学为防治环境污染发挥重大作用.例如,用纳米级的某种氧化物做催化剂,使汽车尾气中的两种有毒气体CO与NO反应转化为两种无毒气体,其中一种是空气中含量最多的气体.这两种气体是________和________.
(3)化学电源在生产、生活、科研中应用十分广泛.例如,银锌纽扣电池的反应原Zn+Ag2O+H2OZn(OH)2+2Ag理是:,该电池在使用时________能转化为电能.
(4)化肥的发明和使用,大大提高了全球的粮食产量,其中“合成氨技术”、“尿素生产技术”等功不可没,在加热、加压条件下,二氧化碳和氨气(NH3)反应生成尿素[CO(NH2)2]和水,该反应的化学方程式是________.九年级化学填空题中等难度题查看答案及解析
-
为纪念化学学科所取得的成就以及对人类文明的贡献,联合国将2011年定为“国际化学年”。请回答有关问题:
(1)材料的发展推动社会的进步,材料技术和应用与化学科学的发展密切相关,下列材料属于有机高分子材料的是________(填序号)。
a.不锈钢 b.聚乙烯塑料 c.钢化玻璃 d.钢筋混凝土
(2)化学科学为防治环境污染发挥重大作用。例如,用纳米级的某种氧化物做催化剂,使汽车尾气中的两种有毒气体CO与NO反应转化为两种无毒气体,其中一种是空气中含量最多的气体。这两种气体是________和________。
(3)化学电源在生产、生活、科研中应用十分广泛。例如,银锌纽扣电池的反应原理是:Zn+Ag2O+H2O
Zn(OH)2+2Ag,该电池在使用时________能转化为电能。
(4)化肥的发明和使用,大大提高了全球的粮食产量,其中“合成氨技术”、“尿素生产技术”等功不可没,在加热、加压条件下,二氧化碳和氨气(NH3)反应生成尿素[CO(NH2)2]和水,该反应的化学方程式是____________________________________________。
九年级化学填空题简单题查看答案及解析
-
(7分)孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料。某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理。

【查阅资料】
1.Cu2(OH)2CO3
2CuO+CO2 + H2O
2CuO+C
2Cu + CO2 ↑
2.CuO为黑色固体,化学性质和氧化铁相似。
(1)实验l:加热分解碱式碳酸铜。装置如图所示。
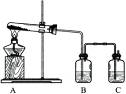
①A中固体的变化为____。
②欲证明反应后有水生成,B中所盛试剂为____。
③反应结束时的操作应该是____,理由是____。
(2)实验2:木炭和氧化铜反应。
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余。该小组同学设计方案验证黑色粉末的成分。
【作出猜想】
剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜。
【实验验证】填写下表。
实验操作及现象
实验结论
该黑色粉末为氧化铜
(3)某同学探究在实际反应中,木炭和氧化铜反应生成铜时反应物的最佳质量比,设计方案如下:
配方l
配方2
配方3
配方4
木炭质量(g)
0.4
0.5
0.6
0.7
氧化铜质量(g)
8
8
8
8
上述设计方案的主要研究方法是__________________。
九年级化学探究题简单题查看答案及解析
-
孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理.
查阅资料:①Cu2(OH)2CO32CuO+CO2↑+H2O 2CuO+C
2Cu+CO2↑
②CuO为黑色固体,化学性质和氧化铁相似.
(1)实验l:加热分解碱式碳酸铜.装置如图所示.
①A中固体的变化为________.
②欲证明反应后有水生成,B中所盛试剂为________.
③反应结束时的操作应该是________,理由是________.
(2)实验2:木炭和氧化铜反应.
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余.该小组同学设计方案验证黑色粉末的成分.
做出猜想:剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜.
实验验证:填写下表.
(3)某同学探究在实际反应中,木炭和氧化铜反应生成铜时反应物的最佳质量比,设计方案如下:实验操作及现象 实验结论 该黑色粉末为氧化铜
上述设计方案的主要研究方法是________.配方l 配方2 配方3 配方4 木炭质量(g) 0.4 0.5 0.6 0.7 氧化铜质量(g) 8 8 8 8 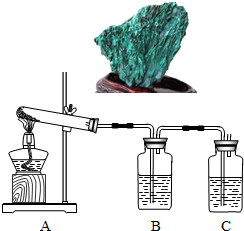
九年级化学填空题中等难度题查看答案及解析
-
碱式碳酸铜[Cu2(OH)2CO3]用作农药防治小麦黑穗病。实验室用加热法测定某农药中碱式碳酸铜的质量分数(假设杂质受热不参与反应)。充分加热100g样品,得到固体84.5g。已知反应的化学方程式为:Cu2(OH)2CO3
2CuO+H2O+CO2↑,Cu2(OH)2CO3的相对分子质量为222。试计算:
(1)Cu2(OH)2CO3中质量分数最大的元素是_______。
(2)若用100g 98%的浓硫酸充分吸收反应所产生的水,得到硫酸溶液的溶质质量分数是多少_______? (计算结果精确到0.1%)
(3)样品中碱式碳酸铜的质量分数是多少______________?
九年级化学计算题中等难度题查看答案及解析
-
(2007•海淀区二模)孔雀石[碱式碳酸铜,主要成分是Cu2(OH)2CO3]具有色彩浓淡的条状花纹(如图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.
冶炼铜的反应原理为:Cu(OH)2CO32CuO+CO2↑+H2O
2CuO+C2Cu+CO2↑
某校课外小组同学在实验室验证上述反应.
(1)加热分解碱式碳酸铜,生成氧化铜.装置如下图所示.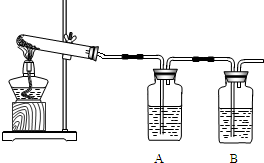
①瓶A中盛有的试剂是______,用来吸收水,证明碱式碳酸铜加热分解的产物中有水.
②瓶B中盛有的试剂是澄清石灰水,用来______,反应的化学方程式为______.
③反应结束,熄灭酒精灯前,应______.
(2)木炭和氧化铜反应,生成铜.
将木炭粉末和氧化铜粉末混合均匀,放进试管,加热充分反应.将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余.该小组同学设计方案验证黑色粉末的成分.
查阅资料:部分内容如下:木炭和氧化铜都是黑色粉末.氧化铜与稀硫酸反应生成硫酸铜,木炭与稀硫酸不反应.
猜想与验证:操作和药品 现象 分析和结论 方案Ⅰ 取少量剩余黑色粉末,充分灼烧 ①______________
________________原剩余黑色粉末是
氧化铜方案Ⅱ ②_______________
__________________③_____________
_________________原剩余黑色粉末是
氧化铜
(3)某同学探究在实际反应中,木炭和氧化铜反应生成铜时反应物的最佳质量比.设计方案如下:
上述设计方案的主要研究方法是______.配方1 配方2 配方3 配方4 木炭质量(g) 0.4 0.5 0.6 0.7 氧化铜质量(g) 8 8 8 8 
九年级化学解答题中等难度题查看答案及解析