-
某小组同学在用过氧化氢溶液与Mn02制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。为此,他们进行了如下探究:
(猜想与假设)
①速度慢、气泡少可能与过氧化氢溶液的浓度有关。
②速度慢、气泡少可能与Mn02的质量有关。
(进行实验)
根据图甲进行如下实验。

实验1:用26mg MnO2与5mL不同浓度过氧化氢溶液进行实验,压强变化如己图1。
实验2:用5mL 15%过氧化氢溶液与不同质量MnO2进行实验,压强变化如乙图2。
(解释与结论)
(l)过氧化氢溶液制取氧气的化学方程式为_________________。
(2)实验1得到的结论是___________。实验2的目的是___________ 欲得出“Mn02对过氧化氢分解有催化作用”的结论,需要对比_____________。(简要的写出实验设想)
(3)小组同学通过互联网得知:多种物质能催化过氧化氧的分解。
(实验探究)
实验证明,CuSO4溶液也能显著加快过氧化氢的分解,CuSO4溶液主要含有三种粒子(H2O、Cu2+、S042+),稀硫酸中含有三种粒子( H2O、H+、S042+)为了进一步探究CuSO4溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。
①小组同学认为最不可能的是H20,他们的理由是___________________。
②要说明另外的两种粒子是否起到催化作用,小组同学设计了如下实验,完成探究活动。
 _____
_____
(反思与评价)
(4)小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是_____________、______________。
(5)利用图甲装置探究“温度对过氧化氢分解速率”的影响,是否合理?_______理由是___________
-
某小组同学在用过氧化氢溶液与MnO2制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。为此,他们进行了如下探究:
(猜想与假设)
①速度慢、气泡少可能与过氧化氢溶液的浓度有关。
②速度慢、气泡少可能与MnO2的质量有关。
(进行实验)
根据图甲进行如下实验。
实验1:用26mg MnO2与5mL不同浓度过氧化氢溶液进行实验,压强变化如乙图1。
实验2:用5mL 1.5%过氧化氢溶液与不同质量MnO2进行实验,压强变化如乙图2。

(解释与结论)
(1)过氧化氢溶液制取氧气的化学方程式为_______________。
(2)实验1得到的结论是___________________________。实验2的目的是_________。
欲得出“MnO2对过氧化氢分解有催化作用”的结论,需要对比____________。(简要的写出实验设想)
(3)小组同学通过互联网得知:多种物质能催化过氧化氢的分解。
(实验探究)
实验证明,CuSO4溶液也能显著加快过氧化氢的分解,CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42﹣ ),稀硫酸中含有三种粒子(H2O、H+、SO42﹣ )为了进一步探究CuSO4,溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。
①小组同学认为最不可能的是H2O,他们的理由是____________。
②要说明另外的两种粒子是否起到催化作用,小组同学设计了如下实验,完成探究活动。
| 实验步骤 | 实验现象 | 结论 |
| a 取一支试管加入5mL 5%过氧化氢溶液,然后加入2﹣3滴稀硫酸 | 溶液几乎没有 气泡放出 | 验证明,起催化作用的是______。 |
| b.另取一支试管加入5mL 5%过氧化氢溶液,然后加入2﹣3滴硫酸铜溶液 | 溶液中有大量气泡放出 |
(反思与评价)
(4)小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是__________、_________。
(5)利用图甲装置探究“温度对过氧化氢分解速率”的影响,是否合理?_____。理由是________。
-
某小组同学在用过氧化氢溶液与MnO2制取氧气的过程中,发现反应的速度很慢,产生的气泡很少。为此,他们进行了如下探究。
(猜想与假设)
①速度慢、气泡少可能与过氧化氢溶液的浓度有关。
②速度慢、气泡少可能与MnO2的质量有关。
(进行实验)根据下图进行如下实验。
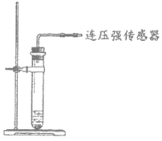
实验1:用26 mg MnO2与5 mL不同浓度过氧化氢溶液进行实验,压强变化如图1。
实验2:用5 mL 1.5%过氧化氢溶液与不同质量MnO2进行实验,压强变化如图2。
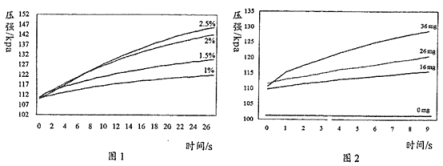
(解释与结论)
(1)实验1得到的结论是______________________________。
(2)实验2的目的是________________________________。
(3)小组同学在制氧气过程中,发现反应的速度很慢,依据上述实验所得结论,推测其原因可能是_____________。
(反思与评价)
(4)利用上图装置探究“温度对过氧化氢分解速率”的影响,是否合理?理由是_____________________。
-
某小组同学在用过氧化氢溶液与 制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。对此,它们进行了如下探究:
制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。对此,它们进行了如下探究:
(猜想与假设)
①速率慢、气泡少可能与过氧化氢溶液的浓度有关。
②速率慢、气泡少可能与 的质量有关。
的质量有关。
(进行实验)
根据图甲进行如下实验。
实验1:用26mg 与5mL不同浓度过氧化氢溶液进行实验,压强变化如乙图1。
与5mL不同浓度过氧化氢溶液进行实验,压强变化如乙图1。
实验2:用5mL 1.5%过氧化氢溶液与不同质量 进行实验,压强变化如乙图2。
进行实验,压强变化如乙图2。

(解释与结论)
(1)实验1得到的结论是______,实验2的目的是______。欲得出“ 能加快过氧化氢的分解”这一结论,需要对比______。(简要的写出实验设想)
能加快过氧化氢的分解”这一结论,需要对比______。(简要的写出实验设想)
(2)小组同学查阅资料得知:多种物质能催化过氧化氢的分解。
(实验探究)
实验证明, 溶液也能显著加快过氧化氢的分解,
溶液也能显著加快过氧化氢的分解, 溶液主要含有三种粒子(
溶液主要含有三种粒子( ),稀硫酸中含有三种粒子(
),稀硫酸中含有三种粒子( )为了进一步探究
)为了进一步探究 溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计:
溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计:
①小组同学认为最不可能的是 ,他们的理由是______。
,他们的理由是______。
②要说明另外的两种粒子是否起到催化作用,小组同学设计了如下实验,完成探究活动。
| 实验步骤 | 实验现象 | 结论 |
| a.取一支试管加入5mL 5%过氧化氢溶液,然后加入2-3滴稀硫酸 | 溶液中几乎没有气泡放出 | 验证明,起催化作用的是______。 |
| b.另取一支试管加入5mL 5%过氧化氢溶液,然后加入2-3滴硫酸铜溶液 | 溶液中有大量气泡放出 |
(3)(反思与评价)
小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是______、______。
(4)利用图甲装置不能探究“温度对过氧化氢分解速率”的影响,其理由是______。
-
某课外活动小组就催化剂对化学反应速率的影响进行了有关探究,已知二氧化锰可作为过氧化氢分解产生氧气的催化剂。同学在用过氧化氢溶液与二氧化锰制取氧气的过程中,发现反应的速率慢,产生的气泡少。为此,他们进行了如下探究:
(猜想与假设)
①分解速度慢可能与过氧化氢溶液的浓度有关。
②分解速度慢可能与二氧化锰的质量有关。
(进行实验)根据图甲进行如下实验。
实验1:用26mg 二氧化锰与5mL不同浓度的过氧化氢溶液进行实验,压强变化如乙图1。
实验2:用5mL 1.5%过氧化氢溶液与不同质量的二氧化锰进行实验,压强变化如乙图2。
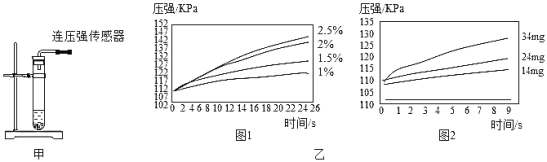
(解释与结论)
(1)过氧化氢溶液制取氧气的文字表达式为__________________。
(2)实验1得到的结论是过氧化氢溶液的浓度越_____________,分解速度越快。实验2得到的结论是二氧化锰的质量越_______________,分解速度越慢。
(3)小组同学通过查阅资料得知:同一个反应的催化剂可能有多种。
(查阅资料)除二氧化锰外,氧化铜、氧化铁也可以作为氯酸钾分解的催化剂。
(进行实验)取等质量的氯酸钾按下表进行实验:测定氯酸钾分解产生氧气的温度。
| 实验编号 | 实验药品 | 分解温度 |
| 氯酸钾 | 580 |
| 氯酸钾、二氧化锰(质量比1:1) | 350 |
| 氯酸钾、氧化铜(质量比1:1) | 370 |
| 氯酸钾、氧化铁(质量比1:1) | 390 |
(分析数据、得出结论)
(1)由实验______与实验 对比,证明氧化铁可作为氯酸钾分解的催化剂。
对比,证明氧化铁可作为氯酸钾分解的催化剂。
(2)实验所用的三种物质中,催化效果最好的是______________。
(反思)证明氧化铜是该反应的催化剂,还要验证它在化学反应前后的质量和____没有改变。
-
某研究小组对过氧化氢溶液制取氧气进行如下探究。
实验一、探究H2O2质量分数、溶液pH、温度对反应速率的影响。设计如下表实验方案:
| 实验序号 | H2O2质量分数% | PH | 温度/℃ | 每分钟气泡数 |
| 1 | 30 | 5 | 20 | |
| 2 | 30 | 6 | 20 | |
| 3 | 30 | 11 | 20 | |
| 4 | 30 | 11 | a | |
| 5 | b | 11 | 20 | |
试分析表中a、b的数值分别是a=__________________,b=______________________。
实验二、探究制取氧气的适宜催化剂。设计如下方案:
I.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
II.取30粒含MnO2的海藻酸钠微球,采用图1装置进行实验。改用其他三种微球,分别重复上述实验,得到如图2的锥形瓶内压强随时间变化的曲线图。
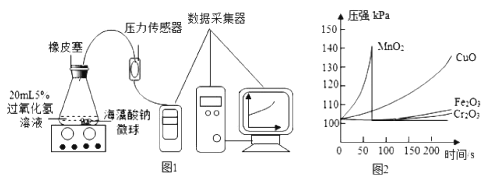
①每次实验时,海藻酸钠微球数应相同的原因是___________________________。
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因可能是______________________。
③从实验曲线看,催化效果较好、反应温和的催化剂是_____________________。
-
实验室常用过氧化氢溶液作反应物、二氧化锰作催化剂来制取氧气。为比较不同质量的二氧化锰对反应速率的影响,某研究小组同学进行了如下探究:
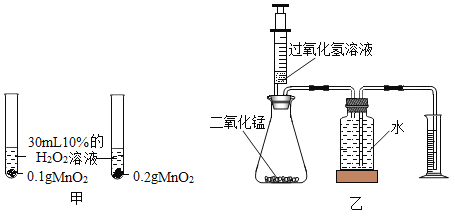
(1)请写出二氧化锰催化过氧化氢分解的化学方程式: ________________________。
(2)实验装置如图甲所示,可通过观察________________________来比较两者的反应速率。
(3)实验装置如图乙所示,量筒中进入水的体积与反应生成氧气的体积____________________(选填“相等”或“不等”),要比较不同质量的二氧化锰对反应速率的影响,可测量相同时间内_____________________。
(4)小组同学设置了10组实验,每组中加入等体积、等浓度的过氧化氢溶液,测定加入不.同质量二氧化锰后,各组收集等体积氧气所用的时间,数据记录如下(其他实验条件均相同):
| 实验序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 二氧化锰用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 待测数据 | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
请分析表中数据,回答问题:
① 实验中用等体积、等浓度的过氧化氢溶液的目的是________________________。
② 条件相同时,随着MnO2用量的增加,反应速率_______________________。
(5)同学们还想探究二氧化锰的颗粒大小对化学反应速率是否有影响,请你帮他们设计实验方案进行探究:__________________________。
-
实验小组对过氧化氢制取氧气中影响反应速率的因素进行探究。
[提出问题] 哪些因素可能影响该反应的反应速率?
[作出猜想] 小芳同学:H2O2溶液的浓度可能影响该反应的反应速率;
小华同学:催化剂(MnO2)的用量可能影响该反应的反应速率……
[实验验证]
(1)为了探究在其他条件相同时H2O2溶液浓度对反应速率的影响,小芳同学的实验是:每次均取10mL30%的H2O2溶液,然后配成不同浓度的溶液,在相同温度下加入等质量MnO2进行实验,测定各次收集到100mL氧气时所用的时间,记录数据如下:
| 实验次序 | 1 | 2 | 3 | 4 | 5 |
| H2O2溶液浓度 | 1% | 5% | 15% | 25% | 30% |
| 所用时间(秒) | 660 | 205 | 25 | 4 | 3 |
通过上表实验数据分析可得到的结论是:在其他条件相同的情况下,_____越大,反应速率越_____。
(2)为了探究在其他条件相同时催化剂(MnO2)的用量对反应速率的影响,小华同学的实验是:每次均用30mL10%的H202溶液在相同温度下进行实验,采用不同量MnO2粉末做催化剂,测定各次收集到100mL氧气时所用的时间,绘图如下:
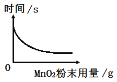
①该反应的化学方程式为:__________
②通过如图实验数据分析可得到的结论是: ________
(3)小明同学认为其他条件也可能会影响该反应的速率。
小明同学的实验是:每次均取10mL30%的H2O2溶液,然后配成一定浓度的溶液进行实验。
| 实验次序 | 1 | 2 | 3 | 4 | 5 |
| H2O2溶液浓度 | ① | 10% | 10% | 10% | 10% |
| 二氧化锰粉末用量/g | 0.2 | 0.2 | ② | 0.2 | 0.2 |
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 待测数据 | | | | | |
填写表中数据:① ___________ ② ___________。
③小明同学实验探究的目的是 _________。
④以下待测数据合理的是_____________
A.测定各次实验收集到100mL氧气时所用的时间
B.测定各次实验在30s里收集到的氧气体积
C.测定各次实验完全反应时收集到的氧气体积
-
某研究小组对过氧化氢溶液制取氧气进行如下探究:
实验一 探究H2O2质暈分数、溶液pH、温度对反应速率的影响
(1)实验室用过氧化氢溶液制氧气的化学方程式为______。
(2)设计如下表实验方案
| 实验序号 | H2O2质量分数/% | pH | 温度/℃ | 每分钟气泡数 |
| 1 | 30 | 5 | 20 | |
| 2 | 30 | 6 | 20 | |
| 3 | 30 | 11 | 20 | |
| 4 | 15 | 11 | 30 | |
| 5 | a | 11 | b | |
①实验1~3的实验目的是______。
②a=______;b=______。
实验二 探究制取氧气的适宜催化剂
(3)实验方案如下:
Ⅰ.MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海濚酸钠徽球,采用如图装置进行实验。改用其他三种微球,分别重复上述实验,得到如图的维形瓶内压强随时间变化的曲线图。
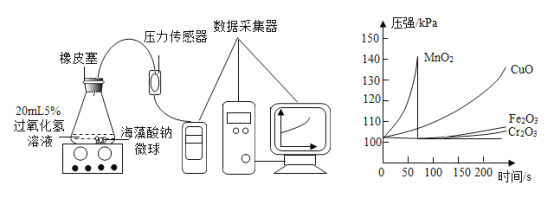
①每次实验时,海藻酸钠微球数应相同的原因______。
②含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因可能是______。
③从实验曲线看,催化效果较好、反应温和的催化剂是______。
-
实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程式: ;
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除Mn02、CuO外,Fe203也可以作KCl03分解的催化剂.
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好).
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | KCl03 | 580 |
| ② | KCl03、Mn02(质量比1:1) | 350 |
| ③ | KCl03、CuO(质量比l:1) | 370 |
| ④ | KCl03、Fe203(质量比1:1) | 390 |
【分析数据、得出结论】
(1)由实验 与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是 .
【反思】
(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后质量和 不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证 ;
(3)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可).

 _____
_____







