一定质量的硫铁矿(主要成分是FeS2),高温烧发生如下反应(杂质不参加反应):4FeS2+11O28SO2+2Fe2O3,生成的SO2经过一系列反应全部变成H2SO4,把生成的H2SO4稀释后加入足量BaCl2溶液完全反应生成4.66t的沉淀,则硫铁矿中FeS2的质量为
A. 1.2t B. 2.28t C. 1.28t D. 2.4t
九年级化学单选题中等难度题
一定质量的硫铁矿(主要成分是FeS2),高温烧发生如下反应(杂质不参加反应):4FeS2+11O28SO2+2Fe2O3,生成的SO2经过一系列反应全部变成H2SO4,把生成的H2SO4稀释后加入足量BaCl2溶液完全反应生成4.66t的沉淀,则硫铁矿中FeS2的质量为
A. 1.2t B. 2.28t C. 1.28t D. 2.4t
九年级化学单选题中等难度题
一定质量的硫铁矿(主要成分是FeS2),高温烧发生如下反应(杂质不参加反应):4FeS2+11O28SO2+2Fe2O3,生成的SO2经过一系列反应全部变成H2SO4,把生成的H2SO4稀释后加入足量BaCl2溶液完全反应生成4.66t的沉淀,则硫铁矿中FeS2的质量为
A. 1.2t B. 2.28t C. 1.28t D. 2.4t
九年级化学单选题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
在工业制取硫酸的过程中,有发生如下反应:4FeS2+11O22Fe2O3+8SO2.现有含FeS260%的黄铁矿100t(假设杂质不参加反应),最多可生产SO2多少吨?(相对分子质量:FeS2﹣120 SO2﹣64)
九年级化学计算题中等难度题查看答案及解析
工业上可用黄铁矿(主要成分FeS2)制取硫,主要流程如下:
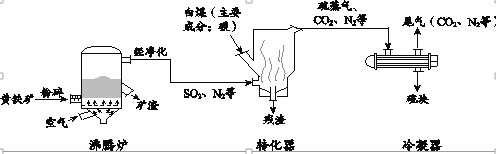
已知:沸腾炉中的主要反应为4FeS2 + 11O2 2Fe2O3 + 8SO2
(1)黄铁矿粉碎的目的是______。
(2)在加热条件下,转化器中发生反应的化学方程式是______。
(3)冷凝器中发生的变化是______(填“物理变化”或“化学变化”)。
(4)以上流程中产生的矿渣和尾气均可再利用,其可能的用途是_____(答1条即可)。
九年级化学流程题中等难度题查看答案及解析
(2013福建南平)在工业制取硫酸的过程中,有发生如下反应:4FeS2+11O22Fe2O3+8SO2.现有含FeS2 60%的黄铁矿100t(假设杂质不参加反应),最多可生产SO2多少吨?(相对分子质量:FeS2-120SO2-64)
九年级化学选择题中等难度题查看答案及解析
黄铁矿(主要成分为FeS2,杂质高温下不反应。)是我国硫酸厂制取硫酸的主要原料。
某兴趣小组欲测定某黄铁矿中FeS2含量,设计了如下实验 (假设每步反应均完全)。
【查阅资料】 ①4FeS2+11O2 2Fe2O3+8SO2 ②Na2SO3+H2O2 =Na2SO4+H2 ③BaSO4为一种不溶于水、不溶于盐酸的沉淀。
【实验探究】
Ⅰ.称取4.80 g黄铁矿样品放入下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。

Ⅱ.反应结束后,将B瓶中的溶液按上图流程进行处理。
【问题讨论】
(1)Ⅰ中B瓶内发生反应的化学反应方程式是______和______;
(2)Ⅰ中通入的空气中作用是______和______;
(3)Ⅱ中加入盐酸溶液的目的是______;
(4)Ⅱ中检验滤渣洗涤是否干净的方法是______。
【含量测定】
(5)另取4.80g黄铁矿样品在空气中加热,测出样品的固体残留率( ×100%)随温度的变化如下图所示,计算该黄铁矿中FeS2的质量分数为______。(请写出计算过程)
×100%)随温度的变化如下图所示,计算该黄铁矿中FeS2的质量分数为______。(请写出计算过程)

九年级化学综合题困难题查看答案及解析
某兴趣小组的同学为测定某黄铁矿(主要成分是FeS2)中硫元素的含量进行了如下的实验探究。
【查阅资料】(1)4FeS2+11O2 8SO2+2Fe2O3
(2)亚硫酸钠与过氧化氢反应生成硫酸钠和水。
【设计方案】甲、乙二个实验小组均设计了下列装置,称取了m1 g黄铁矿样品,将样品放入如下图所示的硬质粗玻璃管中,从a处不断地缓缓通入空气,高温灼烧玻璃管中的黄铁矿样品至反应完全。(假设每步反应均完全,不考虑装置内原有空气对测定结果的影响)

甲组同学仅称量了上述实验所需要的相关装置质量后即完成了测定。
乙组同学则在上述反应结束后,将C瓶中的溶液进行了如下图处理:

【实验分析及数据处理】
(1)上述装置中A瓶内所盛的试剂最好是 溶液,其作用是 。
(2)A、B装置不能对调位置,原因是 。
(3)C瓶中发生反应的化学方程式为 。
(4)甲组同学应称量的数据是 (填编号)。
①反应前C装置及其中物质总质量m2 g
②反应前C、D装置及其中物质总质量m3 g
③反应后C装置及其中物质总质量m4 g
④反应后C、D装置及其中物质总质量m5 g
(5)根据(4)中所选数据,甲组同学测得的该黄铁矿中硫元素的质量分数的表达式为
。
(6)乙组实验中,检验所加BaCl2溶液是否过量的方法是 ,若实验过程中未洗涤滤渣就直接烘干称量,则会使测定结果 (填“偏大、偏小或不变”),检验滤渣是否洗净所用试剂是 溶液。
九年级化学探究题困难题查看答案及解析
黄铁矿(主要成分为FeS2,杂质不含硫元素)是我国大多数硫酸厂制取硫酸的主要原料。化学课外活动小组为测定某黄铁矿中FeS2含量进行了如下的实验探究(假设每步反应均完全)。
【查阅资料】
①4FeS2+11O2 2Fe2O3+8SO2
②Na2SO3+H2O2=Na2SO4+H2O
③Na2SO4+BaCl2=BaSO4 ↓+2NaCl
④Na2CO3+BaCl2=BaCO3 ↓+2NaCl
【实验探究】
Ⅰ. 称取1.60 g黄铁矿样品放入下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。
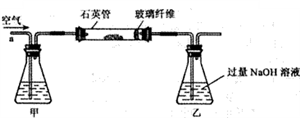
Ⅱ. 反应结束后,将乙瓶中的溶液进行如下处理:
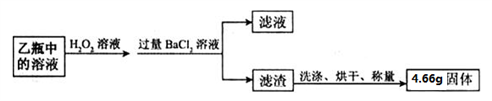
【问题讨论】
(1)Ⅰ中装置中甲瓶内盛放的试剂是氢氧化钠溶液,其作用是____________。
【含量测定】
(2)Ⅱ中最终得到的4.66g固体是_________(填物质的化学式)。
(3)计算该黄铁矿中FeS2的质量分数。_________(请写出计算过程)
【交流反思】
(4)如果缺少甲装置,则最终测得FeS2的质量分数将会_________(填“偏大”“偏小”或“不变”)。
(5)Ⅱ中证明所加BaCl2溶液过量的方法是_________________。
【拓展应用】
工业上以黄铁矿为原料生产硫酸的工艺流程图如下所示:
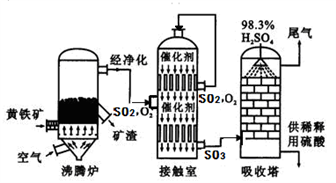
(6)接触室中发生反应的化学方程式为_________________。化学实验室现有质量分数为98%的浓硫酸,但在实验中常需要用到较稀的硫酸。要把100g上述浓硫酸稀释成质量分数为10%的硫酸,需要水的质量是________g,稀释时,应将_________沿烧杯内壁慢慢注入_______中,并不断用玻璃棒搅拌。硫酸是一种重要的化工产品,用途十分广泛,请写出稀硫酸的一种用途_______________。
(7)依据生产硫酸的工艺流程图,下列说法正确的是________(填字母)。
A.为使黄铁矿充分燃烧,需将其粉碎
B.催化剂能够提高SO2的反应速率和产量
C.SO2可做为生产硫酸的原料循环再利用
D.沸腾炉排出的矿渣可供炼铁
九年级化学信息分析题极难题查看答案及解析
益阳市桃江县硫铁矿厂开采的黄铁矿(主要成分是FeS2),是生产H2SO4的重要原料.利用黄铁矿生产H2SO4的第一步反应为:4FeS2+11O2═2Fe2O3+8X.所得产物Fe2O3是冶炼铁的重要原料.回答下列问题:
(1)已知FeS2中Fe的化合价为+2,则S的化合价为________.
(2)X的化学式是_________.
(3)写出高炉中Fe2O3转化成铁的化学方程式__________________________.
九年级化学填空题中等难度题查看答案及解析
益阳市桃江县硫铁矿厂开采的黄铁矿(主要成分是FeS2),是生产H2SO4的重要原料.利用黄铁矿生产H2SO4的第一步反应为:4FeS2+11O2═2Fe2O3+8X.所得产物Fe2O3是冶炼铁的重要原料.回答下列问题:
(1)已知FeS2中Fe的化合价为+2,则S的化合价为________.
(2)X的化学式是_________.
(3)写出高炉中Fe2O3转化成铁的化学方程式__________________________.
九年级化学填空题简单题查看答案及解析