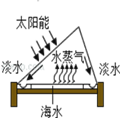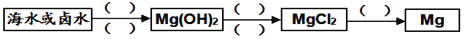-
海洋是人类千万年来赖以生存的重要资源宝库,图1是海水中化学资源的图示。请结合图示回答相关问题。

(1)取海水滴加AgNO3溶液的现象是 。
(2)下列有关海水及其开发的说法正确的是 。
a.图2中海水所含化学资源都是化合物
b.蒸馏法淡化海水是化学变化
c.海水资源的开发不需要考虑环境保护问题
d.海水中含有NaCl和MgCl2
(3)海水中含有10个电子的微粒有H2O、Mg2+和 。
(4)工业利用海水制取纯碱和轻质MgO的流程图如图3,据图回答下列问题。
①MgO的名称是 。
②海水晒盐的一系列操作X是蒸发、 ;过滤;实验室进行操作Y时需使用玻璃棒,其作用是 。
③氨碱法制取纯碱是先制成饱和氨盐水,再不断通入二氧化碳,反应生成碳酸氢钠和氯化铵,产生析出碳酸氢钠的原因是 ,碳酸氢钠分解生成纯碱的化学方程式是 。
④苦卤(含MgCl2与NaCl)加入纯碱的反应类型是 。
⑤2.4×105t海水中含镁元素的质量是 t,生产中实际得到523.6t气体Z,请计算流程中MgO的产率,写出必要的计算过程。
(已知:产率= ×100%,“理论上的产物质量”是不考虑损失,且反应物完全反应时的产物质量)
×100%,“理论上的产物质量”是不考虑损失,且反应物完全反应时的产物质量)
-
海洋是人类千万年来赖以生存的重要资源宝库,图1是海水中化学资源的图示,请结合图示回答相关问题。

(1)向海水中滴加AgNO3溶液的现象是____________________。
(2)下列有关海水及其开发的说法正确的是________。
a.图2中海水所含化学资源都是化合物
b.蒸馏法淡化海水是化学变化
c.海水资源的开发不需要考虑环境保护问题
d.海水中含有NaCl和MgCl2
(3)海水中含有10个电子的微粒有H2O、Mg2+和________。
-
庆祝人民海军成立70周年多国海军活动在青岛举行,习总书记首提构建“海洋命运共同体”。海洋是一个巨大的资源宝库,人类要像对待生命一样关爱海洋。请同学们结合所学化学知识回答下列问题:
(1)海水晒盐得到粗盐,剩余的母液称为苦卤,可以用于工业制取镁,主要流程如图所示:
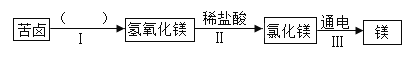
步骤I中选用的试剂名称为____,写出实验II中发生反应的化学方程式__________________。
(2)粗盐晶体中常含有泥沙、氯化钙、氯化镁和硫酸钠杂质,可按照下列实验步骤进行提纯氯化钠:①将固体加入足量水中,加入过量氢氧化钠溶液;②加入过量碳酸钠溶液;③加入过量氯化钡溶液;④过虑;⑤将滤液蒸发即可获得氯化钠晶体。请你评价该实验方案的两处不足之处,并提出改进意见:一是_____________________;二是________________________。
-
(2008•沂源县一模)海洋是人类的母亲,是人类千万年来取之不尽、用之不竭的巨大资源宝库.我国有较长的海岸线,海洋资源十分丰富.以下是我国对海水资源的部分利用.
(1)海水中含量最高的盐是(写化学式),海水经结晶可获得粗盐.
(2)粗盐中含有泥沙、硫酸镁、氯化钙等杂质.将粗盐溶于水,然后再进行如下操作即可得到较纯的氯化钠:①过滤;②加过量的NaOH溶液;③加适量的盐酸;④加过量的Na2CO3溶液;⑤加过量的BaCl2溶液.正确的操作顺序是.
(3)从晒盐后的卤水中提取重要金属镁.提取镁的步骤如下:
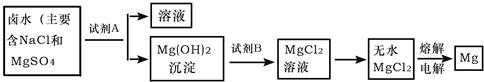
提取镁的过程中,试剂A最好选用(写化学式),试剂B选用(写名称).电解无水氯化镁的过程中能转化为能,写出电解氯化镁的化学反应方程式:.
(4)向饱和的氯化钠溶液中依次通入氨气、二氧化碳,析出碳酸氢钠晶体,加热碳酸氢钠晶体可制得纯碱.写出上述反应的化学方程式:
①;
②.
(5)制得的纯碱在生产、生活中具有广泛用途:
①生活中纯碱常用做洗涤剂,洗涤餐具,原因是纯碱的溶液显性.
②工业上用纯碱和石灰石为原料制烧碱,写出制取过程中所发生反应的化学方程式:.
③工业上通常用纯碱、石英砂、石灰石混合高温煅烧制玻璃,写出制取过程中所发生反应的化学方程式:
.
-
海洋是人类的巨大资源宝库,试回答下列相关问题:

(1)海水淡化:右图为太阳能海水淡化装置。
①该海水淡化过程,相当于实验室中的_____(填“蒸发”或“蒸馏”)。
②下列分离混合物的常用方法中,原理与上述方法相同的是_____(填序号)。
A 过滤法净化水
B 工业法制氧气
C 活性炭吸附
③膜分离技术可用于淡化海水(如图所示),通过膜的主要微粒是_____。

(2)海水制镁:下图是由海水制备金属镁的工业流程:

涉及的主要步骤有:①电解熔融的氯化镁②加石灰乳③加盐酸④过滤,其先后顺序正确的是_____。
A ②④③① B ②④①③ C ②③④① D ③②④①
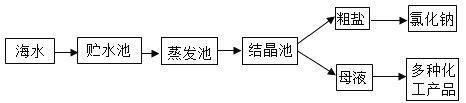
(3)海水中含有氯化钠、氯化钙等物质,下面是从海水中提取氯化钠的大致过程和氯化钠、氯化钙的溶解度表。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 |
①将粗盐从海水中结晶出来的方法中是_____,将粗盐和母液分离的操作是_____。
②经长时间日晒,氯化钙也不易大量结晶析出的原因是_____。40℃时,50g水中最多溶解氯化钙_____g。
③根据海水晒盐的原理,下列说法中正确的是_____。(填序号)
A 海水进入贮水池,海水的成分基本不变
B 在蒸发池里,海水中水的质量逐渐增加
C 析出晶体后的母液是氯化钠的不饱和溶液
-
海洋是人类的巨大资源宝库,试回答下列相关问题:
⑴海水淡化: 下图为太阳能海水淡化装置。
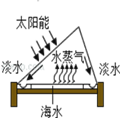
①该海水淡化过程,相当于实验室中的______(填“蒸发”或“蒸馏”)。
②下列分离混合物的常用方法中,原理与上述方法相同的是______(填序号)。
A.过滤法净化水 B.工业法制氧气 C.活性炭吸附
⑵海水制镁: 下图是由海水制备金属镁的工业流程:
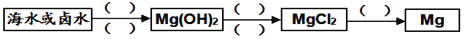
涉及的主要步骤有:①电解熔融的氯化镁 ②加石灰乳 ③加盐酸 ④过滤 ⑤蒸发结晶,其先后顺序正确的是(_______)。
A.②④③⑤① B.②④①⑤③ C.②③④⑤① D.③②④①⑤
⑶海水晒盐: 所得粗盐中常含有泥沙等难溶性杂质,可通过溶解、过滤、__________等操作去除。这样得到的食盐晶体中仍含有可溶性杂质CaCl2,工业上选用试剂______________对其进行除杂。
⑷海水制“碱”: 1926年,我国著名化学家___________创立了侯氏制碱法,以食盐为主要原料制取纯碱。生产过程中,先向饱和食盐水中通氨气,再通二氧化碳,涉及的反应原理如下:
NaCl + NH3 + CO2 + H2O ═ NaHCO3 + NH4Cl , 2NaHCO3 △ Na2CO3 + H2O + CO2↑
试回答下列问题:
①向饱和食盐水中先通氨气,再通二氧化碳的原因是________________。
②纯碱在生活生产中用途广泛。试写出工业上利用纯碱与熟石灰反应制取烧碱的化学方程式:______。
-
海洋是人类赖以生存的重要资源宝库,从海水中提取镁的化工流程图如下:

(1)操作①的名称是_______________,在实验室里进行该操作,玻璃棒的作用是_______________。
(2)试剂a的名称是_________________,写出Mg(OH)2加入试剂a时所发生的化学方程式是________________。
(3)将生石灰制成石灰乳的过程是_____________反应(填“吸热”或“放热”)。
-
海洋是人类千万年来取之不尽、用之不竭的巨大资源宝库,开发前景广阔.
(1)海水淡化:世界上已采用海水淡化的方法有20多种,目前普遍采用________法.
(2)海水“晒盐”.海水提取食盐的方法主要为“盐田法”,其过程如下:
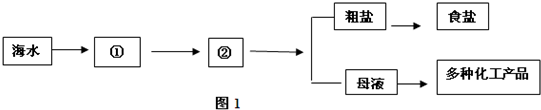
如图1中②是________池,上图中的“母液”是氯化钠的(填“饱和”或“不饱和”)________溶液.
(3)海水“制碱”.如图2是氨碱法制纯碱的部分简单流程.
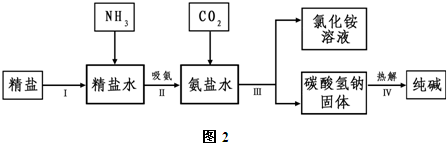
①步骤Ⅲ反应的化学方程式是________.
②制氨盐水的过程中要先通入氨气,再通入二氧化碳.如果反过来,二氧化碳的吸收率会降低.这是因为________.
③氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,首先析出物质的是________,原因是________.
(4)海水提取镁:在海水提取镁的过程中发生一系列化学反应,这些反应中没有涉及到的反应基本类型是________.
-
海洋是人类千万年来取之不尽、用之不竭的巨大资源宝库,开发前景广阔。
(1)目前海水淡化的方法很多,在世界范围之内能做到规模化和产业化的主要是膜法和______。高压反渗透膜法淡化海水是利用海水中各成份的_________不同分离出淡水。
(2)2017年5月18日,在中国南海海域实现可燃冰(CH4·nH2O)试采成功,这将使人类能源格局翻开新篇章。

①可燃冰中,水分子形成一种空间笼状结构,甲烷和少量N2、CO2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于_____(选填“纯净物”或“混合物”)。
②若某种可燃冰中CH4与H2O的质量比是1:9,则该可燃冰中n=_______。
(3)海水“晒盐”
①海水提取食盐的方法主要为“盐田法”,其过程如下;图中②是_____池,下图中的“母液”是氯化钠的_________溶液。(填“饱和”或“不饱和”)
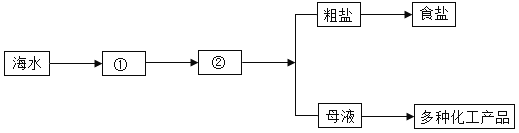
②粗盐纯化。粗盐中含有泥沙、硫酸镁、氯化钙等杂质。将粗盐溶于水,然后通过如下操作即可得到较纯的氯化钠:a过滤;b加过量的Ba(OH)2溶液;c加适量的盐酸;d加过量的Na2CO3溶液;e蒸发。正确的操作顺序是_________(填字母)。
(4)制镁。工业上一般用电解熔融状态的氯化镁制金属镁,若以卤水(含有硫酸镁、氯化钠和氯化钙)为起始原料来制取金属镁。
①从海水中提取镁过程中涉及到的分解反应的化学反应方程式为__________。
②海水本身就是含有MgCl2的溶液,它与通过转化后得到的MgCl2溶液有何不同:_________。
-
海洋是人类千万年来取之不尽、用之不竭的巨大资源宝库,开发前景广阔.
(1)目前海水淡化的方法有20多种,目前普遍采用______法
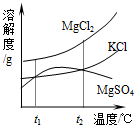
(2)“海水晒盐”后得到的卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线示意图.
①设t1℃时MgCl2、KCl和MgSO4三种物质的溶解度分别为a、b、c,则它们的大小关系为______.
②将卤水加热到t2℃以上,根据溶解度曲线,首先析出的晶体是______(填名称).
(3)“海水制碱”过程中发生的分解反应是______ Na2CO3+H2O+CO2↑

 ×100%,“理论上的产物质量”是不考虑损失,且反应物完全反应时的产物质量)
×100%,“理论上的产物质量”是不考虑损失,且反应物完全反应时的产物质量)