-
写出下列反应的表达式,并填写相关的空格:
①碳酸氢铵受热易“失踪”:______ NH3↑+H2O+CO2↑八年级化学解答题中等难度题查看答案及解析
-
碱式碳酸铜受热分解成CuO、CO2和H2O等三种物质,则碱式碳酸铜的组成是( )
A. 只含有碳、氢、氧元素 B. 一定含有碳、氢、铜元素,可能含有氧元素
C. 一定含有碳、氢、氧元素,可能含有铜元素 D. 肯定含有碳、氢、氧、铜元素
八年级化学单选题简单题查看答案及解析
-
某同学用下图装置测定空气中氧气的体积分数。请你填写有关空格,并与同学交流。
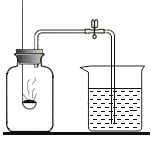
(1)写出红磷燃烧的文字表达式为_______
(2)待该物质熄灭并冷却后,打开弹簧夹观察到的现象是______,由此得出的结论是______
(3)实验后发现测定出的空气中氧气的体积分数低于1/5,这可能的原因是_____、_______(任写两种)
(4)由本实验还可以推测氮气的性质有(任写一种):_____
(5)若将红磷换成碳粉,该实验能否获得成功?_______(填能或否)理由是_____
八年级化学实验题中等难度题查看答案及解析
-
写出下列反应的符号表达式及基本反应类型:
(1)硫在空气中燃烧:_______________________ 属于__________反应;
(2)氧化汞受热分【解析】
_______________________ 属于___________反应。八年级化学填空题中等难度题查看答案及解析
-
写出下列反应的符号表达式并注明是分解反应还是化合反应
(1)木炭在空气中燃烧________(________ 反应)
(2)加热碳酸氢铵________(________ 反应)八年级化学填空题中等难度题查看答案及解析
-
近几年来,世界范围内的地震频发,引起人们的高度关注.地震发生的成因很复杂,据研究,孕震过程中比较活泼的物质有CO2、氢等.
(1)孕震过程中,在地壳的岩层中碳酸盐受热发生如下反应:
CaCO3CaO+CO2↑ MgCa(CO3)2
MgO+CaO+2CO2↑这两个反应均属于基本反应类型中的________.
(2)氢在目前的地震预测中被公认为是一种灵敏元素.一般认为,在高温下地壳中水蒸气和氧化亚铁(FeO)作用会产生氢气和氧化铁(Fe2O3),该反应的化学方程式为________.
(3)震后防疫的众多消毒剂中,有一种高效消毒剂的主要成分是三氯异氰尿酸(又称高氯精),化学式为C3O3N3Cl3高氯精由________种元素组成,高氯精中C、N两种元素的质量比为________.八年级化学填空题中等难度题查看答案及解析
-
近几年来,世界范围内的地震频发,引起人们的高度关注.地震发生的成因很复杂,据研究,孕震过程中比较活泼的物质有CO2、氢等.
(1)孕震过程中,在地壳的岩层中碳酸盐受热发生如下反应:
CaCO3CaO+CO2↑ MgCa(CO3)2
MgO+CaO+2CO2↑这两个反应均属于基本反应类型中的________.
(2)氢在目前的地震预测中被公认为是一种灵敏元素.一般认为,在高温下地壳中水蒸气和氧化亚铁(FeO)作用会产生氢气和氧化铁(Fe2O3),该反应的化学方程式为________.
(3)震后防疫的众多消毒剂中,有一种高效消毒剂的主要成分是三氯异氰尿酸(又称高氯精),化学式为C3O3N3Cl3高氯精由________种元素组成,高氯精中C、N两种元素的质量比为________.八年级化学填空题中等难度题查看答案及解析
-
氧化汞受热的微观过程可以用如图表示:
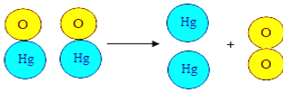
(1)写出该反应的文字表达式:___________;
(2)该反应的基本反应类型是_________;
(3)此反应过程中,没有发生变化的微粒是__________,变化的微粒是___________。
八年级化学简答题简单题查看答案及解析
-
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献.他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱.有关反应的化学方程式为:
NH3+CO2+H2O═NH4HCO3;
NH4HCO3+NaCl═NaHCO3↓+NH4Cl;
2NaHCO3Na2CO3+CO2↑+H2O
回答下列问题:
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是______(填字母标号).
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解 c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验.
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出).
试回答下列有关问题:
(Ⅰ)乙装置中的试剂是 饱和的碳酸氢钠溶液,作用是______;
(Ⅱ)丁装置中稀硫酸的作用是______;
(Ⅲ)实验结束后,分离出NaHCO3晶体的操作是______(填分离操作的名称).
②另一位同学用图中戊装置(其它装置未画出)进行实验.
(Ⅰ)实验时,须先从______管通入______气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是______;
(3)请你再写出一种实验室制取少量碳酸氢钠的方法:______.
(4)“纯碱中常常会混有少量氯化钠.”某研究性学习小组以一包纯碱(只考虑含氯化钠)为研究对象,探究纯碱样品中碳酸钠的含量.
【实验设计】
甲方案
Ⅰ.设计思路:根据样品与氯化钙溶液反应生成沉淀碳酸钙的质量,求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ.操作步骤:称取13.25g纯碱样品,加入过量的氯化钙溶液,充分搅拌.过滤、洗涤、干燥,得到的白色沉淀10.00g.
Ⅲ.数据处理:请根据上述实验数据,计算该样品中碳酸钠的质量分数.
计算过程:
______
乙方案
I.设计思路:根据样品(质量为a g)与稀硫酸完全反应生成二氧化碳的质量(质量为b g),求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
II.实验结论:
(1)当a、b的质量关系满足______(填写含a、b字母的表达式,下同)时,纯碱样品中只含有碳酸钠,样品中碳酸钠的质量分数是100%.
(2)当a、b的质量关系满足______时,纯碱样品室有碳酸钠和少量氯化钠组成的混合物,样品中碳酸钠的质量分数是______.
【实验评价】
误差分析:
(一)甲方案中,白色沉淀的质量在过滤、干燥等操作过程中会有所损耗,造成计算结果与实际值相比偏小.如果将氯化钙溶液换成氯化钡溶液,则可以使误差减小,理由是______.
(二)乙方案中,有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比______(填“偏大”、“偏小”、或“不变”).八年级化学解答题中等难度题查看答案及解析
-
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献.他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱.有关反应的化学方程式为:
NH3+CO2+H2O═NH4HCO3;
NH4HCO3+NaCl═NaHCO3↓+NH4Cl;
2NaHCO3Na2CO3+CO2↑+H2O
回答下列问题:
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是______(填字母标号).
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解 c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验.
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出).
试回答下列有关问题:
(Ⅰ)乙装置中的试剂是 饱和的碳酸氢钠溶液,作用是______;
(Ⅱ)丁装置中稀硫酸的作用是______;
(Ⅲ)实验结束后,分离出NaHCO3晶体的操作是______(填分离操作的名称).
②另一位同学用图中戊装置(其它装置未画出)进行实验.
(Ⅰ)实验时,须先从______管通入______气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是______;
(3)请你再写出一种实验室制取少量碳酸氢钠的方法:______.
(4)“纯碱中常常会混有少量氯化钠.”某研究性学习小组以一包纯碱(只考虑含氯化钠)为研究对象,探究纯碱样品中碳酸钠的含量.
【实验设计】
甲方案
Ⅰ.设计思路:根据样品与氯化钙溶液反应生成沉淀碳酸钙的质量,求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ.操作步骤:称取13.25g纯碱样品,加入过量的氯化钙溶液,充分搅拌.过滤、洗涤、干燥,得到的白色沉淀10.00g.
Ⅲ.数据处理:请根据上述实验数据,计算该样品中碳酸钠的质量分数.
计算过程:
______
乙方案
I.设计思路:根据样品(质量为a g)与稀硫酸完全反应生成二氧化碳的质量(质量为b g),求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
II.实验结论:
(1)当a、b的质量关系满足______(填写含a、b字母的表达式,下同)时,纯碱样品中只含有碳酸钠,样品中碳酸钠的质量分数是100%.
(2)当a、b的质量关系满足______时,纯碱样品室有碳酸钠和少量氯化钠组成的混合物,样品中碳酸钠的质量分数是______.
【实验评价】
误差分析:
(一)甲方案中,白色沉淀的质量在过滤、干燥等操作过程中会有所损耗,造成计算结果与实际值相比偏小.如果将氯化钙溶液换成氯化钡溶液,则可以使误差减小,理由是______.
(二)乙方案中,有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比______(填“偏大”、“偏小”、或“不变”).八年级化学解答题中等难度题查看答案及解析