-
海水资源的利用具有非常广阔的前景。
(1)海水的潮起潮落蕴含巨大的能量,潮汐能和________(写一种)属于新能源。海底矿产“可燃冰”的开发产品与天然气的主要成份相同, 是________(写化学式)
(2)海水淡化是解决淡水资源危机的有效途径之一,下列水的净化方法中,能使海水淡化的是________(填序号,下同)。
①过滤 ②吸附 ③蒸馏 ④消毒
(3)从海水中提炼出来的重水(D2O)可作原子能反应堆的中子减速剂和传热介质,重水中的D原子核内有一个质子、一个中子,下列说法正确的是________。
①D原子与氢原子属于同种元素 ②重水的相对分子质量为18
③D原子核外有一个电子 ④D原子的相对原子质量为2
(4)海水中含有多种盐,如氯化钠、氯化镁等。海水晒盐大致经历图1所示的过程

①图2是苦卤中有关物质的溶解度曲线,已知t1℃时,氯化镁和氯化钾的溶解度分别为M、N,则它们溶解度大小的关系为_____________:将苦卤加热到t2℃以上,根据溶解度曲线,首先析出的晶体应是__________。
②在晒盐时,海水中的氯化镁等也有少量结晶析出,所以海盐生产要经历用饱和食盐水洗盐的过程,采用饱和食盐水做洗液的原因是________。
-
海水资源的利用具有非常广阔的前景.
(1)海水的潮起潮落蕴含巨大的能量,潮汐能和________(写一种)属于新能源.海底矿产“可燃冰”的开发产品与天然气的主要成份相同,是________(写化学式)
(2)海水淡化是解决淡水资源危机的有效途径之一,下列水的净化方法中,能使海水淡化的是________(填序号,下同).
①过滤 ②吸附 ③蒸馏 ④消毒
(3)从海水中提炼出来的重水(D2O)可作原子能反应堆的中子减速剂和传热介质,重水中的D原子核内有一个质子、一个中子,下列说法正确的是________.
①D原子与氢原子属于同种元素 ②重水的相对分子质量为18
③D原子核外有一个电子 ④D原子的相对原子质量为2
(4)海水中含有多种盐,如氯化钠、氯化镁等.海水晒盐大致经历图1所示的过程

①图2是苦卤中有关物质的溶解度曲线,已知t1℃时,氯化镁和氯化钾的溶解度分别为M、N,则它们溶解度大小的关系为________:将苦卤加热到t2℃以上,根据溶解度曲线,首先析出的晶体应是________.
②在晒盐时,海水中的氯化镁等也有少量结晶析出,所以海盐生产要经历用饱和食盐水洗盐的过程,采用饱和食盐水做洗液的原因是________.
-
海洋是地球上最大的聚宝盆,浩瀚的海洋蕴含着丰富的化学资源,海水中化学资源的利用具有非常广阔的前景,目前世界上60%的镁是从海水中提取的,主要步骤如下图
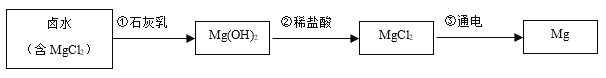
(1)在第①步中观察到的实验现象是_____。
(2)步骤②产生的氯化镁的质量与原卤水中氯化镁的质量相比_____(填“增大”、“减小”或“不变”之一)。
(3)某兴趣小组的同学取一定量的氢氧化镁固体,放入干净的烧杯中,向其中逐滴加入溶质质量分数为10%的稀盐酸,烧杯中固体的质量与加入稀盐酸的质量关系如图所示,当加入10%的稀盐酸73g(即A点)时,请通过计算,求此时所得不饱和溶液的质量_____。
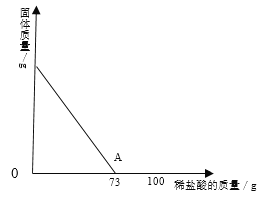
-
海洋是一个远未完全开发的巨大化学资源宝库,海洋资源的综合利用具有非常广阔的前景。工业上从海水中可提取许多广泛应用于生活、生产、科技等方面的物质和原料。
Ι.从海水中获得淡水
下列方法常用于海水淡化的是____________(填字母)。
A.蒸馏法 B.吸附法 C.沉淀法 D.过滤法
Ⅱ.从海水中提取溴(Br2)
工业上通常是将氯气通入海水晒盐后的母液中,将溶液中的溴化钠(NaBr)转化为溴单质(Br2),然后鼓入热空气,使溴单质(Br2)从溶液中挥发出来,冷凝后得到粗溴。该过程中主要反应的化学方程式为_______________________,其反应类型是______________。
Ⅲ.从海水中提取金属镁
镁及其合金是一种用途很广的金属材料,工业上从海水晒盐后的母液中提取镁的主要流程如下:
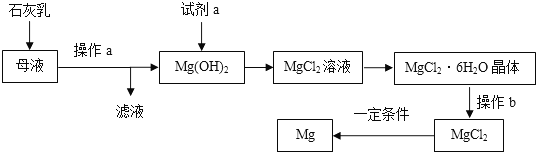
试回答下列问题:
(1)石灰乳主要成分的化学式为_____________。
(2)Mg(OH)2中加入试剂a发生反应的化学方程式为____________________________。
(3)操作b是在HCl气体氛围中高温灼烧进行的。若直接灼烧MgCl2·6H2O晶体,则生成MgO和另外两种化合物,写出有关反应的化学方程式___________________________ 。
Ⅳ.以海水中提取的食盐为原料制备纯碱
制备过程中主要涉及以下三步反应:
① CO2+NH3+H2O ══NH4HCO3
② NH4HCO3 + NaCl══NaHCO3 ↓ + NH4Cl
③ 2NaHCO3  Na2CO3+ CO2 ↑ + H2O
Na2CO3+ CO2 ↑ + H2O
试回答下列问题:
(1)制备过程中可以直接循环回收利用的物质是H2O和__________________。
(2)在实验室里证明反应③中的NaHCO3已完全分解的具体操作是________。
(3)某化学兴趣小组认为,在碳酸氢钠完全分解的情况下,所得的纯碱中也会混有来自反应②中的杂质,为此他们进行了如下探究:
a.取2.2g纯碱样品,加水完全溶解得100g溶液;
b.配制100g 3.65%的稀盐酸;
c.取上述一种溶液25g于锥形瓶中,再将另一种溶液逐滴加入锥形瓶内,反应后溶液的pH变化情况如下图所示。
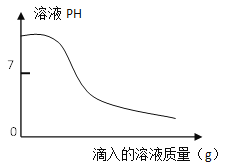
步骤c中当滴入另一种溶液为10g时,锥形瓶内物质恰好完全反应。则纯碱样品中碳酸钠的质量分数为___________(写出计算过程,计算结果保留1位小数)
-
海洋是一个远未完全开发的巨大化学资源宝库,海洋资源的综合利用具有非常广阔的前景。工业上从海水中可提取许多广泛应用于生活、生产、科技等方面的物质和原料。
Ι.从海水中获得淡水
下列方法常用于海水淡化的是____________(填字母)。
A.蒸馏法 B.吸附法 C.沉淀法 D.过滤法
Ⅱ.从海水中提取溴(Br2)
工业上通常是将氯气通入海水晒盐后的母液中,将溶液中的溴化钠(NaBr)转化为溴单质(Br2),然后鼓入热空气,使溴单质(Br2)从溶液中挥发出来,冷凝后得到粗溴。该过程中主要反应的化学方程式为_______________________,其反应类型是______________。
Ⅲ.从海水中提取金属镁
镁及其合金是一种用途很广的金属材料,工业上从海水晒盐后的母液中提取镁的主要流程如下:
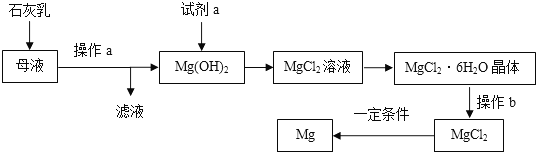
试回答下列问题:
(1)石灰乳主要成分的化学式为_____________。
(2)Mg(OH)2中加入试剂a发生反应的化学方程式为____________________________。
(3)操作b是在HCl气体氛围中高温灼烧进行的。若直接灼烧MgCl2·6H2O晶体,则生成MgO和另外两种化合物,写出有关反应的化学方程式___________________________ 。
Ⅳ.以海水中提取的食盐为原料制备纯碱
制备过程中主要涉及以下三步反应:
① CO2+NH3+H2O ══NH4HCO3
② NH4HCO3 + NaCl══NaHCO3 ↓ + NH4Cl
③ 2NaHCO3  Na2CO3+ CO2 ↑ + H2O
Na2CO3+ CO2 ↑ + H2O
试回答下列问题:
(1)制备过程中可以直接循环回收利用的物质是H2O和__________________。
(2)在实验室里证明反应③中的NaHCO3已完全分解的具体操作是________。
(3)某化学兴趣小组认为,在碳酸氢钠完全分解的情况下,所得的纯碱中也会混有来自反应②中的杂质,为此他们进行了如下探究:
a.取2.2g纯碱样品,加水完全溶解得100g溶液;
b.配制100g 3.65%的稀盐酸;
c.取上述一种溶液25g于锥形瓶中,再将另一种溶液逐滴加入锥形瓶内,反应后溶液的pH变化情况如下图所示。
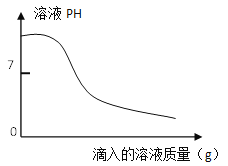
步骤c中当滴入另一种溶液为10g时,锥形瓶内物质恰好完全反应。则纯碱样品中碳酸钠的质量分数为___________(写出计算过程,计算结果保留1位小数)
-
海洋是地球上最大的储水库,浩瀚的海洋蕴含着丰富的化学资源.我市具有较长的海岸线,海洋资源开发前景广阔.
(1)目前海水淡化普遍采用的方法是,证明得到的水是淡水的方法是.
(2)海底不仅蕴藏着大量的煤、石油、天然气等常规化石燃料,人们还在海底发现了一种新型矿产资源是,被科学家誉为“21世纪能源”.
(3)海水晒盐能够得到粗盐和卤水.
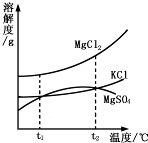
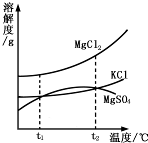
①卤水中含有MgCl2、KCl和MgSO4等物质,右图是它们的溶解度曲线.t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是.将t1℃的MgCl2、KCl和MgSO4三种物质的饱和溶液加热到t2℃以上时,会析出晶体(填名称).
②将粗盐提纯可以得到纯净的NaCl.欲用纯净的NaCl配制100g0.9%的生理盐水,需要NaCl的质量为克.配制该溶液时需要的玻璃仪器有.
-
海洋是地球上最大的储水库,浩瀚的海洋蕴含着丰富的化学资源.我市具有较长的海岸线,海洋资源开发前景广阔.
(1)目前海水淡化普遍采用的方法是,证明得到的水是淡水的方法是.
(2)海底不仅蕴藏着大量的煤、石油、天然气等常规化石燃料,人们还在海底发现了一种新型矿产资源是,被科学家誉为“21世纪能源”.
(3)海水晒盐能够得到粗盐和卤水.
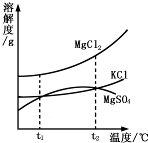
①卤水中含有MgCl2、KCl和MgSO4等物质,右图是它们的溶解度曲线.t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是.将t1℃的MgCl2、KCl和MgSO4三种物质的饱和溶液加热到t2℃以上时,会析出晶体(填名称).
②将粗盐提纯可以得到纯净的NaCl.欲用纯净的NaCl配制100g0.9%的生理盐水,需要NaCl的质量为克.配制该溶液时需要的玻璃仪器有.
-
海洋是地球上最大的储水库,浩瀚的海洋蕴含着丰富的化学资源.我市具有较长的海岸线,海洋资源开发前景广阔.
(1)目前海水淡化普遍采用的方法是,证明得到的水是淡水的方法是.
(2)海底不仅蕴藏着大量的煤、石油、天然气等常规化石燃料,人们还在海底发现了一种新型矿产资源是,被科学家誉为“21世纪能源”.
(3)海水晒盐能够得到粗盐和卤水.
①卤水中含有MgCl2、KCl和MgSO4等物质,右图是它们的溶解度曲线.t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是.将t1℃的MgCl2、KCl和MgSO4三种物质的饱和溶液加热到t2℃以上时,会析出晶体(填名称).
②将粗盐提纯可以得到纯净的NaCl.欲用纯净的NaCl配制100g0.9%的生理盐水,需要NaCl的质量为克.配制该溶液时需要的玻璃仪器有.
-
海洋是人类巨大的资源宝库,海洋资源的开发前景十分广阔。下列有关海洋资源的叙述错误的是( )
A.利用海水可以提取镁盐制取镁
B.海水中溶解盐的质量分数高达5%
C.海底蕴藏着大量的煤、石油和天然气
D.海洋中蕴含着丰富的海洋动力资源
-
海洋是人类巨大的资源宝库,海洋资源的开发前景十分广阔.下列有关海洋资源的叙述错误的是( )
A.利用海水可以提取镁盐制取镁
B.海水中溶解盐的质量分数高达5%
C.海底蕴藏着大量的煤、石油和天然气
D.海洋中蕴含着丰富的海洋动力资源










