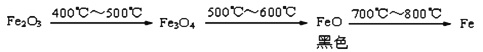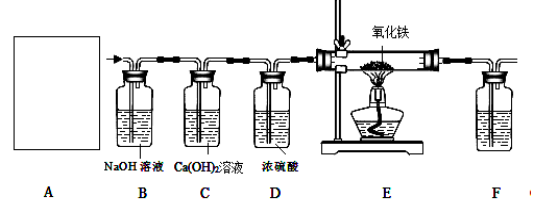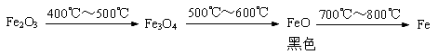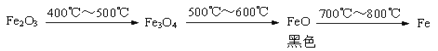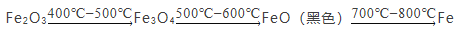-
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的应用
(1)下列铁制品的利用与金属导热性有关的是 (填字母,下同)。
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的 。
Ⅱ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式: ;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ;
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;
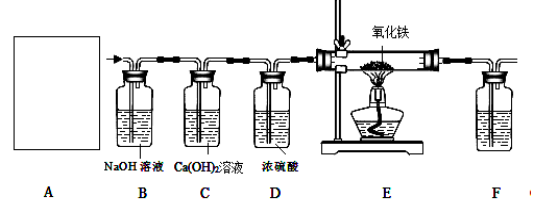
于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 (填装置编号);

(2)图中装置C、D的作用分别是 、 ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的 (填试剂名称),反应的化学方程式为 ;
(4)该装置设计有一个明显缺陷,你认为是 。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下:
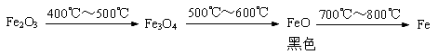
根据“无气泡”猜想,黑色粉末可能是:① Fe3O4 ;② ③ 。
(6)定量分析 用电子天平称量得部分数据如下:
| 玻璃管质量 | 玻璃管及其中固体的质量 | 装置F及其中物质的总质量 |
| 反应前 | 28.20 g | 33.00 g | 300.0 g |
| 反应后 | 32.84 g | 300.4 g |
根据上述数据,纯净的Fe2O3固体质量为 g,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程) 。
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式:
-
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的利用与金属导热性有关的是(填字母)。
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的。
II.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿(主要成分氧化铁)为原料,在高温下炼铁的化学方程式:;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能;
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:
①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,化学反应方程式为
H2C2O4 CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;浓硫酸具有强烈的吸水性
于是他设计了下图的实验装置,结合装置回答下列问题:

(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的(填装置编号);
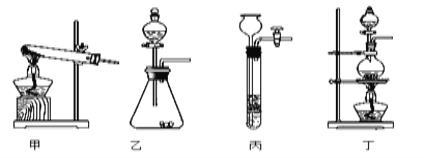
(2)图中装置C的作用是;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的(填试剂名称),反应的化学方程式为;
(4)该装置设计有一个明显缺陷,你认为是。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a.铁的氧化物在足量的稀盐酸中均能全部溶解。
b.Fe2O3与CO反应的固体生成物可能情况如下:
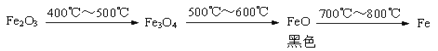
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;②③。
(6)定量分析用电子天平称量得部分数据如下:
| 玻璃管质量 | 玻璃管及其中固体的质量 | 装置F及其中物质的总质量 |
| 反应前 | 28.20g | 33.00g | 300.0g |
| 反应后 | 32.84g | 300.4g |
根据上述数据,纯净的Fe2O3固体质量为g,
请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程)(3分)
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式
-
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的利用与金属导热性有关的是_____(填字母,下同)。
A 铁钳 B 铁锅 C 刀具
(2)我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理________。
(3)某品牌的麦片中含微量铁粉,食用后可在胃酸(主要成分是盐酸)的作用下转化为人体可吸收的铁元素,反应的化学方程式为______________。
(4)“纳米α-Fe粉”可用于食品保鲜,称为“双吸剂”,因为它能吸收空气中的____和_____。
II.铁的冶炼。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:________;
(2)高炉炼铁中,焦炭的作用_________,_____。(用化学方程式表示)
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
(查阅资料):
①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
②NaOH溶液可以吸收二氧化碳。
③浓硫酸是一种常用的干燥剂。于是他设计了下图的实验装置,结合装置回答下列问题:
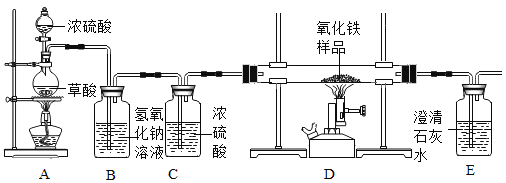
(1)图中装置C作用是_____________;
(2)装置E中澄清石灰水的作用是_______;
(3)从实验操作程序和实验安全看,首先要检查装置的气密性,实验开始先加热_____(填A或D)处。实验结束应_____(先或后)停止加热该处,这样做的主要目的是_______。
(4)该装置设计有一个明显缺陷,你认为是____________。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当D中固体全部变黑后,停止加热,继续通入CO直到玻璃管冷却。将得到的黑色固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
(查阅资料):a.铁的氧化物在足量的稀盐酸中均能全部溶解,但无气泡产生。
b.Fe2O3与CO反应的固体生成物可能情况如下:
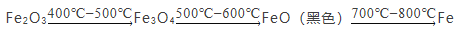
根据“无气泡”猜想,黑色粉末可能是:① Fe3O4 ;②__________ ;③Fe3O4 和FeO。
(6)定量分析 用电子天平称量得部分数据如下:(玻璃管质量60.0 g)
| 反应前 | 反应后 |
| 玻璃管及其中固体的质量 | 66.0g | 65.8 g |
根据上述数据,纯净的Fe2O3固体质量为_______g,通过上述数据,可推断出反应后黑色固体的成分_________, 根据推断结果,写出该实验中玻璃管内发生的化学反应方程式:_____。
-
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的利用与金属导热性有关的是________(填字母,下同)。
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可用于食品保鲜,称为“双吸剂”,因为它能吸收空气中的____和_____。
II.铁的冶炼 请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:______;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能_______。
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
(查阅资料):
①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:
H2C2O4  CO2
CO2 +CO
+CO +H
+H O
O
②NaOH溶液可以吸收二氧化碳, ③ 浓硫酸是一种常用的干燥剂。
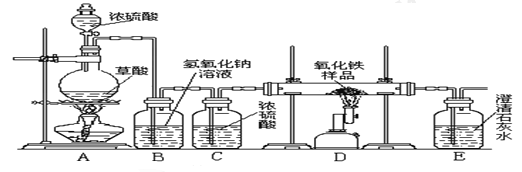
于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图中装置C作用是_______________;
(2)装置E中澄清石灰水的作用是________________,该反应化学方程式为_____________;
(3)从实验操作程序和实验安全看,首先要检查装置的气密性,实验开始先加热__________(填A或D)处。实验结束应先停止加热该处,这样做的目的除了可防止生成的铁被氧化,还可以起到的目的是___________。
(4)该装置设计有一个明显缺陷,你认为是_________。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当D中固体全部变黑后,停止加热,继续通入CO直到玻璃管冷却。将得到的黑色固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
(查阅资料):a. 铁的氧化物在足量的稀盐酸中均能全部溶解,但无气泡产生。
b. Fe2O3与CO反应的固体生成物可能情况如下:
根据“无气泡”猜想,黑色粉末可能是:① Fe3O4 ;②__________ ;③Fe3O4 和Fe O 。
(6)定量分析 用电子天平称量得部分数据如下:
| 玻璃管质量 | 玻璃管及其中固体的质量 | 装置E及其中物质的总质量 |
| 反应前 | 28.20 g | 37.80g | 300.0 g |
| 反应后 | 37.48 g | 300.8 g |
根据上述数据,纯净的Fe2O3固体质量为_______ g,请选择有效的数据,推断出反应后黑色固体的成分 _____________, 根据推断结果,写出该实验中玻璃管内发生的化学反应方程式:_____________。
-
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的利用与金属导热性有关的是_________________
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的_______。
II.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:______________;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能____________。
Ⅲ.铁的活动性探究
现用一定量的AgNO3和Cu (NO3)2混合溶液,进行了如下图所示的实验,并对溶液A和固体B的成分进行了分析和研究.

【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】
①只有Zn(NO3)2
②有Zn(NO3)2、AgNO3
③有Zn(NO3)2、Cu(NO3)2
④有Zn(NO3)2、Cu(NO3)2、AgNO3
【交流讨论】不合理的猜想是_______(填标号),其理由是__________
【实验探究】根据如表中的实验步骤及现象,完成表中的实验结论
| 实验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加稀盐酸 | 有气泡产生 | 溶液A中的溶质成分符合猜想__, 固体B中的金属成分有________种. |
Ⅳ.生铁中铁含量的测定
某课外兴趣小组测定生铁(含杂质的铁,杂质既不溶于水也不溶于酸)中铁的质量分数,他们取五份样品,分别加稀硫酸反应.测得部分数据如下,请根据有关信息回答问题.
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 取样品质量(g) | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 |
| 取稀硫酸质量(g) | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 产生气体质量(g) | 0.2 | a | 0.6 | 0.8 | 0.9 |
(1)a的数值为_______________.
(2)第5次实验结束后,所得到溶液中溶质的化学式为_________________.
(3)列式计算该样品中单质铁的质量分数是______________。
(4)所用稀硫酸的溶质的质量分数为____________。
-
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ铁的应用
(1)下列铁制品的利用与金属导热性有关的是____________(填字母):
A铁铲 B铁锅 C刀具
(2)“纳米a-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的_____________;
Ⅱ铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从其氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:______________;
(2)高炉炼铁中,焦炭的作用除了可以提供热量外,还能________________;
Ⅲ实验探究炼铁原理:
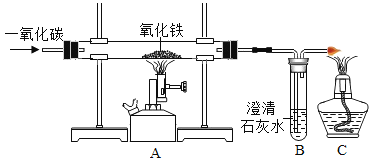
某化学兴趣小组的同学利用上图装置模拟工业炼铁的过程,请按要求填空:、
(1)实验时装置A中的现象是_____________;
(2)B中发生反应的化学方程式:_____________;
(3)实验过程中,CO的作用有____________(填序号);
①CO气体作为反应物;②实验开始时,排尽装置中的空气,防止加热时发生爆炸;③停止加热后,防止A中生成物被氧化;④停止加热后防止B中的溶液倒吸入A中。
Ⅳ拓展延伸
利用上面的装置测定某铁的氧化物中铁元素和氧元素的质量比。实验记录数据如下:①装铁的氧化物的硬质玻璃管的质量为20g;②硬质玻璃管与铁的氧化物的质量共为26.4g;③通入一氧化碳并加热至铁的氧化物全部转化为铁后,生成的二氧化碳全部被澄清石灰水吸收,且B中生成沉淀的质量为12g。
根据以上实验记录,计算此铁的氧化物中铁元素和氧元素的质量比____________。
-
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的应用与金属导热性有关的是_____。
A 铁锤 B 铁锅 C 菜刀
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的_____。
II.铁的冶炼
工业炼铁的主要反应原理是在高温下CO夺取铁矿石里的氧,将铁还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:_____;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能_____。
Ⅲ.铁的活动性探究
现用一定量的AgNO3和Cu (NO3)2混合溶液,进行了如下图所示的实验,并对溶液A和固体B的成分进行了分析和研究。
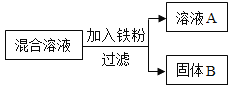
(提出问题)溶液A中的溶质成分可能有哪些?
(作出猜想)
①只有Fe(NO3)2
②有Fe(NO3)2、AgNO3
③有Fe(NO3)2、Cu(NO3)2
④有Fe(NO3)2、Cu(NO3)2、AgNO3
(交流讨论)不合理的猜想是_____(填序号)。
(实验探究)根据下表中的实验步骤及现象,完成表中的实验结论。
| 实验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加稀盐酸 | 有气泡产生 | 溶液A中的溶质成分符合猜想_____(填序号),固体B中有_____种金属。 |
Ⅳ.生铁中铁含量的测定
某课外兴趣小组测定生铁(含杂质的铁,杂质既不溶于水也不溶于酸)中铁的质量分数,他们取6份样品,分别与稀硫酸反应。测得数据如下,请根据有关信息回答问题。
| 实验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 取样品质量(g) | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 |
| 取稀硫酸质量(g) | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 | 300.0 |
| 产生气体质量(g) | 0.2 | 0.4 | 0.6 | 0.8 | 1.0 | 1.05 |
(1)第5次实验结束后,所得溶液中溶质的化学式为_____。
(2)所用稀硫酸中溶质的质量分数为_____。
(3)若配制上述浓度的稀硫酸100克,则需质量分数为98%的浓硫酸_____克。
(4)计算该样品中铁的质量分数是_____。(写出计算过程)
-
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的应用与金属导热性有关的是_____。
A 铁锤 B 铁锅 C 菜刀
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的_____。
II.铁的冶炼
工业炼铁的主要反应原理是在高温下CO夺取铁矿石里的氧,将铁还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:_____;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能_____。
Ⅲ.铁的活动性探究
现用一定量的AgNO3和Cu (NO3)2混合溶液,进行了如下图所示的实验,并对溶液A和固体B的成分进行了分析和研究。
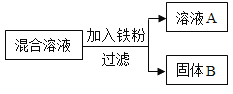
(提出问题)溶液A中的溶质成分可能有哪些?
(作出猜想)
①只有Fe(NO3)2
②有Fe(NO3)2、AgNO3
③有Fe(NO3)2、Cu(NO3)2
④有Fe(NO3)2、Cu(NO3)2、AgNO3
(交流讨论)不合理的猜想是_____(填序号)。
(实验探究)根据下表中的实验步骤及现象,完成表中的实验结论。
| 实验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加稀盐酸 | 有气泡产生 | 溶液A中的溶质成分符合猜想_____(填序号),固体B中有_____种金属。 |
Ⅳ.生铁中铁含量的测定
某课外兴趣小组测定生铁(含杂质的铁,杂质既不溶于水也不溶于酸)中铁的质量分数,他们取6份样品,分别与稀硫酸反应。测得数据如下,请根据有关信息回答问题。
| 实验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 取样品质量(g) | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 |
| 取稀硫酸质量(g) | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 | 300.0 |
| 产生气体质量(g) | 0.2 | 0.4 | 0.6 | 0.8 | 1.0 | 1.05 |
(1)第5次实验结束后,所得溶液中溶质的化学式为_____。
(2)所用稀硫酸中溶质的质量分数为_____。
(3)若配制上述浓度的稀硫酸100克,则需质量分数为98%的浓硫酸_____克。
(4)计算该样品中铁的质量分数是_____。(写出计算过程)
-
金属和金属材料在生产、生活中应用非常广泛.
(1)钢铁很容易锈蚀,锈蚀后形成的铁锈可用稀盐酸除去,该反应方程式是 .
(2)铝制成铝锅,是利用了铝的 性和导热性,铝制品不易锈蚀的原因是 .
(3)探究铁、铜的金属活动性顺序,除铁、铜外,还需要一种试剂,你选择的试剂是 (填序号,可多选).
①AgNO3溶液 ②CuSO4溶液 ③Al2(SO4)3溶液 ④H2SO4溶液 ⑤FeSO4溶液.
-
(2009•西城区一模)金属材料在生产、生活中应用广泛.
(1)下列铁制品中,利用金属导热性的是(填序号).

(2)联合钢铁工业的基本生产流程示意图如:
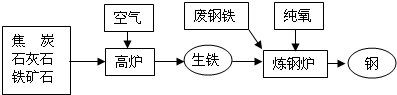
石灰石、生铁和钢均属于(填“纯净物”或“混合物”).生铁和钢的主要区别是.写出以赤铁矿(主要成分是氧化铁)为原料,用一氧化碳冶炼生铁的化学方程式为.
(3)颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”.实验室制备的方法是:以高纯氮气作保护气,在高温条件下用氢气和氯化亚铁发生置换反应,生成“纳米铁”,反应的化学方程式为.
(4)氯化铁能腐蚀铜(2FeCl3+Cu=2FeCl2+CuCl2),工业上常用此原理生产印刷线路板.
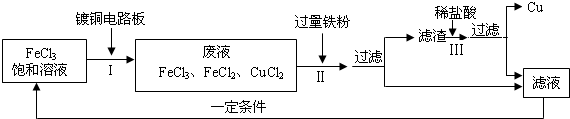
步骤Ⅱ中发生了两个反应:2FeCl3+Fe=3FeCl2和;滤渣的成分有.
CO2
+CO
+H
O