-
探究某氧化铜与炭的混合物中氧化铜的质量分数,取样品10g进行如下实验。查阅资料:氧气能与热的铜反应生成氧化铜。
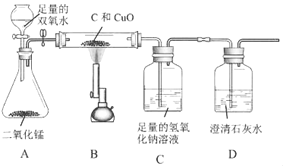
(1)关闭弹簧夹,高温加热装置B,观察黑色固体部分变___,有关反应的化学方程式是___;装置C增加1.1g后质量不再增加,装置C中吸收了___mol的气体,由此可知装置B中___。
a.氧化铜过量 b.炭过量 c.恰好完全反应 d.无法判断
(2)装置D的作用是___。
(3)打开活塞和弹簧夹,装置A中发生的化学方程式是___,装置C的质量又增加,则观察到装置B中红色固体又变黑色,同时看到___,用化学方程式解释装置C质量增加的原因___、___。
(4)实验过程中,通入装置B中氧气的量大于参与反应的量,请设计一个简单的实验加以证明___。
-
超氧化钾(KO2)是一种黄色固体,可用作呼吸面具的供氧剂。实验室有一瓶放置较长时间的超氧化钾样品,某化学兴趣小组对其成分和性质进行了如下探究。
(查阅资料)Ⅰ超氧化钾能与空气中水或二氧化碳反应生成氧气并放热:
4KO2+2CO2==2K2CO3+3O2,4KO2+2H2O==4KOH+3O2↑。
(提出问题)超氧化钾是否变质?
(猜想与假设)假设1:超氧化钾未变质;假设2:_____;假设3:超氧化钾全部变质。
(实验探究)
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加入足量的水,在试管口插入带火星的木条。 | 固体完全溶解,放热,木条复燃 | 假设_____不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的_____, 振荡。 | 有气泡生成 | 假设2成立 |
(提出新问题)部分变质的超氧化钾样品中是否含有氢氧化钾呢?
(实验探究)③取少量①中溶液于试管中,加入足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红。
(定性分析)(l)由实验探究③可以确定①中溶液含有的溶质是_____(填化学式);
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钾,理由是_____。
(反思提高)超氧化钾长时间露置在空气中会全部变质,最终转化为_____(填化学式)。
-
(10分)过氧化钠(Na2O2)可用作呼吸面具的供氧剂.实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.
【查阅资料】1.过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2 O2 +2H2 O=4NaOH+02↑,2Na202+2C02==2Na2CO3+O2.
【提出问题]1.过氧化钠是否变质?
【猜想与假设】
假设1:过氧化钠未变质;假设2:过氧化钠部分变质;假设3:过氧化钠全部变质.
【实验探究】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解,木条复然 | 假设_____ 不成立 |
| 取少量①中溶液于试管中,滴加足量的 ______,振荡. | 有气泡生成 | 假设2成立 |
| | | |
【提出新问题】部分变质的过氧化钠中是否含有氢氧化钠?
【实验探究】取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层 清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】
(1)由实验③可以确定①中溶液含有的溶质是_______(填化学式);
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是_________。
【定量研究】称取6.04g的过氧化钠样品于锥形瓶中,加入足量的蒸馏水,共收集到气体0.64g,再向上述锥形瓶中加入足量的澄清石灰水,充分反应后,经过沉淀、过滤、干燥等,得到固体2.00g。
写出加入澄清石灰水的反应方程式__________________________
6.04g上述样品中,含氢氧化钠的质量_______________。
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为_______(填化学式)
-
(10分)过氧化钠(Na2O2)可用作呼吸面具的供氧剂.实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.
【查阅资料】1.过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2+2H2O=4NaOH+02↑, 2Na202+2C02==2Na2CO3+O2.
【提出问题】1.过氧化钠是否变质?
【猜想与假设】
假设1:过氧化钠未变质; 假设2:过氧化钠部分变质; 假设3:过氧化钠全部变质.
【实验探究】

【提出新问题】部分变质的过氧化钠中是否含有氢氧化钠?
【实验探究】③取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】
(1)由实验③可以确定①中溶液含有的溶质是___ ____(填化学式);
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是_________。
【定量研究】称取6.04g的过氧化钠样品于锥形瓶中,加入足量的蒸馏水,共收集到气体0.64g,再向上述锥形瓶中加入足量的澄清石灰水,充分反应后,经过沉淀、过滤、干燥等,得到固体2.00g。
(1)写出加入澄清石灰水的反应方程式_____________________
(2)6.04g上述样品中,含氢氧化钠的质量_______________。
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为 (填化学式)
-
过氧化钠(Na2O2)可用作呼吸面具的供氧剂.实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.
【查阅资料】过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2 +2H2O=4NaOH+O2↑, 2Na2O2+2CO2==2Na2CO3+O2.
【提出问题】过氧化钠是否变质?
【猜想与假设】假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:过氧化钠全部变质.
【实验探究】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解,木条复然 | 假设____ 不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的__ ____,振荡. | 有气泡生成 | 假设2成立 |
【提出新问题】部分变质的过氧化钠中是否含有氢氧化钠?
【实验探究】实验③:取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】(1)由实验③可以确定①中溶液含有的溶质是___________(填化学式);实验③中所发生的化学方程式为:_____________________
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是_______。
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为______(填化学式)
-
过氧化钠(Na2O2)可用作呼吸面具的供氧剂。实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究。
[查阅资料]过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2 +2H2O=4NaOH+O2↑
2Na2O2+2CO2 =2Na2CO3+O2
[提出问题]过氧化钠是否变质?
[提出猜想]猜想一:________;
猜想二:过氧化钠部分变质;
猜想三:过氧化钠全部变质。
[实验探究]
| 实验操作 | 实验现象 | 实验结论 |
| ①取部分固体于试管中,加入适量水,在试管口插入带火星木条 | 固体溶解,有气泡产生_______ | 猜想三不成立 |
| ②取少量①中溶液于另一试管中,滴加足量_______,振荡 | 有气泡生成 | 猜想二成立 |
[反思评价]
(1)请写出实验②中产生气泡的化学反应方程式_________;
(2)小华同学想通过实验,进一步确定部分变质的过氧化钠中是否含有氢氧化钠,于是进行了如下的实验操作:取少量①中溶液于试管中,加入足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中加入少量________,溶液变红,证明部分变质的过氧化钠中含有氢氧化钠。
(3)小明同学认为,小华同学的实验仍无法确定原固体样品中是否含有氢氧化钠,理由是________。
-
(2009•朝阳区一模)化学实验小组讨论测定双氧水溶液中溶质的质量分数的实验方案.
查阅资料:常温下氧气密度为1.42g/L.
设计原理:将一定质量的双氧水样品与二氧化锰混合,测定反应产生氧气的质量.

过程方法:
(1)组长首先设计了A装置:向质量为75 g的锥形瓶中加入0.5g二氧化锰和20 g双氧水溶液,待反应完毕后测得锥形瓶和反应后混合物的总质量为94.7g.请写出该反应的化学方程式______ 2H2O+O2↑
-
市售某品牌饮料的罐体是A1-Fe合金,为测定其中Al的质量分数,某学习小组精确称取0.050g合金样品,设计了如下装置并进行实验:
[查阅资料]:
1、Al和NaOH溶液反应,放热并生成H2,反应中对应关系为2Al~3H2,Fe和NaOH溶液不反应;2、实验条件下,H2的密度近似为0.090g•L-1.
[实验步骤]:
①______;
②装入药品和水,连接装置;
③记录量气管中水面读数为5mL;
④打开分液漏斗活塞,逐滴滴入NaOH溶液,至不再产生气泡为止,关闭活塞;
⑤待温度降至室温时,记录量气管中水面读数为49mL;
⑥处理剩余药品,整理实验台.
[实验分析及数据处理]:
(1)完善实验步骤中的所缺部分;
(2)检查气密性的方法:打开分液漏斗活塞,向量气管中加入水,使水准管和量气管中水面相平,关闭活塞,降低量气管,若两侧水面高度差______(填“改变”或“不变”),则气密性良好;
(3)实验结束后,读取量气管中水面刻度之前,需进行的操作是______;
(4)计算此A1-Fe合金样品中Al的质量分数(精确到小数点后3位);______;
[实验反思]:
(5)造成实验结果偏大的原因可能是______.
A.实验过程加入NaOH溶液的体积 B.没有冷却至室温就开始读数 C.装置漏气.
-
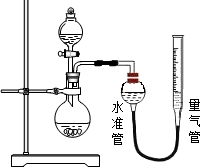
市售某品牌饮料的罐体是A1-Fe合金,为测定其中Al的质量分数,某学习小组精确称取0.050g合金样品,设计了如下装置并进行实验:
[查阅资料]:
1、Al和NaOH溶液反应,放热并生成H2,反应中对应关系为2Al~3H2,Fe和NaOH溶液不反应;2、实验条件下,H2的密度近似为0.090g•L-1.
[实验步骤]:
①______;
②装入药品和水,连接装置;
③记录量气管中水面读数为5mL;
④打开分液漏斗活塞,逐滴滴入NaOH溶液,至不再产生气泡为止,关闭活塞;
⑤待温度降至室温时,记录量气管中水面读数为49mL;
⑥处理剩余药品,整理实验台.
[实验分析及数据处理]:
(1)完善实验步骤中的所缺部分;
(2)检查气密性的方法:打开分液漏斗活塞,向量气管中加入水,使水准管和量气管中水面相平,关闭活塞,降低量气管,若两侧水面高度差______(填“改变”或“不变”),则气密性良好;
(3)实验结束后,读取量气管中水面刻度之前,需进行的操作是______;
(4)计算此A1-Fe合金样品中Al的质量分数(精确到小数点后3位);______;
[实验反思]:
(5)造成实验结果偏大的原因可能是______.
A.实验过程加入NaOH溶液的体积 B.没有冷却至室温就开始读数 C.装置漏气.
-
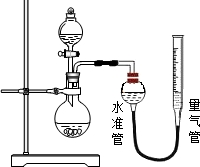
(7分)市售某品牌饮料的罐体是A1—Fe合金,为测定其中Al的质量分数,某学习小组精确称取0.050 g合金样品,设计了如下装置并进行实验:
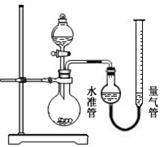
【查阅资料】:1、Al和NaOH溶液反应,放热并生成H2,反应中对应关系为2Al ~ 3H2,Fe和NaOH溶液不反应;2、实验条件下,H2的密度近似为0.090 g·L—1。
【实验步骤】:
①________;②装入药品和水,连接装置;③记录量气管中水面读数为5 mL;④打开分液漏斗活塞,逐滴滴入NaOH溶液,至不再产生气泡为止,关闭活塞;⑤待温度降至室温时,记录量气管中水面读数为49 mL;⑥处理剩余药品,整理实验台。
【实验分析及数据处理】:
(1)完善实验步骤中的所缺部分;
(2)检查气密性的方法:打开分液漏斗活塞,向量气管中加入水,使水准管和量气管中水面相平,关闭活塞,降低量气管,若两侧水面高度差________(填“改变”或“不变”),则气密性良好;
(3)实验结束后,读取量气管中水面刻度之前,需进行的操作是________;
(4)计算此A1—Fe合金样品中Al的质量分数(3分,精确到小数点后3位);________;
【实验反思】:
(5)造成实验结果偏大的原因可能是________。
A.实验过程加入NaOH溶液的体积
B.没有冷却至室温就开始读数
C.装置漏气





