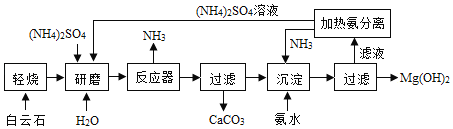
工业上以白云石(主要成分为CaCO3•MgCO3)为原料制备氢氧化镁的流程如图所示,请回答以下问题:
温馨提示:
①轻烧时温度低于700℃
②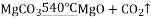
③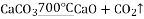
④
(1)写出白云石轻烧后所得固体的主要成分_____;
(2)请分析流程中研磨的目的_____;
(3)写出流程中除水以外可以循环利用的物质_____;(写出一种)
(4)请分析如果轻烧时温度超过700℃对流程产生的影响。_____
九年级化学流程题困难题
工业上以白云石(主要成分为CaCO3•MgCO3)为原料制备氢氧化镁的流程如图所示,请回答以下问题:

温馨提示:
①轻烧时温度低于700℃
②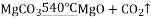
③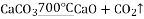
④
(1)写出白云石轻烧后所得固体的主要成分_____;
(2)请分析流程中研磨的目的_____;
(3)写出流程中除水以外可以循环利用的物质_____;(写出一种)
(4)请分析如果轻烧时温度超过700℃对流程产生的影响。_____
九年级化学流程题困难题
工业上以白云石(主要成分为CaCO3•MgCO3)为原料制备氢氧化镁的流程如图所示,请回答以下问题:

温馨提示:
①轻烧时温度低于700℃
②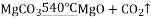
③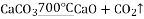
④
(1)写出白云石轻烧后所得固体的主要成分_____;
(2)请分析流程中研磨的目的_____;
(3)写出流程中除水以外可以循环利用的物质_____;(写出一种)
(4)请分析如果轻烧时温度超过700℃对流程产生的影响。_____
九年级化学流程题困难题查看答案及解析
以白云石(主要成分化学式为 MgCO3•CaCO3)为原料制备氢氧化镁的工艺流程如下图(流程图方框中的文字均表示操作过程):

(1)白云石属于________物(选填“混合”“纯净”),白云石“轻烧”过程中只发生了碳酸镁的分解,写出碳酸镁分解反应的化学方程式________________。
(2)流程图中“加热反应”是指硫酸铵与氧化镁在加热条件下反应生成一种盐、氨气和水,其化学方程式为____________________; 流程图中“沉淀”过程是指氨水和硫酸镁发生复分解反应,其化学方程式为_________________; 硫酸铵中氮元素的化合价是_________价。
(3)该工艺中可以循环使用的物质是_______________、(NH4)2SO4 等.
(4)传统制备氢氧化镁的工艺是将白云石高温下分解为氧化镁和氧化钙后再提取,而本工艺流程采用轻烧白云石的方法,其优点是______________(填写一条,合理即可).
九年级化学流程题中等难度题查看答案及解析
以白云石(主要成分为 MgCO3·CaCO3)为原料制备氢氧化镁的流程如下:
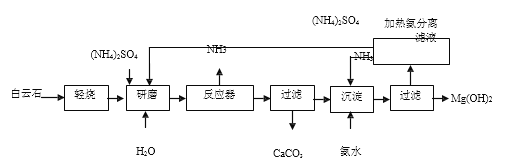
已知:MgCO3 MgO+CO2↑;CaCO3
CaO+CO2↑。
请回答下列问题:
(1)“研磨”的目的是___________,实验室“过滤”操作中玻璃棒的作用是_______。
(2)根据流程,“轻烧”温度不应超过______℃,“轻烧”后的固体主要成份是_____。
(3)该流程中可循环使用的物质是_______。
九年级化学流程题困难题查看答案及解析
以白云石(主要成分为CaCO3·MgCO3)为原料制备氢氧化镁的流程如下图:
已知:①MgCO3MgO+CO2↑,CaCO3
CaO+CO2↑ ;
②反应器中发生的反应是 (NH4)2SO4 + MgO MgSO4 + 2NH3↑+ H2O 。
(1)实验室进行过滤操作时,玻璃棒的作用是__________________。
(2)该流程中,研磨的目的是__________________;轻烧的温度不超过________℃,经轻烧得到的固体的主要成分是__________________(写化学式)。
(3)该流程中,不考虑H2O,可循环利用的物质是__________________(写化学式)。
九年级化学信息分析题中等难度题查看答案及解析
以白云石(主要成分为CaCO3·MgCO3)为原料制备氢氧化镁的流程如下图:
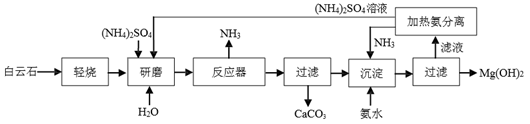
已知:①MgCO3MgO+CO2↑,CaCO3
CaO+CO2↑ ;
②反应器中发生的反应是(NH4)2SO4+MgO MgSO4+2NH3↑+H2O 。
(1)实验室进行过滤操作时,玻璃棒的作用是____________________。
(2)该流程中,研磨的目的是____________________;轻烧的温度不超过__________℃,经轻烧得到的固体的主要成分是____________________(写化学式)。
(3)该流程中,不考虑H2O,可循环利用的物质是____________________(写化学式)。
九年级化学探究题极难题查看答案及解析
七水硫酸镁(MgSO4·7H2O)是一种重要的化工原料,在48.1℃以下的潮湿空气中稳定,在温热干燥空气中易失去结晶水。工业上将白云石(主要成分为MgCO3、CaCO3)煅烧成粉,用于制取MgSO4·7H2O,工艺流程如下图所示:
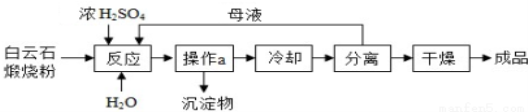
(1)煅烧过程中,MgCO3转化为MgO的基本反应类型是___ _________。
(2)写出MgO与H2SO4反应的化学方程式_____________ ____________。
(3)操作a的名称为_____ ___________。
(4)将分离后的母液循环利用的目的是____________ ___________________。
(5)干燥得成品时,需要控制的条件是_________ _______________。
九年级化学填空题困难题查看答案及解析
七水硫酸镁(MgSO4·7H2O)是一种重要的化工原料,在48.1℃以下的潮湿空气中稳定,在温热干燥空气中易失去结晶水。工业上将白云石(主要成分为MgCO3、CaCO3)煅烧成粉,用于制取MgSO4·7H2O,工艺流程如下图所示:
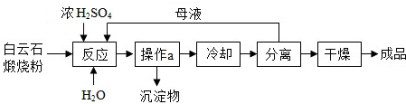
(1)煅烧过程中,MgCO3转化为MgO的基本反应类型是______________________。
(2)写出MgO与H2SO4反应的化学方程式_________________________。
(3)操作a的名称为________________。
(4)将分离后的母液循环利用的目的是_______________________________。
(5)干燥得成品时,需要控制的条件是__________________________________。
九年级化学填空题中等难度题查看答案及解析
工业上利用白云石(主要成分是CaCO3.MgCO3)制得结晶镁的主要流程如图:
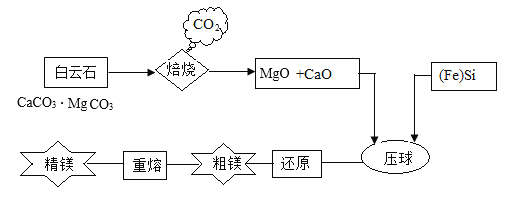
(1)生产上将白云石打碎的目的是_____。
(2)还原过程中发生的主要反应为:Si + 2MgO2Mg + SiO2 ,该反应中化合价发生改变的元素是_______。欲通过该反应生产24t镁,需要投入硅的质量是_______吨。
九年级化学综合题中等难度题查看答案及解析
工业上利用白云石(主要成分是 CaCO3·MgCO3)制得结晶镁的主要流程如图所示:
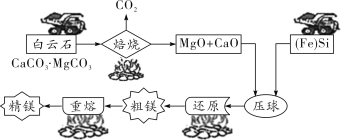
(1)生产上将白云石粉碎的目的是_____,白云石焙烧过程发生反应的化学方程式为_____。
(2)将白云石的焙烧产物和硅铁(含 75%Si)压制成球发生的是_____(填“物理”或“化学”)变化。
(3)还原过程中发生的主要反应为 2CaO+2MgO+Si2Mg+Ca2SiO4,该反应中化合价降低的元素是_____。采用真空操作除了能降低操作温度外,还具有的优点是_____。
九年级化学流程题中等难度题查看答案及解析
(7分)氧化镁在医药、建筑等行业应用广泛.硫酸镁还原热解制备高纯氧化镁是一种新的探索.以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
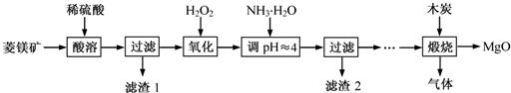
(1)MgCO3与稀硫酸反应的化学方程式为 ;
(2)加入H2O2 氧化时,发生反应的化学方程式为(已经配平,X属于常见的化合物):
,则X的化学式为 ;
(3)NH3·H2O是氨水的主要成分,溶液显 性,加入氨水时,溶液的PH值 (填“增大”、“减少”或“不变”),当PH≈4时,会产生红褐色沉淀,则滤渣2 的成分是 (填化学式)。
(4)通常用PH试纸测定溶液的PH值,其操作方法是 。
(5)煅烧过程存在以下反应:木炭和硫酸镁在高温下除得到氧化镁外,还得两种气体,一种会造成酸雨,另一种大量排放则会引起温室效应。请写出该反应的化学方程式: 。
九年级化学填空题困难题查看答案及解析