-
工业上生产电石 并制备重要工业原料乙炔
并制备重要工业原料乙炔 流程如下:
流程如下:
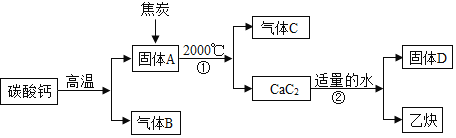
资料: .碳酸钙高温分解可得两种氧化物。
.碳酸钙高温分解可得两种氧化物。
 .乙炔的相对分子质量是26,一个乙炔分子有四个原子构成。
.乙炔的相对分子质量是26,一个乙炔分子有四个原子构成。
 .B、C组成的元素相同,C有毒。
.B、C组成的元素相同,C有毒。
(1)写出A、B、C的化学式:A______B______C______。
(2)反应①化学方程式为______。
(3)将一定量的乙炔 完全燃烧,生成
完全燃烧,生成 水和
水和 二氧化碳,则乙炔的化学式为______。
二氧化碳,则乙炔的化学式为______。
(4)若向D的澄清溶液中通入二氧化碳,有白色浑浊现象,则反应②的化学方程式为______。
-
工业上生产电石 并制备重要工业原料乙炔
并制备重要工业原料乙炔 流程如下:
流程如下:
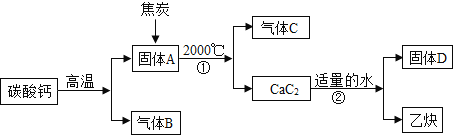
资料: .碳酸钙高温分解可得两种氧化物。
.碳酸钙高温分解可得两种氧化物。
 .乙炔的相对分子质量是26,一个乙炔分子有四个原子构成。
.乙炔的相对分子质量是26,一个乙炔分子有四个原子构成。
 .B、C组成的元素相同,C有毒。
.B、C组成的元素相同,C有毒。
(1)写出A、B、C的化学式:A______B______C______。
(2)反应①化学方程式为______。
(3)将一定量的乙炔 完全燃烧,生成
完全燃烧,生成 水和
水和 二氧化碳,则乙炔的化学式为______。
二氧化碳,则乙炔的化学式为______。
(4)若向D的澄清溶液中通入二氧化碳,有白色浑浊现象,则反应②的化学方程式为______。
-
工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如图1所示:

(资料)
(1)碳酸钙高温分解可得两种氧化物。
(2)浓硫酸具有强吸水性,NaOH溶液能吸收CO2。
(讨论)(1)C、B组成元素相同,C有毒,反应①化学方程式为_________。
(2)D微溶于水,溶解度随温度升高而减小,D的化学式是_________。
(测定乙炔组成)
资料:一个乙炔分子有四个原子构成。
(3)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过如图2所示的____(选填“甲”或“乙”)装置,并再缓缓通一段时间的N2,并记录实验数据于如表中。
| 装置 | 反应前质量 | 反应后质量 |
| 浓硫酸 | 125.3g | 127.1g |
| 浓NaOH溶液 | 78.2g | 87.0g |
(4)实验中“缓缓通一段时间的N2”的目的是_________。
(5)计算:乙炔中碳元素质量为_____g,氢元素质量为_____g
(6)乙炔的化学式为______________。
-
工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如图1所示:
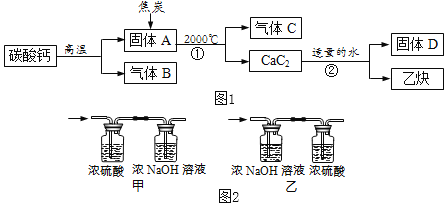
【资料】
①碳酸钙高温分解可得两种氧化物。
②浓硫酸具有强吸水性,NaOH溶液能吸收CO2。
【讨论】
(1)C、B组成元素相同,C有毒,反应①化学方程式为_____。
(2)D微溶于水,溶解度随温度升高而减小,D的化学式是_____。
【测定乙炔组成】
资料:一个乙炔分子有四个原子构成。
(3)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过如图2所示的_____(选填“甲”或“乙”)装置,并再缓缓通一段时间的N2,并记录实验数据于如表中。
| 装置 | 反应前质量 | 反应后质量 |
| 浓硫酸 | 125.3g | 127.1g |
| 浓NaOH溶液 | 78.2g | 87.0g |
(4)实验中“缓缓通一段时间的N2”的目的是_____。
(5)计算:乙炔中碳元素质量为_____g,氢元素质量为_____g,乙炔化学式为_____。
(6)反应②的化学方程式为_____。
-
工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如图1所示:
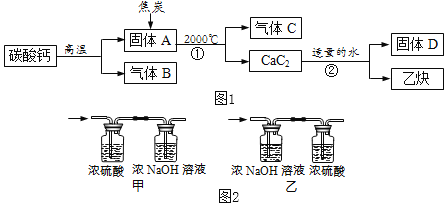
【资料】
①碳酸钙高温分解可得两种氧化物。
②浓硫酸具有强吸水性,NaOH溶液能吸收CO2。
【讨论】
(1)C、B组成元素相同,C有毒,反应①化学方程式为_____。
(2)D微溶于水,溶解度随温度升高而减小,D的化学式是_____。
【测定乙炔组成】
资料:一个乙炔分子有四个原子构成。
(3)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过如图2所示的_____(选填“甲”或“乙”)装置,并再缓缓通一段时间的N2,并记录实验数据于如表中。
| 装置 | 反应前质量 | 反应后质量 |
| 浓硫酸 | 125.3g | 127.1g |
| 浓NaOH溶液 | 78.2g | 87.0g |
(4)实验中“缓缓通一段时间的N2”的目的是_____。
(5)计算:乙炔中碳元素质量为_____g,氢元素质量为_____g,乙炔化学式为_____。
(6)反应②的化学方程式为_____。
-
工业上生产电石(CaC2)制备重要工业原料乙炔(CxHy)流程如下:
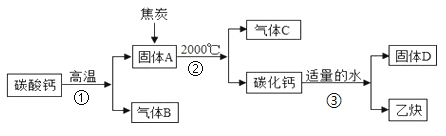
请回答下列问题:
(1)写出碳酸钙高温分解①的化学方程式____________________;B、C组成的元素相同,C有毒,则反应②的化学方程式____________________;根据反应③可推断固体D中一定含有的元素是____________________。
(2)已知:浓硫酸具有强吸水性。一个乙炔分子由4个原子构成。为了测定乙炔的组成,将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过下图的__________(选填“甲”或“乙”)装置,再缓缓通过一段时间的N2,缓缓通过一段时间的N2的目的是__________。
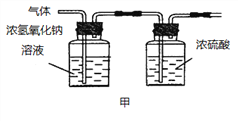

记录实验数据如下:
| 装置 | 反应前质量 | 反应后质量 |
| 浓硫酸 | 125.3g | 127.1g |
| 浓氢氧化钠溶液 | 78.2g | 87.0g |
根据实验数据推断乙炔的化学式(写出推断过程):__________
-
工业上生产电石(CaC2)制备重要工业原料乙炔(CxHy)流程如下:
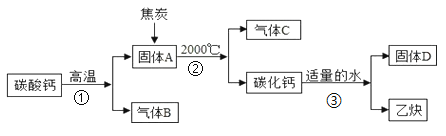
请回答下列问题:
(1)写出碳酸钙高温分解①的化学方程式____________________;B、C组成的元素相同,C有毒,则反应②的化学方程式____________________;根据反应③可推断固体D中一定含有的元素是____________________。
(2)已知:浓硫酸具有强吸水性。一个乙炔分子由4个原子构成。为了测定乙炔的组成,将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过下图的__________(选填“甲”或“乙”)装置,再缓缓通过一段时间的N2,缓缓通过一段时间的N2的目的是__________。
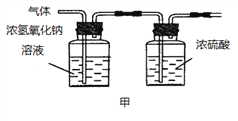
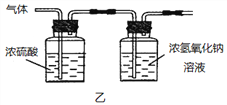
记录实验数据如下:
| 装置 | 反应前质量 | 反应后质量 |
| 浓硫酸 | 125.3g | 127.1g |
| 浓氢氧化钠溶液 | 78.2g | 87.0g |
根据实验数据推断乙炔的化学式(写出推断过程):__________
-
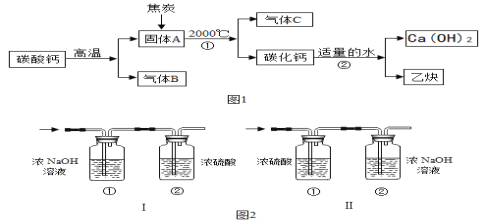
工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如图1:
(资料)
(1)CaCO3 CaO(固体)+CO2↑。
CaO(固体)+CO2↑。
(2)浓硫酸是常用的干燥剂,NaOH 溶液能吸收CO2。
(讨论)
(1)C、B组成元素相同,C有毒,反应①的化学方程式为_______。
(测定乙炔组成)资料:一个乙炔分子由四个原子构成。
(2)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过图2的_________
(选填“I”或“II”)装置,并再缓缓通入一段时间 的 N2,并记录实验数据于表中。
| 反应前质量/g | 反应后质量/g |
| 装置① | 125.3 | 127.1 |
| 装置② | 78.2 | 87.0 |
(3)实验中“缓缓通入一段时间 N2”的目的是___________。
(4)计算:乙炔中碳元素的质量为________g,氢元素 的质量为_______g,乙炔的化学式为_________。
(5)反应②的化学方程式___________。
-
以焦炭和碳酸钙为原料生产碳化钙( CaC2 ),并制备重要工业原料乙炔( C2 H2 )气体, 其工艺流程如下图:
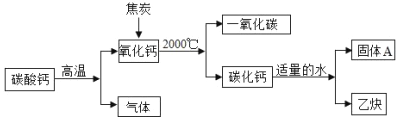
(1)写出碳酸钙分解的化学方程式_____。
(2)将氧化钙和焦炭反应的化学方程式补充完整, CaO + C CaC2 CO ;生成的 CO 不能排放到空气中,是因为_____。
(3)猜想:固体 A 的成分可能是氢氧化钙或碳酸钙。
设计实验证明猜想。
| 实验 | 现象 | 结论 |
| _____ | _____ | 固体A的成分不是碳酸钙 |
-
以焦炭和碳酸钙为原料生产碳化钙(CaC2),并制备重要工业原料乙炔(C2H2)气体,其工艺流程如图。
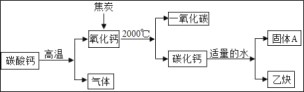
(1)写出碳酸钙分解的化学方程式_____。
(2)将氧化钙和焦炭反应的化学方程式补充完整:_____CaO+_____C _____CaC2+_____CO,生成的CO不能排放到空气中,是因为_____。
_____CaC2+_____CO,生成的CO不能排放到空气中,是因为_____。
(3)猜想:固体A的成分可能是紅氧化钙或碳酸钙。设计实验证明猜想。
| 实验 | 现象 | 结论 |
| _____。 | _____。 | 固体A的成分不是碳酸钙 |
并制备重要工业原料乙炔
流程如下:

.碳酸钙高温分解可得两种氧化物。
.乙炔的相对分子质量是26,一个乙炔分子有四个原子构成。
.B、C组成的元素相同,C有毒。
完全燃烧,生成
水和
二氧化碳,则乙炔的化学式为______。












