-
在一体积固定的密闭容器中,某化学反应2A(g)
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
实验
序号
时间
浓度
温度
0
10
20
30
40
50
60
1
800℃
1.0
0.80
0.67
0.57
0.50
0.50
0.50
2
800℃
c2
0.60
0.50
0.50
0.50
0.50
0.50
3
800℃
c3
0.92
0.75
0.63
0.60
0.60
0.60
4
820℃
1.0
0.40
0.25
0.20
0.20
0.20
0.20
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内,用A表示表示该反应的平均速率
为_______ mol/(L . min)
(2)在实验2,A的初始浓度c2=________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_______________________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3_______v1(填>、=、<),c3=________mol/L
(4)比较实验4和实验1,可推测该反应是________反应(选填吸热、放热)。
理由是___________________________________________________________
(5)根据以上实验请指出要加快该反应可采取什么样的方法(列举方法最少2种)
________________________________________________________
高二化学简答题困难题查看答案及解析
-
烟气中含有 SO2 等大量有害的物质,烟气除硫的方法有多种,其中石灰石法烟气除硫工艺的主要反应如下:
ⅠCaCO3(s)
CO2(g)+CaO (s) △H = + 178.2 kJ/mol
ⅡSO2(g)+CaO(s)
CaSO3(s) △H = - 402 kJ/mol
Ⅲ 2CaSO3(s) + O2 (g) + 4H2O(l)
2[CaSO4· 2H2O](s) △H = - 234.2 kJ/mol
(1)试写出由石灰石、二氧化硫、氧气和水反应生成生石膏的热化学方程式________________________________________________________
(2)反应Ⅱ为烟气除硫的关键,取相同用量的反应物在3种不同的容器中进行该反应,A容器保持恒温恒压,B容器保持恒温恒容,C容器保持恒容绝热,且初始时3个容器的容积和温度均相同,下列说法正确的是_______________
a.3个容器中SO2的平衡转化率的大小顺序为:αA > αB > αC
b.当A容器内气体的平均摩尔质量不变时,说明该反应处于化学平衡状态
c.A、B两个容器达到平衡所用的时间:tA > tB
d.当 C 容器内平衡常数不变时,说明该反应处于化学平衡状态
(3)依据上述反应Ⅱ来除硫,将一定量的烟气压缩到一个 20 L的容器中,测得不同温度下,容器内 SO2 的质量(mg)如下表:
时间/min
SO2质量/mg
温度/℃
0
20
40
60
80
100
120
T1
2100
1052
540
199
8.7
0.06
0.06
T2
2100
869
242
x
x
x
x
①在T1温度下,计算20~40min内SO2 的反应速率____________mol/(L· min)。
②若其它条件都相同,则T1______T2(填“>”、 “<” 或 “=”,下同); x _____ 0.06。
③在T2温度下,若平衡后将容器的容积压缩为10 L,则新平衡时SO2的浓度_____原平衡时SO2的浓度(填“>”、 “<” 或 “=”),理由是________________________________。
高二化学简答题困难题查看答案及解析
-
为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物的含量显得尤为重要。
I.氮氧化物研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g)
2NO2(g),下列各项能说明反应达到平衡状态的是 ________________(填字母代号) 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗1 molO2同时生成2 molNO2
(2)汽车内燃机工作时会引起N2和O2的反应:N2 +O2
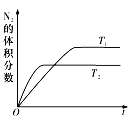
2NO,是导致汽车尾气中含有NO的原因之一。在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如右图所示,根据图像判断反应N2(g)+O2(g)
2NO(g)的△H__________0(填“>”或“<”)。
Ⅱ.碳氧化物研究
(1)体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如右图所示,现将3molH2和2molCO放入容器中,移动活塞至体积V为2L,用铆钉固定在A、B点,发生合成甲醇的反应如下:CO(g)+2H2(g)
CH3OH(g)。
测定不同条件、不同时间段内的CO的转化率,得到如下数据:
T(℃)
10min
20min
30min
40min
T1
20%
55%
65%
65%
T2
35%
50%
a1
a2
①根据上表数据,请比较T1_________T2(选填“>”、“<”或“=”);T2℃下,第30min 时,a1=________,该温度下的化学平衡常数为__________________。
②T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通入6molCO,此时v(正)________v(逆)(选填“>”、“<”或“=”)。
(2)一定条件下可用甲醇与CO反应生成醋酸消除CO污染。常温下,将a mol/L的醋酸与b mol/L Ba(OH)2溶液等体积混合(混合后溶液体积变化忽略不计),充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则根据溶液中的电荷平衡可知,溶液的pH=___________,则可以求出醋酸的电离常数Ka =____________ (用含a和b的代数式表示)。
高二化学简答题困难题查看答案及解析
-
航天员呼吸产生的CO2用下列反应处理,可实现空间站中O2的循环利用。
Sabatier反应:CO2(g)+4H2(g)
CH4(g)+2H2O(g)
水电解反应:2H2O(l)
2H2(g)+O2(g)
(1)将原料气按
∶
=1∶4置于密闭容器中发生Sabatier反应,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线)。
① 该反应的平衡常数K随温度升高而__________(填“增大”或“减小”)。

② 温度过高或过低均不利于该反应的进行,原因是________。
③ 200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算式为________。(不必化简。用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(2)Sabatier反应在空间站运行时,下列措施能提高CO2转化效率的是______(填标号)。
A.适当减压
B.增大催化剂的比表面积
C.反应器前段加热,后段冷却
D.提高原料气中CO2所占比例
E.合理控制反应器中气体的流速
(3)一种新的循环利用方案是用Bosch反应CO2(g)+2H2(g)
C(s)+2H2O(g)代替Sabatier反应。
① 已知CO2(g)、H2O(g)的生成焓分别为–394 kJ∙mol-1、–242 kJ∙mol-1,Bosch反应的ΔH =________kJ∙mol-1。(生成焓指一定条件下由对应单质生成1mol化合物时的反应热)
② 一定条件下Bosch反应必须在高温下才能启动,原因是________。
③ 新方案的优点是________。
高二化学简答题困难题查看答案及解析
-
氮及其化合物如NH3及铵盐、N2H4、N2O4等在中学化学、化工工业、国防等领域占有重要地位。
(1)发射航天火箭常用肼(N2H4)与N2O4作燃料与助燃剂。N2H4 (1)与N2O4(g)生成4 mol H2O(g)时放出热量1077 kJ,写出其热反应方程式:_____________________________________。
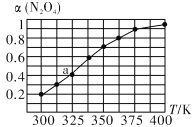
(2)N2O4与NO2之间存在反应N2O4(g)
2NO2 (g)将一定量的 N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度的变化如图所示。
①由图推测该反应ΔH_______0(填“>”或“<”),理由为__________________________。
②图中a点对应温度下,已知N2O4的起始压强p0为108 kPa,列式计算该温度下反应的平衡常数Kp =____________。(保留一位小数,并带单位。用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
③在一定条件下,该反应N2O4、NO2两者的消耗速率与自身压强间存在关系:v消耗(N2O4)=k1· P(N2O4),v消耗(NO2)=k2·P2(NO2),其中k1、k2是与反应温度有关的速率常数。则一定温度下,k1、k2与平衡常数Kp的关系是k1=________________。
高二化学简答题困难题查看答案及解析
-
钛的化合物如TiO2、Ti(NO3)4、TiCl4、 Ti(BH4)2等均有着广泛用途。
(1)写出Ti的基态原子的外围电子排布式____________。
(2)TiCl4熔点是-25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于_____晶体;BH4-中B原子的杂化类型为____________;
(3)在 TiO2催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO-互为等电子体的分子化学式为_________________。
(4)Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色),[TiCl(H2O)5]Cl2•H2O(绿色),两者配位数_____(填“相同”或“不同”),绿色晶体中配体是______。
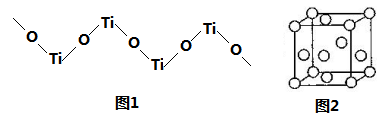
(5)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为____________。
(6)金属钛内部原子的堆积方式是面心立方堆积方式,如图2。若该晶胞的密度为
g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。
高二化学简答题困难题查看答案及解析
-
I下图表示一些晶体中的某些结构,他们分别是氯化钠、氯化铯、干冰、金刚石、石墨结构中的某一种的某一部分(黑点可表示不同或相同的粒子)。
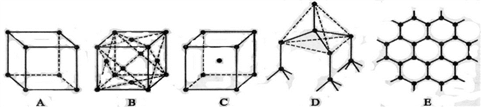
(1)其中代表金刚石的是_______(填编号字母,下同),金刚石中每个碳原子与_____个碳原子最接近且距离相等。
(2)其中代表石墨的是________,其中每个正六边形占有的碳原子数平均为________个;
(3)其中表示氯化钠的是___,每个钠离子周围与它最接近且距离相等的钠离子有___个;
(4)代表氯化铯的是______,每个铯离子与______个氯离子紧邻;
(5)代表干冰的是_______,每个二氧化碳分子与________个二氧化碳分子紧邻;
II将少量CuSO4粉末溶于盛有水的试管中得到一种天蓝色溶液,先向试管里的溶液中滴加氨水,首先形成蓝色沉淀。继续滴加氨水,沉淀溶解,得到深蓝色溶液;再加入乙醇溶剂,将析出深蓝色的晶体。
(1)溶液中呈天蓝色微粒的化学式是______,1 mol该天蓝色微粒所含的σ键数目为______。
(2)加入乙醇的作用是_____________________。
(3)写出蓝色沉淀溶解成深蓝色溶液的离子方程式______________。
(4)得到的深蓝色晶体是[Cu(NH3)4]SO4·H2O,晶体中Cu2+与NH3之间的化学键类型为_____, 该晶体中配体分子的空间构型为_________。(用文字描述)
高二化学简答题困难题查看答案及解析
-
砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________。
(2)根据元素周期律,原子半径Ga____As,第一电离能Ga______As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________ ,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_________。
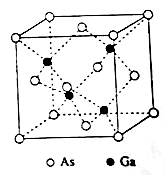
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________,
Ga与As以________键合。Ga和As的摩尔质量分别为MGa g·mol-1 和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为__________。
高二化学简答题困难题查看答案及解析
-
丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+
O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+
O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
反应①的ΔH1为________ kJ·mol-1。图(a)是反应①平衡转化率与反应温度及压强的关系图,x_____________0.1(填“大于”或“小于”);欲使丁烯的平衡产率提高,应采取的措施是__________(填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
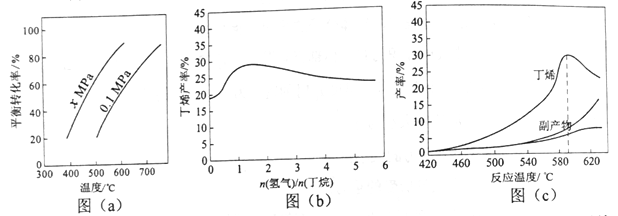
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是___________。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590 ℃之前随温度升高而增大的原因可能是___________、____________;590℃之后,丁烯产率快速降低的主要原因可能是_____________。
高二化学简答题困难题查看答案及解析
-
1 L某混合溶液,可能含有的离子如表所示:
可能大量含有的阳离子
H+、K+、Mg2+、Al3+、NH
、Fe2+、Fe3+
可能大量含有的阴离子
Cl-、Br-、I-、CO
、AlO
(1)往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。
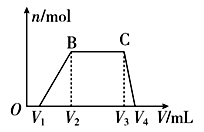
则该溶液中一定不含有的离子是________________________。
(2)BC段离子方程式为_______________________。
(3)V1、V2、V3、V4之间的关系为____________________。
(4)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
Cl2的体积(标准状况)
2.8 L
5.6 L
11.2 L
n(Cl-)
1.25 mol
1.5 mol
2 mol
n(Br-)
1.5 mol
1.4 mol
0.9 mol
n(I-)
a mol
0
0
①当通入Cl2的体积为2.8 L时,溶液中发生反应的离子方程式为________________。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为________。
高二化学简答题困难题查看答案及解析