氰氨化钙(CaCN2)是一种重要的化工原料,制备CaCN2的化学方程式为+
===
+
↑+
↑+
↑,该反应中下列说法正确的是( )
A. 可用氢氧化钠溶液处理有害的气体产物 B. 反应后气体质量减少
C. X的化学式为HCNO D. X溶液的pH<7
九年级化学单选题中等难度题
氰氨化钙(CaCN2)是一种重要的化工原料,制备CaCN2的化学方程式为+
===
+
↑+
↑+
↑,该反应中下列说法正确的是( )
A. 可用氢氧化钠溶液处理有害的气体产物 B. 反应后气体质量减少
C. X的化学式为HCNO D. X溶液的pH<7
九年级化学单选题中等难度题
氰氨化钙(CaCN2)是一种重要的化工原料,制备CaCN2的化学方程式为+
===
+
↑+
↑+
↑,该反应中下列说法正确的是( )
A. 可用氢氧化钠溶液处理有害的气体产物 B. 反应后气体质量减少
C. X的化学式为HCNO D. X溶液的pH<7
九年级化学单选题中等难度题查看答案及解析
氰氨化钙(CaCN2)是一种重要的化工原料,制备CaCN2的化学方程式为+
===
+
↑+
↑+
↑,该反应中下列说法正确的是( )
A. 可用氢氧化钠溶液处理有害的气体产物 B. 反应后气体质量减少
C. X的化学式为HCNO D. X溶液的pH<7
九年级化学单选题中等难度题查看答案及解析
氰氨基化钙(CaCN2)是一种重要的化工原料,制备CaCN2的化学方程式为CaCO3+2X=CaCN2+CO↑+H2↑+CO2↑.该反应中下列说法正确的是( )
A. 可用氢氧化钠溶液处理有害的气体产物 B. 反应后气体质量减少
C. X的化学式为HCNO D. X溶液的
九年级化学单选题中等难度题查看答案及解析
高纯氧化钙是用于电子工业的重要无机化工原料,用生石灰(主要成分为CaO)制备高纯氧化钙的工艺流程如下:
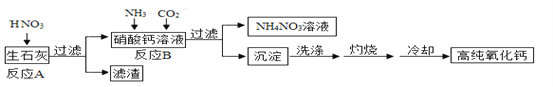
请回答下列问题:
(1)过滤操作中玻璃棒的作用是_______________;
(2) 反应B的化学方程式为________________________;
(3)灼烧时发生反应的化学方程式为_________, 该工艺流程中可循环使用的物质是 _________;
(4)冷却需在密闭和干燥的环境中进行,否则制得的高纯氧化钙中会混有的两种杂质名称分别 是 ___________ 和__________ 。
九年级化学流程题困难题查看答案及解析
高纯氧化钙是用于电子工业的重要无机化工原料,用生石灰(主要成分为CaO)制备高纯氧化钙的工艺流程如下:
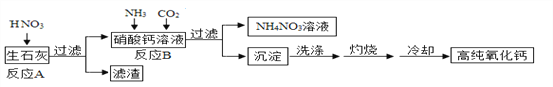
请回答下列问题:
(1)过滤操作中玻璃棒的作用是_______________;
(2) 反应B的化学方程式为________________________;
(3)灼烧时发生反应的化学方程式为_________, 该工艺流程中可循环使用的物质是 _________;
(4)冷却需在密闭和干燥的环境中进行,否则制得的高纯氧化钙中会混有的两种杂质名称分别 是 ___________ 和__________ 。
九年级化学流程题困难题查看答案及解析
电石,学名碳化钙(CaC2),以焦炭和碳酸钙为原料生产碳化钙并制备重要工业原料乙炔(CxHy)气体的原理如下图。
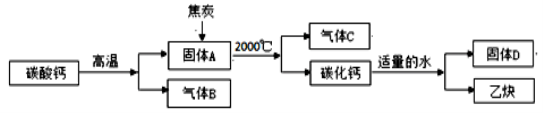
【实验探究】
(1)气体C有毒,写出固体A和焦炭反应得到碳化钙的化学方程式为 。
(2)小组同学对固体D提出三种猜想:
猜想一:氧化钙;
猜想二:氢氧化钙;
猜想三:碳酸钙。
同学们经过分析将猜想一排除了,理由是 。
(3)检验固体D:取样,滴加足量的稀盐酸,观察到 ,猜想二正确。
【组成测定】
(一)实验设计:
将一定量的乙炔(CxHy)在足量的氧气中完全燃烧,生成的气体全部缓缓通过下图
装置(选填“Ⅰ”或“Ⅱ”)。
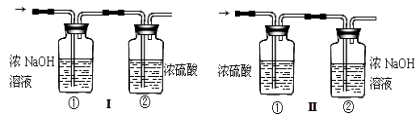
(二)实验测定:(小资料:乙炔的相对分子质量为26)
实验数据记录于下表中,试通过计算,确定乙炔的化学式。
| 反应前质量/g | 反应后质量/g | |
| 装置① | 125.3 | 127.1 |
| 装置② | 78.2 | 87.0 |
结论:乙炔的化学式 。
【归纳小结】写出碳化钙与水反应的化学方程式: 。
九年级化学探究题困难题查看答案及解析
电石,学名碳化钙(CaC2),以焦炭和碳酸钙为原料生产碳化钙并制备重要工业原料乙炔(CxHy)气体的原理如下图。
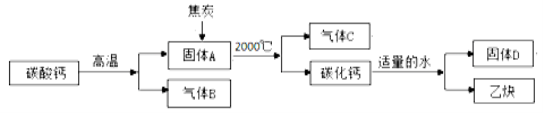
【实验探究】
(1)气体C有毒,写出固体A和焦炭反应得到碳化钙的化学方程式为 。
(2)小组同学对固体D提出三种猜想:
猜想一:氧化钙;
猜想二:氢氧化钙;
猜想三:碳酸钙。
同学们经过分析将猜想一排除了,理由是 。
(3)检验固体D:取样,滴加足量的稀盐酸,观察到 ,猜想二正确。
【组成测定】
(一)实验设计:
将一定量的乙炔(CxHy)在足量的氧气中完全燃烧,生成的气体全部缓缓通过下图
装置(选填“Ⅰ”或“Ⅱ”)。
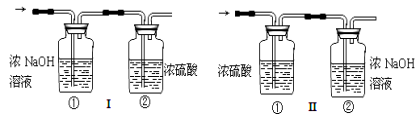
(二)实验测定:(小资料:乙炔的相对分子质量为26)
实验数据记录于下表中,试通过计算,确定乙炔的化学式。
| 反应前质量/g | 反应后质量/g | |
| 装置① | 125.3 | 127.1 |
| 装置② | 78.2 | 87.0 |
结论:乙炔的化学式 。
【归纳小结】写出碳化钙与水反应的化学方程式: 。
九年级化学实验题困难题查看答案及解析
以焦炭和碳酸钙为原料生产碳化钙( CaC2 ),并制备重要工业原料乙炔( C2 H2 )气体, 其工艺流程如下图:
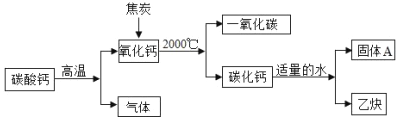
(1)写出碳酸钙分解的化学方程式_____。
(2)将氧化钙和焦炭反应的化学方程式补充完整, CaO + C CaC2 CO ;生成的 CO 不能排放到空气中,是因为_____。
(3)猜想:固体 A 的成分可能是氢氧化钙或碳酸钙。
设计实验证明猜想。
| 实验 | 现象 | 结论 |
| _____ | _____ | 固体A的成分不是碳酸钙 |
九年级化学流程题中等难度题查看答案及解析
高纯氧化钙是用于电子工业重要的无机化工原料。用硝酸钙溶液制备高纯氧化钙的工艺流程如下,已知:反应池中发生反应的化学方程式为:CO2+2NH3•H2O+Ca(NO3)2═2NH4NO3+X↓+H2O(该流程中硝酸钙完全反应)
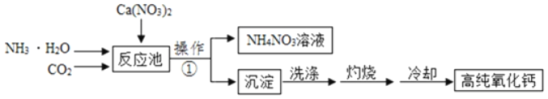
请回答下列问题:
(1)操作①需要用到的玻璃仪器有烧杯、_____、玻璃棒,其中玻璃棒的作用是_____。
(2)该工艺流程中可循环使用的物质是_____。
(3)灼烧过程中,发生的反应的化学方程式为_____。
(4)冷却需在干燥的环境中进行,否则制得的高纯氧化钙中会混有的杂质是_____(填化学式),原因是_____(用化学方程式表示)。
九年级化学流程题中等难度题查看答案及解析

九年级化学解答题中等难度题查看答案及解析