-
为确定试样xNa2CO3·yNaHCO3的组成,某同学将质量为a g的试样加水溶解后,所得试样溶液进行如下实验:

注:NaHCO3溶液pH约为8.3,饱和H2CO3溶液pH约为4.0。
下列说法正确的是
A. 当pH=8.3时,溶液中只存在Na+、H+、HCO3-、Cl-、OH-
B. 溶液pH由8.3变为4.0过程中,发生反应:CO32- +2H+ =CO2↑+H2O
C. 若V2=2V1,则x=y
D. 试样中,NaHCO3的质量分数=[(8.4×10-3V2)/a]×100%
-
为了测定含有H2C2O4·2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0 g试样,加水溶解,配成250 mL试样溶液。
②用酸式滴定管量取25.00 mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500 mol/L NaOH溶液滴定,消耗NaOH溶液20.00 mL。
③再取25.00 mL试样溶液放入另一锥形瓶中,用0.1000 mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00 mL。
回答下列问题:
(1)已知:0.10mol/LKHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺为 。
(2)步骤①所需要的玻璃仪器有烧杯、玻璃棒、 。
(3) 完成并配平下列离子方程式:
C2O42- + MnO4—+ H+ = CO2↑+ Mn2+ +
(4)步骤③中判断滴定终点的方法是 。
(5)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4·2H2O的质量分数 。(填“偏大”、“偏小”或“无影响”)
(6)试样中H2C2O4·2H2O的质量分数为 。
-
为了测定含有H2C2O4·2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0 g试样,加水溶解,配成250 mL试样溶液。
②用酸式滴定管量取25.00 mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500 mol/L NaOH溶液滴定,消耗NaOH溶液20.00 mL。
③再取25.00 mL试样溶液放入另一锥形瓶中,用0.1000 mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00 mL。
回答下列问题:
(1)已知:0.10mol/LKHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺为_________________。
(2)步骤①所需要的玻璃仪器有烧杯、玻璃棒、_____________________________。
(3) 完成并配平下列离子方程式:
____C2O42- +____MnO4—+____H+ =_____CO2↑+____Mn2+ +________________
(4)步骤③中判断滴定终点的方法是_______________________________________。
(5)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4·2H2O的质量分数___________。(填“偏大”、“偏小”或“无影响”)
(6)试样中H2C2O4·2H2O的质量分数为_____________。
-
为了测定含有H2C2O4·2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0 g试样,加水溶解,配成250 mL试样溶液。
②用酸式滴定管量取25.00 mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500 mol/L NaOH溶液滴定,消耗NaOH溶液20.00 mL。
③再取25.00 mL试样溶液放入另一锥形瓶中,用0.1000 mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00 mL。
回答下列问题:
(1)已知:0.10 mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为________。
(2)步骤①所需要的玻璃仪器有烧杯、玻璃棒、________。
(3)完成并配平下列离子方程式:________C2O42-+________MnO4-+________H+=________CO2+________Mn2++________ ________
(4)滴定时边滴边摇动锥形瓶,眼睛应观察。
(5)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4·2H2O的质量分数________。(填“偏大”、“偏小”或“无影响”)
(6)步骤③中判断滴定终点的方法是________。
(7)试样中H2C2O4·2H2O的质量分数为。
-
为了测定含有H2C2O4·2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0g试样,加水溶解,配成250mL试样溶液。
②用酸式滴定管量取25.00mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500mol/LNaOH溶液滴定,消耗NaOH溶液20.00mL。
③再取25.00 mL试样溶液放入另一锥形瓶中,用0.1000mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL。
回答下列问题:
(1)已知:0.10 mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为 。
(2)步骤①所需要的玻璃仪器有烧杯、玻璃棒、 。
(3)完成并配平下列离子方程式: C2O42-+ MnO4-+ H+= CO2↑+ Mn2++
(4)步骤③中判断滴定终点的方法是 。
(5)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4·2H2O的质量分数 。(填“偏大”、“偏小”或“无影响”)
(6)试样中H2C2O4·2H2O的质量分数为 。
-
某天然碱组成可表示为xNa2CO3·yNaHCO3·zH2O。取m g该天然碱配成1L溶液M。取出100mLM向其中加入50mL1 mol·L-1盐酸,两者恰好完全反应生成NaCl,同时产生CO2的体积为672mL(标准状况下),下列推断正确的是( )
A. m g该天然碱中含0.3molNa2CO3 B. m g该天然碱中含0.3molNa+
C. 溶液M中c(Na+)=0.5 mol·L-1 D. 该天然碱中x:y:z=2:1:2
-
已知H2C2O4为二元中强酸。某化学兴趣小组为测定含Na2SO4、NaHC2O4和H2C2O4·2H2O的试样中各物质的质量分数,进行了如下实验:
①称取10.0 g试样,加水溶解,配成250 mL试样溶液
②用酸式滴定管分别量取25.00 mL试样溶液两份于锥形瓶中
③第一份溶液中加2~3滴指示剂,用0.2500 mol·L-1NaOH溶液滴定,消耗NaOH溶液20.00 mL
④第二份溶液用0.1000 mol·L-1的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00 mL
回答下列问题:
(1)写出NaHC2O4溶液与NaOH溶液反应的离子方程式 。
(2)步骤①配制试样溶液时所需要的玻璃仪器有烧杯、玻璃棒、量筒、 。
(3)步骤③若滴定终点时溶液的pH=8.3,则选择的指示剂为 。若用某部分刻度模糊不清的50mL滴定管进行实验,当滴定管中的液面处于如图所示的刻度处,则管内液体的体积 (填代号) 。

a.等于23.60mL b.等于27.60mL c.小于23.60mL d.大于27.60mL
(4)滴定时边滴边摇动锥形瓶,眼睛应观察 。
(5)完成并配平下列离子方程式:

(6)步骤③中,高锰酸钾溶液应装在 滴定管里;该步判断滴定终点的方法是 。
(7)试样中Na2SO4的质量分数为 (保留3位有效数字)。
-
已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
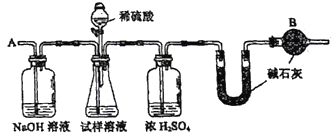
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到bg
④从分液漏斗滴入6mol/L的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到cg
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为dg
请回容以下问题:
(1)装置中干燥管B的作用是____________。
(2)如果将分浓漏斗中的硫酸换成浓度相同的盐酸,测试的结果______(填偏高、偏低或不变);
(3)步骤⑤的目的是______________。
(4)步骤⑦的目的是___________________。
(5)该试样中纯碱的质量分数的计算式为________________。
-
粉末状试样A是由 和Fe2O3组成的混合物。进行如下实验:
和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取 全部溶于
全部溶于 盐酸中,固体全部溶解,得溶液C;
盐酸中,固体全部溶解,得溶液C;
③将①中得到的单质B和溶液C反应,放出 (标况)气体。同时生成溶液D,还残留有固体物质B;
(标况)气体。同时生成溶液D,还残留有固体物质B;
④用 溶液检查时,溶液D不变色。
溶液检查时,溶液D不变色。
请填空:
(1)①中引发铝热反应的实验操作是____________,产物中的单质B是___________________。
(2)②中所发生反应的化学方程式是____________、____________。
(3)③中所发生反应的离子方程式是____________、____________。
(4)若溶液D的体积仍视为 ,则该溶液中
,则该溶液中 为____________,
为____________, 为____________。
为____________。
-
下列根据实验操作和现象得出的结论正确的是
| 实验操作 | 实验现象 | 结论 |
| A | 将少量Fe(NO3)2试样加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成血红色 | Fe(NO3)2试样已变质 |
| B | 向甲苯中滴加少量酸性髙锰酸钾溶液 | 高锰酸钾溶液褪色 | 甲苯发生了氧化反应 |
| C | 常温下分别测定浓度均为0.1mol/L的Na2SiO3溶液和Na2CO3溶液的pH | pH:Na2SiO3>Na2CO3 | 非金属性:Si>C |
| D | 将少量某无色气体通入澄清石灰水中 | 出现白色沉淀 | 该气体一定是CO2 |
A. A B. B C. C D. D



