-
摩尔盐的成分为(NH4)2Fe(SO4)2·6H2O(M=392g·mol-1),常作氧化还原滴定剂。学校购买了一批摩尔盐样品(假设杂质不参与反应),某学习小组拟设计实验方案测定其纯度:
方案1:沉淀法。甲同学准确称量一定质量样品溶于适量的蒸馏水,滴加适量BaCl2溶液至S042-完全沉淀,经过滤、洗涤、干燥,称得BaSO4质量。
(1)检验SO42-是否完全沉淀的操作是____________________________________________。
方案2:滴定法。乙同学准确称取mg摩尔盐样品溶于蒸馏水配制成250mL溶液,量取25.00mL所配制溶液于锥形瓶中,滴加适量的稀硫酸,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液的体积为VmL。
(2)用KMnO4溶液滴定时应选用___(填“酸式”或“碱式”)滴定管,写出滴定反应的离子方程式:_________。
(3)该样品的纯度为_________________________________。
(4)若用待测液润洗锥形瓶,测得结果___________(填“偏高”“偏低”或“无影响”)。
方案3:量气法。丙同学准确称量4.0g样品按下图所示装置进行实验。

(5)①橡胶管L的作用是______________________。
②B中液体可以是___________(填字母)。
a.饱和食盐水 b四氯化碳 c.煤油 d饱和氯化铵溶液
③当A中样品完全反应后,待装置冷却至室温,测得NH3的体积为448mL(已折合成标准状况)。根据上述数据计算,该产品的纯度为____________。
-
已知硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]俗称莫尔盐,其摩尔质量为392 g/mol,可溶于水,在100℃~ 110 ℃时分解。为探究其化学组成,甲乙两同学设计了如下实验。
Ⅰ.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如下图所示的装置进行实验,装置C中可观察到的现象是溶液变红,由此可知分解产物中有_____________。
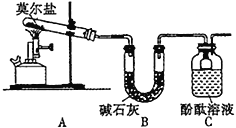
(2)乙同学认为莫尔盐晶体分解的产物中还含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验:
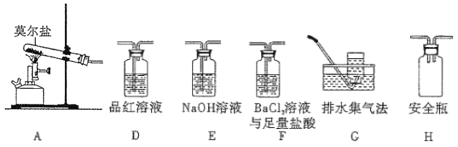
①乙组同学的实验中,装置依次连接的合理顺序为A→H→__________________________→G
②证明含有SO3的实验现象是_______________。
II.为测硫酸亚铁铵纯度,称取m g 莫尔盐样品,配成500 mL溶液。甲、乙两同学设计了如下两个实验方案。
甲方案:取25.00mL硫酸亚铁铵溶液用0.1000mol•L-1的酸性K2Cr2O7溶液分三次进行滴定。
乙方案:(通过NH4+测定)设计装置如下图所示。取25.00 mL样品溶液进行该实验。
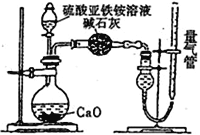
(1)滴定过程中,酸性K2Cr2O7溶液应装在_____________滴定管中。甲方案中的离子方程式为_________________________________。
(2)乙方案中量气管中最佳试剂是______(填字母)。
a.水 b.饱和NaHCO3溶液 c.CC14
(3)乙方案中收集完气体并恢复至室温,读数前应进行的操作是______________________________。
(4)若测得NH3(已折算为标准状况下)为VL,则硫酸亚铁铵纯度为___________。(用含V、m的式子表示)
-
已知硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]俗称莫尔盐,其摩尔质量为392 g/mol,可溶于水,在100℃~ 110 ℃时分解。为探究其化学组成,甲乙两同学设计了如下实验。
Ⅰ.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如下图所示的装置进行实验,装置C中可观察到的现象是溶液变红,由此可知分解产物中有_____________。
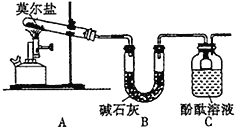
(2)乙同学认为莫尔盐晶体分解的产物中还含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验:
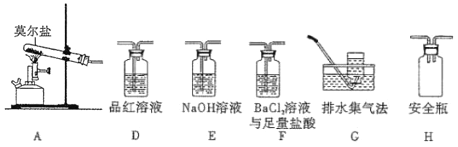
①乙组同学的实验中,装置依次连接的合理顺序为A→H→__________________________→G
②证明含有SO3的实验现象是_______________。
II.为测硫酸亚铁铵纯度,称取m g 莫尔盐样品,配成500 mL溶液。甲、乙两同学设计了如下两个实验方案。
甲方案:取25.00mL硫酸亚铁铵溶液用0.1000mol•L-1的酸性K2Cr2O7溶液分三次进行滴定。
乙方案:(通过NH4+测定)设计装置如下图所示。取25.00 mL样品溶液进行该实验。
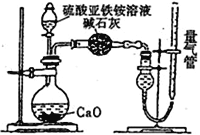
(1)滴定过程中,酸性K2Cr2O7溶液应装在_____________滴定管中。甲方案中的离子方程式为_________________________________。
(2)乙方案中量气管中最佳试剂是______(填字母)。
a.水 b.饱和NaHCO3溶液 c.CC14
(3)乙方案中收集完气体并恢复至室温,读数前应进行的操作是______________________________。
(4)若测得NH3(已折算为标准状况下)为VL,则硫酸亚铁铵纯度为___________。(用含V、m的式子表示)
-
(4分)某种盐可表示为[xFeSO4·y(NH4)2SO4·6H2O](其摩尔质量为392g·mol-1),可用作标定重铬酸钾、高锰酸钾等溶液的标准物质,也可用于冶金、电镀。为测定其组成,进行下列实验:
①取一定质量的上述盐样品,准确配制100mL的溶液X;
②量取20.00mL的溶液X,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,烘干至恒重,得到白色固体Y 4.660g
③另取20.00mL的X溶液,滴加适量硫酸,用0.1000mol·L-1的KMnO4溶液滴定至终点,生成Mn2+,消耗KMnO4溶液20.00mL。
(1)在20.00mL试样溶液中c(SO42-)= mol·L-1,n(Fe2+)= mol;
(2)该盐的化学式为 。
-
某种盐可表示为[xFeSO4·y(NH4)2SO4·6H2O](其摩尔质量为392g·mol-1),可用作标定重铬酸钾、高锰酸钾等溶液的标准物质,也可用于冶金、电镀。为测定其组成,进行下列实验:
①取一定质量的上述盐样品,准确配制100mL的溶液X;
②量取20.00mL的溶液X,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,烘干至恒重,得到白色固体Y 4.660g
③另取20.00mL的X溶液,滴加适量硫酸,用0.1000mol·L-1的KMnO4溶液滴定至终点,生成Mn2+,消耗KMnO4溶液20.00mL。
(1)在20.00mL试样溶液中c(SO42-)= mol·L-1,n(Fe2+)= mol;
(2)该盐的化学式为 。
-
莫尔盐[(NH4)2Fe(SO4)2·6H2O]常作氧化还原滴定法的基准物质,在0.1mol/L的该盐的溶液中,下列有关比较不正确的是( )
A.c(SO )> c(NH
)> c(NH )>c(Fe2+)>c(H+)>c(OH-)
)>c(Fe2+)>c(H+)>c(OH-)
B.c(NH3·H2O)+c(NH )= 0.2mol/L
)= 0.2mol/L
C.2c(SO )+ c(OH-)= c(NH
)+ c(OH-)= c(NH )+2 c(Fe2+)+c(H+)
)+2 c(Fe2+)+c(H+)
D.c(H+)= c(OH-)+c(NH3·H2O)
-
硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]是一种稳定的还原剂,常用作分析化学中的滴定剂。某课题组采用下列方案制备该晶体,并对其热稳定性进行了如下实验。
Ⅰ.硫酸亚铁铵晶体的制备:
铁粉 FeSO4溶液
FeSO4溶液 结晶
结晶 硫酸亚铁铵晶体
硫酸亚铁铵晶体
(1)硫酸浓度过大,反应过快同时会使FeSO4溶液中混有_____________(填离子符号)。
(2)利用FeSO4溶液与(NH4)2SO4晶体制备该晶体的化学方程式_____________。
Ⅱ.硫酸亚铁铵晶体的热分解产物探究:该小组同学选用如图所示部分装置进行实验(夹持装备略)。查阅资料:隔绝空气加热至500℃硫酸亚铁铵能完全分解,产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
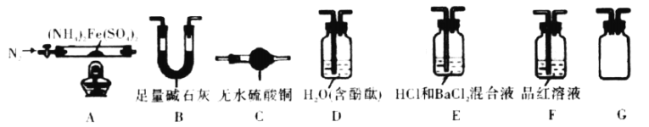
(3)点燃A处的酒精灯之前,先打开弹簧夹,通一段时间N2,其目的是____________。
(4)选用上述部分必要的装置完成下列相应实验,填写横线上的内容。
| 检验可能产物 | 装置连接顺序 | 装置作用 | 实验现象 | 实验结论 |
| H2O、NH3 | ACBGD | ①B的作用______ | ②C中________; D中__________。 | 有H2O、NH3 |
| SO2、SO3 | ③___________ | ④E中HCl的作用 ___________ | E中没有明显现象,F中溶液褪色 | ⑤___________ |
(5)为证明热分解完全后残留的固体仅为Fe2O3,而不含FeO或Fe3O4,需要选用的试剂有__________(选下列字母);简述利用所选试剂进行实验证明的方案____________。
A.稀硫酸 B.稀硝酸 C.KSCN溶液 D.H2O2溶液 E.K3[Fe(CN)6]溶液
-
莫尔盐[(NH4)2Fe(SO4)2·6H2O]溶液经常用于定量滴定实验。下列有关说法正确的是 ( )
A. 配制0.1mol•L-1莫尔盐溶液500mL,需莫尔盐19.6克
B. 可与含Fe2+、HClO、H+、Cl-微粒的溶液大量共存
C. 加入过量Ba(OH)2溶液发生反应:2Ba2++2SO42-+Fe2++2OH-=2BaSO4↓+Fe(OH)2↓
D. 取样,加入浓NaOH溶液并加热,出现可让蓝色石蕊试纸变红的气体,证明含NH4+
-
莫尔盐[(NH4)2Fe(SO4)2•6H2O]溶液经常用于定量滴定实验,下列有关说法正确的是
A.配制0.1mol·L-1莫尔盐溶液500mL,需莫尔盐19.6克
B.可与含Fe2+、HClO、H+、Cl﹣微粒的溶液大量共存
C.加入过量Ba(OH)2溶液发生反应:2Ba2++2SO42﹣+Fe2++2OH﹣=2BaSO4↓+Fe(OH)2↓
D.取样,加入浓NaOH溶液并加热,出现可让蓝色石蕊试纸变红的气体,证明含NH4+
-
CuAlO2是重要化工品,(NH4)2Fe(SO4)2·6H2O(摩尔盐)是化学上常用的分析试剂。某小组以黄铜矿(主要成分是CuFeS2,含少量SiO2)为原料制备这两种化工品,流程如图:
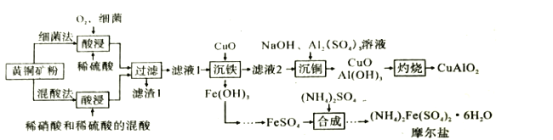
已知:①几种氢氧化物的开始沉淀和完全沉淀的pH,如表所示。
| Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀/pH | 4.7 | 7.6 | 2.7 |
| 完全沉淀/pH | 6.7 | 9.6 | 3.7 |
②4CuO+4Al(OH)3 4CuAlO2+6H2O+O2↑
4CuAlO2+6H2O+O2↑
回答下列问题:
(1)CuAlO2中铜的化合价为__;滤渣1的主要成分是__(填化学式)。
(2)反应物中铁元素被氧化的目的是__。
(3)提高这两种方案中“酸浸”反应速率都需要加热,但温度都不宜过高,其原因是__。
(4)在混酸法中,CuFeS2溶于混酸生成Cu2+,Fe3+,SO42-和一种无色气体,该气体遇空气迅速变为红棕色。写出CuFeS2与混酸反应的离子方程式__。
(5)评价上述流程,补充完整:
| 优点 | 缺点 |
| 细菌法 | ①__ | 化学反应慢,需要时间长 |
| 混酸法 | 节省时间 | ②___ |








