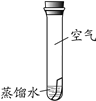-
实验室里久置的铜制燃烧匙表面生锈了,同学们展开如下探究活动。
[查阅资料]铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3]
[提出问题]铜锈蚀的条件有哪些?
[提出猜想]猜想一:铜生锈可能需要接触水;
猜想二:铜生锈可能需要接触氧气;
猜想三:铜生锈可能需要接触氮气;
猜想四:铜生锈可能还需要接触_____。
[讨论交流]依据化学反应前后元素种类守恒的思想,可知猜想_____是错误的。
[设计实验]将铜片用砂纸打磨光亮,分别置于如下图所示的试管中。一个月后,发现A、B、C三支试管里的铜片都未生锈,D试管里的铜片生锈了。

[实验分析](1)通过A组和D组实验的对比,可以得出铜生锈需要铜与_____接触;
(2)通过_____实验的对比,可以得出铜生锈需要铜与氧气接触;
(3)通过_____实验的对比,可以得出铜生锈需要铜与_____接触;
[实验结论]铜生锈需要铜同时接触_____。
-
小丽同学发现自己的铜制镜框表面出现了绿色的“铜锈”,利用兴趣小组活动的时间,小丽和几位同学对铜锈产生的条件进行探究.
(提出问题)铜生锈的条件是什么?
(查阅资料)铜锈的主要成分是Cu2(OH)2CO3(俗称铜绿)。
(作出猜想)铜生锈的条件是铜与H2O、CO2接触。
(进行实验)将4小块铜片(长度和宽度相同)按下图装置所示放置一个月,结果如下:
| 编号 | ① | ② | ③ | ④ |
| 实验 | 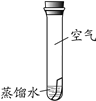
| 
| 
| 
|
| 现象 | 铜片表面有绿色物质 | 无明显现象 | 无明显现象 | 无明显现象 |
(得出结论)铜生锈的条件是与H2O、CO2接触。。
回答问题:
(1)铜绿由_____种元素组成。
(2)小组同学作出“铜生锈的条件是铜与H2O、CO2接触”这一猜想,其理由是_____。
(3)对比实验①③得到的结论是_____。
(4)能说明铜生锈与H2O有关的实验是_____。
(5)经过反思,小刚同学对所得结论提出疑议:与氧气接触也可能是铜生锈的条件之一。小丽同学认为实验①、④对比即可说明铜生锈与氧气有关。请判断小丽的说法是否正确并说明理由_____。
(6)通过实验证明,铜生锈的条件是铜与氧气、水、二氧化碳接触。由此,你对保存铜制品的建议是_____。
-
(8分)生活中常遇见铜制品生锈的情况。活动课上,同学们设计实验对铜锈进行了如下探究活动。
探究活动一:验证铜锈的组成
【查阅资料】
① 铜锈为绿色,其主要成分是Cu2(OH)2CO3。
② 白色的硫酸铜粉末遇水能变为蓝色。
③ 碳不与稀硫酸反应。
④ 氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液。
【进行实验1】
同学们设计了下图所示装置并进行实验。

| 实验操作 | 实验现象 | 实验结论 |
| ① 按上图组装仪器,装入药品。 ② 加热铜锈,直至不再有气体产生,停止加热。 | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊。 | 加热铜锈生成的物质有_____;铜锈由_____元素组成;烧杯中发生反应的化学方程式为______。 |
| ③ 冷却后,向试管中固体加入适量稀硫酸,稍加热。 | 黑色固体溶解,溶液变为蓝色。 |
探究活动二:探究铜生锈的条件
【进行实验2】
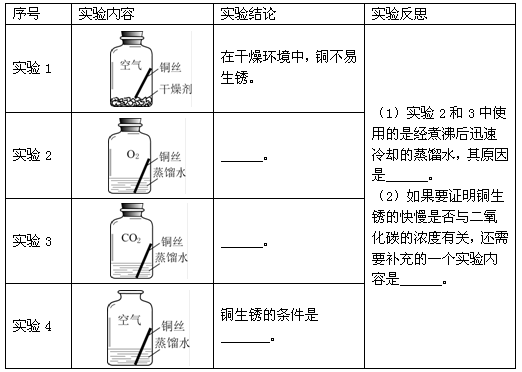
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显。
-
生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.
探究活动一:验证铜锈的组成
(查阅资料)
①铜锈为绿色,其主要成分是Cu2(OH)2CO3.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应.
④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
(进行实验1)
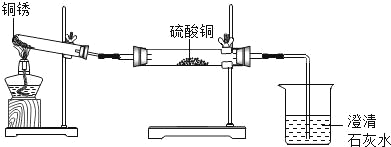
同学们设计了如图所示装置并进行实验.
| 
实验操作 | 实验现象 | 实验结论 |
| ①按上图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有__;铜锈由___元素组成;烧杯中发生反应的化学方程式为___. |
| ③冷却后,向试管中固体加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变为蓝色. |
探究活动二:探究铜生锈的条件
(进行实验2)
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 
| 在干燥环境中,铜不易生锈. | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是___. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是___. |
| 实验2 | 
| ___. |
| 实验3 | 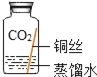
| ___. |
| 实验4 | 
| 铜生锈的条件是___. |
-
生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.
探究活动一:验证铜锈的组成
(查阅资料)
①铜锈为绿色,其主要成分是Cu2(OH)2CO3.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应.
④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
(进行实验1)
同学们设计了如图所示装置并进行实验.
| 
实验操作 | 实验现象 | 实验结论 |
| ①按上图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有__;铜锈由___元素组成;烧杯中发生反应的化学方程式为___. |
| ③冷却后,向试管中固体加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变为蓝色. |
探究活动二:探究铜生锈的条件
(进行实验2)
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 
| 在干燥环境中,铜不易生锈. | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是___. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是___. |
| 实验2 | 
| ___. |
| 实验3 | 
| ___. |
| 实验4 | 
| 铜生锈的条件是___. |
-
生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.
探究活动一:验证铜锈的组成
(查阅资料)
①铜锈为绿色,其主要成分是Cu2(OH)2CO3.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应.
④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
(进行实验1)
同学们设计了如图所示装置并进行实验.
| 
实验操作 | 实验现象 | 实验结论 |
| ①按上图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有__;铜锈由___元素组成;烧杯中发生反应的化学方程式为___. |
| ③冷却后,向试管中固体加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变为蓝色. |
探究活动二:探究铜生锈的条件
(进行实验2)
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 
| 在干燥环境中,铜不易生锈. | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是___. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是___. |
| 实验2 | 
| ___. |
| 实验3 | 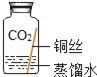
| ___. |
| 实验4 | 
| 铜生锈的条件是___. |
-
小花同学发现自己的铜制眼镜框表面出现了绿色的铜锈。为了弄清铜绿的组成和铜生锈生成铜绿的条件,小花与她们的化学实验小组进行了如下探究实验:
(一)探究铜绿的组成。
(查阅资料)“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);铜绿受热易分解。
(实验设计)
①小花同学从铜制眼镜框上取下适量的干燥铜绿,按图所示装置进行实验。在实验过程中,观察到:试管口有水珠出现,说明了铜绿中含有_________元素;澄清石灰水变浑浊,说明了铜绿中含有________元素。
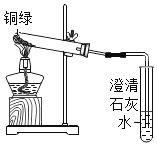
②小阳取下少量试管内反应后的剩余物,放人另一支试管中,滴入稀硫酸,充分反应后,溶液变蓝色,说明铜绿中含有___________元素。
(实验结论)③______________________________________________________________________________。
(二)探究铜生锈的条件。
(查阅资料)1铜绿受热会分解成三种氧化物。
①写出铜绿分解的化学方程式为_______________________________________________________________。
2碱石灰主要成分是氢氧化钠和氧化钙固体的混合物,实验室常用氢氧化钠溶液吸收二氧化碳气体、常用碱石灰除去二氧化碳气体和水蒸气。
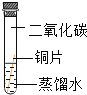
(实验设计)借鉴课本“铁钉锈蚀条件的探究”实验,小平设计了“铜片锈蚀条件的探究”实验,实验如下图所示将四小块铜片分别按下图所示放置一个月,观察现象如下:
| 实验装置 | 
| 
| 
| 
|
| 实验现象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面附近锈蚀最严重的 |
(实验结论)②铜生锈是铜与氧气、___________、__________等物质共同作用的结果。
(反思应用)③写出防止铁或铜等金属制品生锈的两种不同原理的方法__________________________________________________________________________________________________。
-
小花同学发现自己的铜制眼镜框表面出现了绿色的铜锈。为了弄清铜绿的组成和铜生锈生成铜绿的条件,小花与她们的化学实验小组进行了如下探究实验:
(一)探究铜绿的组成。
(查阅资料)“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);铜绿受热易分解。
(实验设计)
①小花同学从铜制眼镜框上取下适量的干燥铜绿,按图所示装置进行实验。在实验过程中,观察到:试管口有水珠出现,说明了铜绿中含有_________元素;澄清石灰水变浑浊,说明了铜绿中含有________元素。
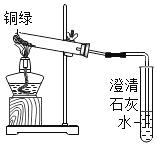
②小阳取下少量试管内反应后的剩余物,放人另一支试管中,滴入稀硫酸,充分反应后,溶液变蓝色,说明铜绿中含有___________元素。
(实验结论)③______________________________________________________________________________。
(二)探究铜生锈的条件。
(查阅资料)1铜绿受热会分解成三种氧化物。
①写出铜绿分解的化学方程式为_______________________________________________________________。
2碱石灰主要成分是氢氧化钠和氧化钙固体的混合物,实验室常用氢氧化钠溶液吸收二氧化碳气体、常用碱石灰除去二氧化碳气体和水蒸气。
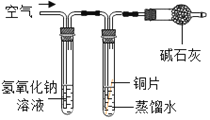
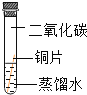
(实验设计)借鉴课本“铁钉锈蚀条件的探究”实验,小平设计了“铜片锈蚀条件的探究”实验,实验如下图所示将四小块铜片分别按下图所示放置一个月,观察现象如下:
| 实验装置 | 
| 
| 
| 
|
| 实验现象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面附近锈蚀最严重的 |
(实验结论)②铜生锈是铜与氧气、___________、__________等物质共同作用的结果。
(反思应用)③写出防止铁或铜等金属制品生锈的两种不同原理的方法__________________________________________________________________________________________________。
-
铜锈,俗称“铜绿”,主要成分是Cu2(OH)2CO3。课外活动小组围绕铜生锈的条件展开探究:
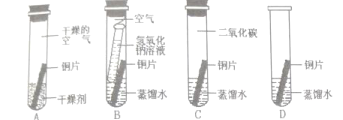

(查阅资料)二氧化碳易与氢氧化钠溶液发生化学反应,生成碳酸钠和水。
提出问题)铜在什么条件下会生锈?
(假设猜想)根据铜锈主要成分的化学式,猜想铜生锈可能是铜与空气中水、氧气、_______共同作用的结果。
(探究过程)小组同学设计了“铜片锈蚀条件的探究”实验如上图所示:实验进行较长一段时间后,观察现象可发现_______(填序号)试管中的光亮铜片最先生锈。B试管中氢氧化钠溶液的作用____________。
(评价与改进)我认为课外小组设计的实验不够完普,若要得出正确结论,还要补充的一个实验是(也可在上面方框内画图表示)_____________
(反思与小结)补充实验后,通过实验证明了原猜想正确,则铜生锈变成铜绿的化学方程式为______
(拓展应用)写出一种防止铁或铜等金属制品生锈的具体方法为______。
-
生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.

探究活动一:验证铜锈的组成
【査阅资料】①铜锈为绿色,其主要成分是Cu2(OH)2CO3.②白色的硫酸铜粉末遇水能变为蓝色.③碳不与稀硫酸反应.④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
【进行实验1】同学们设计了如图所示装置并进行实验.
| 实验橾作 | 实验现象 | 实验结论 |
| ①按如图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有 ; 铜绣由 元素组成; 烧杯中发生反应的化学方程式为 . |
| ③冷却后,向试管中固体 加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变 为蓝色. |
【进行实验2】同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 
| 在干燥环境中,铜不易生锈 | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是 . (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是 |
| 实验2 | 
| |
| 实验3 | 
| |
| 实验4 | 
| 铜生锈的条件是 |