-
亚硝酰氯((ClNO)是合成有机物的重要中间体,某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度,相关实验装置如图所示。
已知:1).亚硝酰氯沸点为-5.5℃,易水解,C1NO+H2O=HNO2+HCl;
2).AgNO2微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3+HNO2。
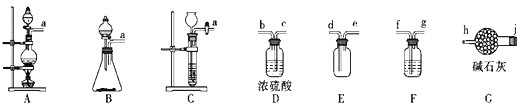
(1)制备Cl2的发生装置可以选用__(填字母代号)装置,发生反应的离子方程式为__。
(2)欲收集一瓶干燥纯净的氯气,选择合适的装置,其连接顺序为a→__(按气流方向,用小写字母表示)。
(3)实验室可用图示装置制备亚硝酰氯:
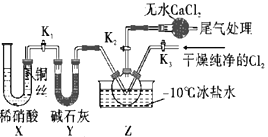
本实验利用X装置制备NO最主要的优点为__,装置中无水CaCl2的作用是__。
(4)通过以下实验测定C1NO样品的纯度。取Z中所得液体mg溶于水,配制成250mL溶液;取出25.00mL样品溶于锥形瓶中,以K2CrO4溶液为指示剂,用cmol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。滴定终点的现象是__,亚硝酰氯(ClNO)的质量分数为__。(已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-2)
-
亚硝酰氯(ClNO)是有机物合成中的重要试剂,红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种氢化物和两种氧化物。某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度,相关实验(夹持装置略去) 如下。请回答:
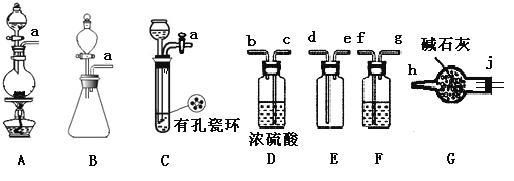
(1)制备Cl2发生装置可以_____(填大写字母),反应的离子方程式为____________________。
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a ______________________(按气流方向,用小写字母表示),若用到F,其盛装药品为____________________。
______________________(按气流方向,用小写字母表示),若用到F,其盛装药品为____________________。
(3)实验室可用下图装置制备亚硝酰氯(ClNO);
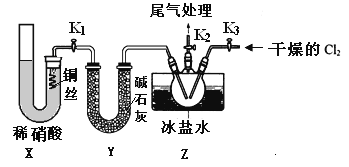
①实验室也可用B装置制备NO,X装置的优点为________________________________。
②检验装置气密性并装入药品,打开k2,然后再打开________(填“k1”"或“k3”),通入一段时间气体,(其目的为_________________________________________________),然后进行其它操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中ClNO可能发生反应的化学方程式为__________________。
(4)取Z中所得液体m g溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用c mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。(已知:Ag2CrO4为砖红色固体;
Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12),则亚硝酰氯(ClNO)的质量分数为_______________(用代数式表示)。
-
亚硝酰氯(ClNO)是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味、遇水反应生成一种氯化物和两种氮化物。某学习小组在实验空用Cl2和NO制备ClNO并测定其纯度,相关实验装置(夹持装置略去)如下图所示。请回答:
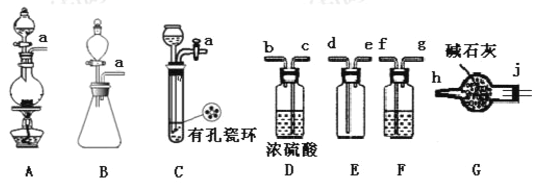
(1)制备C12发生装置可以选用____(填写字母代号),请写出发生反应的离子方程式:____________。
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→_______(按气流方向,用小写字母表示)。
(3)实验室可用下图装置制备亚硝酰氯(C1NO):
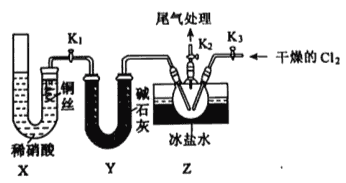
①实验室也可用B装置制备NO,X装置的优点为__________。
②检验装置气密性并装入药品,打开K2,然后再打开K1,通入一段时间气体,其目的为_______,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中C1NO可能发生反应的化学方程式为________。
(4)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol•L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。则亚硝酰氯(C1NO)的质量分数为______(用代数式表示)。[已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(K2CrO4)=1×10-12]
-
亚硝酰氯(ClNO)常用于合成洗涤剂、触媒及用作中间体,某学习小组在实验室用Cl2与NO制备ClNO并测定其纯度,进行如下实验(夹持装置略去)。
查阅资料:亚硝酰氯(ClNO)的熔点为-64.5℃、沸点为-5.5℃,气态呈黄色,液态时呈红褐色,遇水易反应生成一种氢化物和两种氮的常见氧化物,其中一种呈红棕色。
请回答下列问题:
Ⅰ.Cl2的制备:舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。
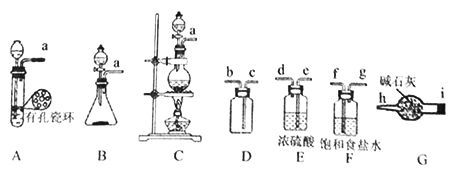
(1)该方法可以选择上图中的________(填字母标号)为Cl2发生装置,该反应中被氧化与被还原物质的物质的量之比为_____________。
(2)欲收集一瓶干燥的氯气,选择上图中的装置,其连接顺序为:a→____→i→h(按气流方向填小写字母标号)。
Ⅱ.亚硝酰氯(ClNO)的制备、实验室可用下图装置制备亚硝酰氯(ClNO):
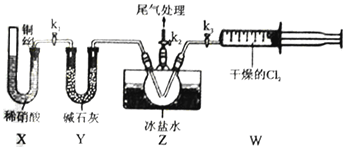
(3)实验室也可用B装置制备NO,与之相比X 装置的优点为__________________________。
(4)组装好实验装置后应先____________,然后依次装入药品、打开k2、再打开__________(填“k1”或“k3”),通入一段时间气体,其目的是为了排尽三颈烧瓶中的空气,防止NO、ClNO 变质。接下来,两种气体在Z中反应的现象为________________________________。
III.亚硝酰氯(ClNO)纯度的测定:将所得亚硝酰氯(ClNO)产品13.10g溶于水,配制成250mL溶液;取出25.00mL,以K2CrO4溶液为指示剂,用0.8mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为 22.50mL。(已知:AgCrO4为砖红色固体)
(5)亚硝酰氯(ClNO)与水反应的化学方程式为_________________________。
(6)亚硝酰氯(ClNO)的质量分数为______________________。
-
亚硝酰氯(ClNO)常用于合成洗涤剂、触媒及用作中间体,某学习小组在实验室用Cl2与NO制备ClNO并测定其纯度,进行如下实验(夹持装置略去)。
查阅资料:亚硝酰氯(ClNO)的熔点为-64.5℃、沸点为-5.5℃,气态呈黄色,液态时呈红褐色,遇水易反应生成一种氯化物和两种氮的常见氧化物,其中一种呈红棕色。
请回答下列问题:
Ⅰ.Cl2的制备:舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。
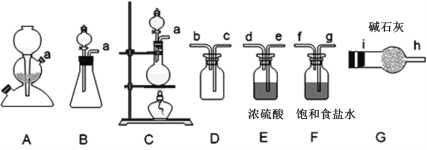
(1)该方法可以选择上图中的______(填字母标号)为Cl2发生装置,该反应中被氧化与被还原物质的物质的量之比为____________。
(2)欲收集一瓶纯净干燥的氯气,选择上图中的装置,其连接顺序为:a→______→i→h(按气流方向填小写字母标号)。
Ⅱ.亚硝酰氯(ClNO)的制备、实验室可用下图装置制备亚硝酰氯(ClNO):
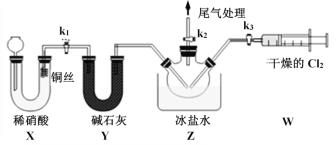
(3)实验室也可用B装置制备NO,与B装置相比,使用X装置的优点为___________。
(4)组装好实验装置后应先________________________,然后装入药品。一段时间后,两种气体在Z中反应的现象为____________________________。
III.亚硝酰氯(ClNO)纯度的测定:将所得亚硝酰氯(ClNO)产品13.10 g溶于水,配制成250 mL溶液;取出25.00 mL,以K2CrO4溶液为指示剂,用0.8 mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为 22.50 mL。(已知:Ag2CrO4为砖红色固体)
(5)亚硝酰氯(ClNO)与水反应的离子方程式为__________________________。
(6)滴定终点的现象是________________________________________。
(7)亚硝酰氯(ClNO)的质量分数为____________。
-
亚硝酰氯(ClNO)常用于合成洗涤剂、触媒及用作中间体,某学习小组在实验室用Cl2与NO制备ClNO并测定其纯度,进行如下实验(夹持装置略去)。
查阅资料:亚硝酰氯(ClNO)的熔点为-64.5℃、沸点为-5.5℃,气态呈黄色,液态时呈红褐色,遇水易反应生成一种氯化物和两种氮的常见氧化物,其中一种呈红棕色。
请回答下列问题:
Ⅰ.Cl2的制备:舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。
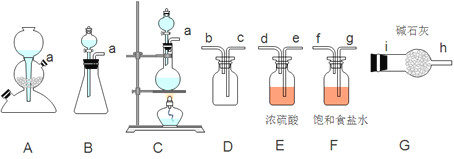
(1)该方法可以选择上图中的______(填字母标号)为Cl2发生装置,该反应中被氧化与被还原物质的物质的量之比为______。
(2)欲收集一瓶纯净干燥的氯气,选择上图中的装置,其连接顺序为:a→______→i→h(按气流方向填小写字母标号)。
Ⅱ.亚硝酰氯(ClNO)的制备、实验室可用下图装置制备亚硝酰氯(ClNO):
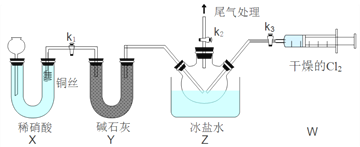
(3)实验室也可用B装置制备NO,与B装置相比,使用X 装置的优点为______。
(4)组装好实验装置后应先______,然后装入药品。一段时间后,两种气体在Z中反应的现象为______。
III.亚硝酰氯(ClNO)纯度的测定:将所得亚硝酰氯(ClNO)产品13.10 g溶于水,配制成250 mL溶液;取出25.00 mL,以K2CrO4溶液为指示剂,用0.8 mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为 22.50 mL。(已知:Ag2CrO4为砖红色固体)
(5)亚硝酰氯(ClNO)与水反应的离子方程式为______。
(6)亚硝酰氯(ClNO)的质量分数为______。(保留两位有效数字)
-
亚硝酰氯 是有机物合成中的重要试剂,其沸点为
是有机物合成中的重要试剂,其沸点为 ,易水解。已知:
,易水解。已知: 微溶于水,能溶于硝酸,
微溶于水,能溶于硝酸, ,某学习小组在实验室用
,某学习小组在实验室用 和NO制备ClNO并测定其纯度,相关实验装置如图所示。
和NO制备ClNO并测定其纯度,相关实验装置如图所示。
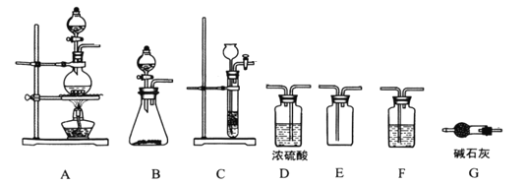
⑴制备 的发生装置可以选用_______(填字母代号)装置,发生反应的离子方程式为___________。
的发生装置可以选用_______(填字母代号)装置,发生反应的离子方程式为___________。
⑵欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为 ________________(填字母代号)。
________________(填字母代号)。
⑶实验室可用图示装置制备亚硝酰氯,检验装置气密性并装入药品,打开 ,然后再打开
,然后再打开 ,通入一段时间气体,其目的是____________,然后进行其他操作,当Z中有一定量液体生成时,停止实验。
,通入一段时间气体,其目的是____________,然后进行其他操作,当Z中有一定量液体生成时,停止实验。
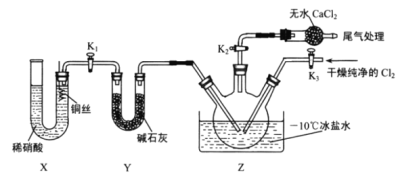
⑷已知:ClNO水解生成 写出化学反应方程式__________________。
写出化学反应方程式__________________。
①欲设计实验证明 是弱酸,需选择如下_____________试剂开展实验
是弱酸,需选择如下_____________试剂开展实验 填选项
填选项 。
。
A.  溶液 B.
溶液 B.  溶液 C. 红色石蕊试纸 D. 蓝色石蕊试纸
溶液 C. 红色石蕊试纸 D. 蓝色石蕊试纸
 已知下列物质在常温下的
已知下列物质在常温下的 如图:
如图:
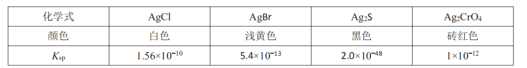
通过以下实验测定ClNO样品的纯度。取Z中所得液体 溶于水,配制成
溶于水,配制成 溶液;取出
溶液;取出 样品溶于锥形瓶中,用
样品溶于锥形瓶中,用 标准溶液滴定至终点,应加入的指示剂是_______________。
标准溶液滴定至终点,应加入的指示剂是_______________。
A. B.
B.  C.
C.  D.
D. 
消耗标准溶液的体积为 ,滴定终点的现象是 ________________,亚硝酰氯
,滴定终点的现象是 ________________,亚硝酰氯 的质量分数为________。
的质量分数为________。
-
亚硝酰氯 常用于合成洗涤剂、触媒及用作中间体。某学习小组在实验室用
常用于合成洗涤剂、触媒及用作中间体。某学习小组在实验室用 与NO制备ClNO并测定其纯度,进行如下实验
与NO制备ClNO并测定其纯度,进行如下实验 夹持装置略去
夹持装置略去 。
。
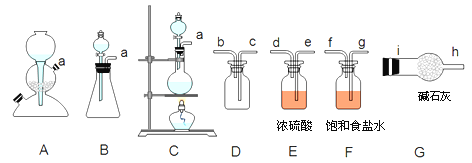
查阅资料:
 年,瑞典化学家舍勒在研究软锰矿
年,瑞典化学家舍勒在研究软锰矿 主要成分是
主要成分是 的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。
的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。
 亚硝酰氯
亚硝酰氯 的熔点为
的熔点为 、沸点为
、沸点为 ,气态呈黄色,液态时呈红褐色。
,气态呈黄色,液态时呈红褐色。
 亚硝酰氯遇水易反应生成一种氯化物和两种氮的常见氧化物,其中一种呈红棕色。
亚硝酰氯遇水易反应生成一种氯化物和两种氮的常见氧化物,其中一种呈红棕色。
请回答下列问题:
Ⅰ 的制备:舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。
的制备:舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。
(1)该方法可以选择上图中的______ 填字母标号
填字母标号 为
为 发生装置,该反应中被氧化与被还原物质的物质的量之比为______。
发生装置,该反应中被氧化与被还原物质的物质的量之比为______。
(2)欲收集一瓶纯净干燥的氯气,选择上图中的装置,其连接顺序为: ______
______ 按气流方向填小写字母标号
按气流方向填小写字母标号 。
。
Ⅱ 亚硝酰氯
亚硝酰氯 的制备。实验室可用下图装置制备亚硝酰氯
的制备。实验室可用下图装置制备亚硝酰氯 冰盐水的温度一般在
冰盐水的温度一般在 :
:
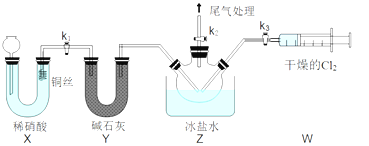
(3)实验室也可用B装置制备NO;与B装置相比,使用X装置的优点为 ______。
(4)组装好实验装置后应先______,然后装入药品。一段时间后,两种气体在Z中反应的现象为______。
 亚硝酰氯
亚硝酰氯 纯度的测定:将所得亚硝酰氯
纯度的测定:将所得亚硝酰氯 产品
产品 溶于水,配制成
溶于水,配制成 溶液;取出
溶液;取出 ,以
,以 溶液为指示剂,用
溶液为指示剂,用 标准溶液滴定至终点,消耗标准溶液的体积为
标准溶液滴定至终点,消耗标准溶液的体积为  。
。 已知:
已知: 为砖红色固体
为砖红色固体
(5)配制溶液时除使用烧杯、玻璃棒、胶头滴管外,还需用到的玻璃仪器是_________;滴定终点判断的方法是____________________________。
(6)亚硝酰氯 与水反应的离子方程式为_________________________。亚硝酰氯
与水反应的离子方程式为_________________________。亚硝酰氯 的质量分数为_____________。
的质量分数为_____________。
-
亚硝酰氯 是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种氢化物和两种氧化物。某学习小组在实验室用
是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种氢化物和两种氧化物。某学习小组在实验室用 和NO制备ClNO并测定其纯度。请回答:
和NO制备ClNO并测定其纯度。请回答:
I.甲组的同学拟制备原料气NO和 ,制备装置如下图所示:
,制备装置如下图所示:
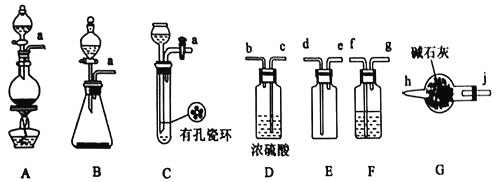
(1)若制备 发生装置选B,则反应的离子方程式为_________________。若制备NO发生装置也选B,锥形瓶中放的是Cu片,则分液漏斗中的试剂为_______。
发生装置选B,则反应的离子方程式为_________________。若制备NO发生装置也选B,锥形瓶中放的是Cu片,则分液漏斗中的试剂为_______。
(2)欲收集一瓶干燥纯净的氯气,选择装置其连接顺序为: ___
___ ___
___ ___
___ ___
___ ___
___ ___
___ 按气流方向,用小写字母表示
按气流方向,用小写字母表示 ,其中F装置的作用为________。
,其中F装置的作用为________。
II.乙组同学利用甲组制得的NO和 制备NOCl,装置如图所示:
制备NOCl,装置如图所示:


(3)为了使气体充分反应,从A处进入的气体是_______ 填
填 或
或 。
。
(4)装置Ⅲ、Ⅳ除可干燥NO、 外,另一个作用是_________________。
外,另一个作用是_________________。
(5)装置Ⅷ的烧杯中盛放的试剂是______ 填编号:
填编号: 水
水  热水
热水  冰水
冰水
-
亚硝酰氯(NOCl)是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种烈化物和两种氧化物。某学习小组在实验用C12和NO制备NOCl并测定其纯度,相关实验(装置略去)如下。请回答:
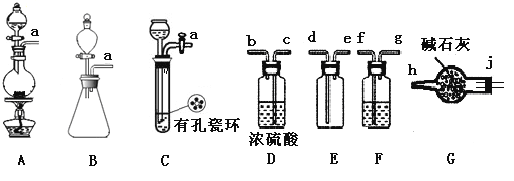
(1)制备Cl2发生装置可______ (填大写字母),反应的离子方程式为_______。
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→________(按气流方向,用小写字母表示),若用到F,其盛装药品为_________。
(3)实验室可用下图装置制备亚硝酰氯(NOCl)
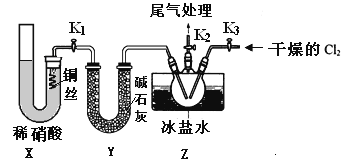
①实验室也可用B装置制备NO,上图X装置的优点为__________(至少写出两点)
②检验装置气密性并装入药品,打开k2,然后再打开____(填“k1”或“k3”),通入一段时间气体,其目的为________,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装肖Y,则Z中NOCl可能发生反应的化学方程式为_________
(4)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol/LAgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL.已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12,则亚硝酰氯(NOC1)的质量分数为____(用代数式表示,不必化简)。





















