-
乙二醛(OHC-CHO)是一种重要的精细化工产品。长郡中学高三化学兴趣小组利用乙醛液相硝酸氧化法制备乙二醛并测定乙二醛纯度,装置如图所示。
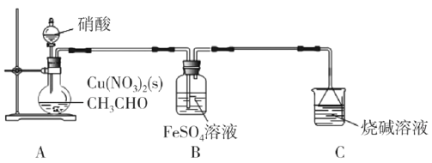
已知:①NO+FeSO4=FeSO4·NO(棕色)。
②几种有机物的部分性质如表所示:
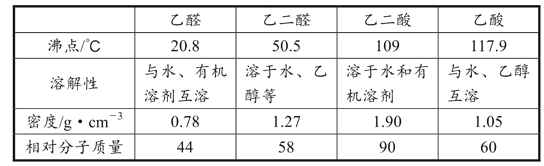
实验步骤:
①取20mL的乙醛装于烧瓶,加入2gCu(NO3)2粉末作催化剂,向烧瓶中缓慢滴加2mol·L-1硝酸至乙醛完全反应为止;
②提纯产品,最终得到10.0mL产品。
请回答下列问题:
(1)盛装硝酸的仪器名称是__。
(2)实验中,观察到装置B中溶液变为棕色,制备乙二醛的化学方程式为__。
(3)向烧瓶中滴加硝酸要“缓慢”,其目的是__;判断烧瓶中制备乙二醛的反应已完成的标志是__。
(4)分离提纯产品,宜选择下列装置__(填字母)。
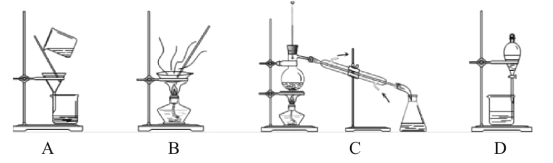
(5)根据上述实验数据,该实验中乙二醛的产率约为__(填字母)。
a.56.5% b.61.8% c.67.9% d.72.6%
(6)实验室可用酸性KMnO4溶液测定乙二醛的纯度,发生反应的离子方程式为:18H++6MnO4-+5C2H2O2→10CO2↑+6Mn2++14H2O。实验步骤如下:取VmL产品,加蒸馏水稀释至250mL,量取25.00mL稀释后的溶液于锥形瓶,滴加5.00mL稀硫酸,用cmol·L-1KMnO4溶液,三次平行实验消耗KMnO4溶液体积如下:
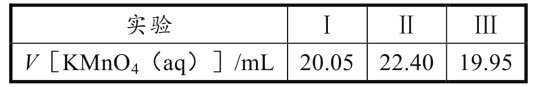
滴定终点的标志是__;该产品纯度为___g·mL-1(用含V和c的代数式表示)。
-
乙二醛(OHC-CHO)是一种重要的精细化工产品。
Ⅰ.工业生产乙二醛
(1)乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,反应的化学方程式为 。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点是 。
(2)乙二醇(HOCH2CH2OH)气相氧化法
① 已知:OHC-CHO(g)+2H2(g) HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
2H2(g)+O2(g) 2H2O(g) ΔH=-484 kJ·mol-1 K2
2H2O(g) ΔH=-484 kJ·mol-1 K2
乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g) OHC—CHO(g)+2H2O(g)的ΔH= kJ·mol-1。相同温度下,该反应的化学平衡常数K= (用含K1、K2的代数式表示)。
OHC—CHO(g)+2H2O(g)的ΔH= kJ·mol-1。相同温度下,该反应的化学平衡常数K= (用含K1、K2的代数式表示)。
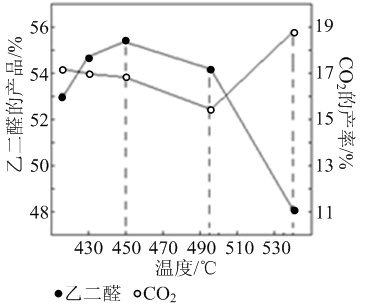
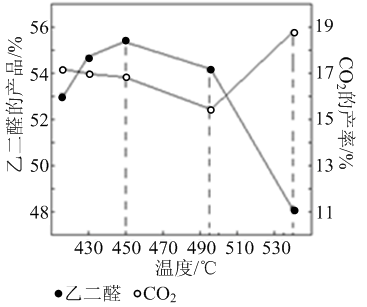
② 当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示。反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是 、
Ⅱ.乙二醛电解氧化制备乙醛酸(OHC—COOH)的生产装置如下图所示,通电后,阳极产生的Cl2 与乙二醛溶液反应生成乙醛酸。
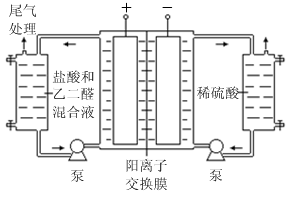
(3)阴极电极式为
(4)阳极液中盐酸的作用,除了产生氯气外,还有
(5)保持电流强度为a A,电解t min,制得乙醛酸m g,列式表示该装置在本次电解中的电流效率η=
(设:法拉第常数为f C·mol-1;η= )
)
-
乙二醛(OHC—CHO)是一种重要的精细化工产品。
Ⅰ. 工业生产乙二醛
(1)乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,反应的化学方程式为 。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点是 。
(2)乙二醇(HOCH2CH2OH)气相氧化法
①已知:OHC—CHO(g) +2H2(g) HOCH2CH2OH(g) △H=−78kJ·mol−1 K1
HOCH2CH2OH(g) △H=−78kJ·mol−1 K1
2H2(g) + O2(g) 2H2O(g) △H=−484kJ·mol−1 K2
2H2O(g) △H=−484kJ·mol−1 K2
乙二醇气相氧化反应HOCH2CH2OH(g) +O2(g) OHC—CHO(g) + 2H2O(g)的△H= kJ·mol−1。相同温度下,该反应的化学平衡常数K= (用含K1、K2的代数式表示)。
OHC—CHO(g) + 2H2O(g)的△H= kJ·mol−1。相同温度下,该反应的化学平衡常数K= (用含K1、K2的代数式表示)。
②当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示。反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是 、 。
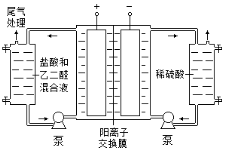
Ⅱ. 乙二醛电解氧化制备乙醛酸(OHC—COOH)的生产装置如下图所示,通电后,阳极产生的Cl2与乙二醛溶液反应生成乙醛酸。
(3)阴极反应式为 。
(4)阳极液中盐酸的作用,除了产生氯气外,还有 。
(5)保持电流强度为a A,电解t min,制得乙醛酸m g,列式表示该装置在本次电解中的电流效率η= 。(设:法拉第常数为f C•mol−1;η= )
)
-
乙二醛(OHC-CHO)是一种重要的精细化工产品。
Ⅰ.工业生产乙二醛
(1).乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,反应的化学方程式为______该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点是_______
(2).乙二醇(HOCH2CH2OH)气相氧化法
l).已知:OHC-CHO(g)+2H2(g) HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
2H2(g)+O2(g) 2H2O(g) ΔH=-484 kJ·mol-1 K2
2H2O(g) ΔH=-484 kJ·mol-1 K2
乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g) OHC—CHO(g)+2H2O(g)的ΔH=________kJ·mol-1。相同温度下,该反应的化学平衡常数K=________(用含K1、K2的代数式表示)。
OHC—CHO(g)+2H2O(g)的ΔH=________kJ·mol-1。相同温度下,该反应的化学平衡常数K=________(用含K1、K2的代数式表示)。
2).反应②在热力学上趋势很大,其原因是________
3).当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示。反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是_____________、_____________________
4).在恒温恒容下,如果从反应物出发建立平衡,能说明乙二醇气相氧化反应达到平衡状态的是_______(填选项字母)。
A.体系压强不再变化 B.氧醇比保持不变
C.混合气体的密度保持不变 D.气体平均相对分子质量保持不变
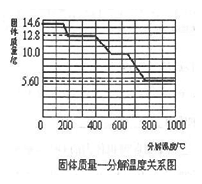
Ⅱ.乙二醛被氧化可生成乙二酸即草酸,某些蔬菜中含有较多的草酸,如果人类不注意合理饮食容易形成草酸钙结石。某研究所利用SDT Q600热分析仪对草酸钙晶体(CaC2O4·H2O)进行热分解,获得相关数据,绘制成固体质量一一分解温度的关系如下图。如果残留固体为11.12 克,求残留固体的成分和物质的量_________。
-
碳及其化合物在有机合成、能源开发等工农业方面具有十分广泛的应用。
I.工业生产精细化工产品乙二醛(OHC-CHO)
(1)乙醇(CH3CH2OH)液相硝酸氧化法:在Cu(NO3)2催化下,用稀硝酸氧化乙醇制取乙二醛,此反应的化学方程式为_______________。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点____________。
(2)乙二醇(HOCH2CH2OH)气相氧化法
已知:2H2(g)+O2(g)  2H2O(g) ΔH=-484kJ/mol,化学平衡常数为K1
2H2O(g) ΔH=-484kJ/mol,化学平衡常数为K1
OHC-CHO(g)+2H2(g)  HOCH2CH2OH(g) ΔH=-78kJ/mol,化学平衡常数为K2
HOCH2CH2OH(g) ΔH=-78kJ/mol,化学平衡常数为K2
则乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g)  OHC-CHO(g)+2H2O(g)的ΔH=______;相同温度下,该反应的化学平衡常数K=______(用含K1、K2的代数式表示)。
OHC-CHO(g)+2H2O(g)的ΔH=______;相同温度下,该反应的化学平衡常数K=______(用含K1、K2的代数式表示)。
Ⅱ.CO2的综合利用
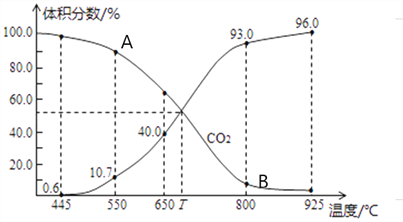
(3)一定量的CO2与足量的碳在体积可变的恒压密闭容器中发生反应C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示,则下列说法正确的是______(填字母)。
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示,则下列说法正确的是______(填字母)。
a.反应达平衡状态时,混合气体的平均相对分子质量保持不变
b.A点的正反应速率比B点正反应速率小
C.550℃时,若充入氦气,则V正、V逆均减小,平衡不移动
d.T℃时,反应达平衡后CO2的转化率为66.7%
e. T℃时,若再充入1molCO2和1molCO,平衡不移动
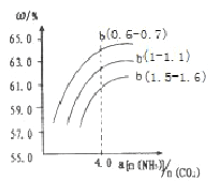
(4)氨气、CO2在一定条件下可合成尿素,其反应为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g),右图表示合成塔中氨碳比a与CO2转化率ω的关系。a为{n(NH3)/n(CO2)},b为水碳比{n(H2O)/n(CO2)}。则
CO(NH2)2(s)+H2O(g),右图表示合成塔中氨碳比a与CO2转化率ω的关系。a为{n(NH3)/n(CO2)},b为水碳比{n(H2O)/n(CO2)}。则
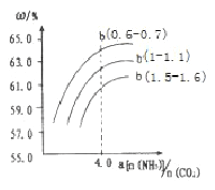
①b应控制在______
a.1.5-1.6 b.1-1.1 c.0.6-0.7
②a应控制在4.0的理由是_________
-
碳及其化合物在有机合成、能源开发等工农业方面具有十分广泛的应用。
I.工业生产精细化工产品乙二醛(OHC-CHO)
(1)乙醇(CH3CH2OH)液相硝酸氧化法:在Cu(NO3)2催化下,用稀硝酸氧化乙醇制取乙二醛,此反应的化学方程式为_______________。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点____________。
(2)乙二醇(HOCH2CH2OH)气相氧化法
已知:2H2(g)+O2(g)  2H2O(g) ΔH=-484kJ/mol,化学平衡常数为K1
2H2O(g) ΔH=-484kJ/mol,化学平衡常数为K1
OHC-CHO(g)+2H2(g)  HOCH2CH2OH(g) ΔH=-78kJ/mol,化学平衡常数为K2
HOCH2CH2OH(g) ΔH=-78kJ/mol,化学平衡常数为K2
则乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g)  OHC-CHO(g)+2H2O(g)的ΔH=______;相同温度下,该反应的化学平衡常数K=______(用含K1、K2的代数式表示)。
OHC-CHO(g)+2H2O(g)的ΔH=______;相同温度下,该反应的化学平衡常数K=______(用含K1、K2的代数式表示)。
Ⅱ.CO2的综合利用
(3)一定量的CO2与足量的碳在体积可变的恒压密闭容器中发生反应C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示,则下列说法正确的是______(填字母)。
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示,则下列说法正确的是______(填字母)。

a.反应达平衡状态时,混合气体的平均相对分子质量保持不变
b.A点的正反应速率比B点正反应速率小
C.550℃时,若充入氦气,则V正、V逆均减小,平衡不移动
d.T℃时,反应达平衡后CO2的转化率为66.7%
e. T℃时,若再充入1molCO2和1molCO,平衡不移动
(4)氨气、CO2在一定条件下可合成尿素,其反应为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g),右图表示合成塔中氨碳比a与CO2转化率ω的关系。a为{n(NH3)/n(CO2)},b为水碳比{n(H2O)/n(CO2)}。则
CO(NH2)2(s)+H2O(g),右图表示合成塔中氨碳比a与CO2转化率ω的关系。a为{n(NH3)/n(CO2)},b为水碳比{n(H2O)/n(CO2)}。则
①b应控制在______
a.1.5-1.6 b.1-1.1 c.0.6-0.7
②a应控制在4.0的理由是_________
-
乙二醛(OHC-CHO )化学性质活泼,是纺织工业中常用的一种有机原料,能增加棉花、尼龙等纤维的防缩性和防皱性。其工业生产方法主要是乙二醇(HOCH2CH2OH )气相催化氧化法和乙醛液相硝酸氧化法。请回答下列相关问题:
(1)乙二醇气相催化氧化法
以乙二醇、氧气为原料,在催化剂存在的条件下,250℃左右开始缓慢进行,生成乙二醛和副产物乙醇酸[CH2(OH)COOH]的反应方程式:
I.HOCH2CH2OH(g)+O2(g)  OHC-CHO(g)+2H2O(g) △H1
OHC-CHO(g)+2H2O(g) △H1
II.HOCH2CH2OH(g)+O2(g)  CH2(OH)COOH(g)+H2O(g) △H2
CH2(OH)COOH(g)+H2O(g) △H2
已知反应I中相关化学键键能数据如下:
| 化学键 | C-H | C-O | H-O | O==O | C==O | C-C |
| E/kJ·mol-1 | 413 | 343 | 465 | 498 | 728 | 332 |
①△H1=_____kJ/mol,反应I的化学平衡常数表达式为K=________。
②欲提高I的平衡产率,可以采取的措施是______ (填标号)。
A.升高温度 B.增大压强 C.降低温度 D.减小压强
③提高乙二醛反应选择性的关键因素是_________________________。
④保持温度和容积不变,下列描述能说明反应I达到平衡状态的是 ________ (填标号)。
A.v正(O2) =2v逆(H2O)
B.混合气体的压强不再随时间变化而变化
C.混合气体的密度不再发生变化
D.乙二醇与OHC-CHO 的物质的量之比为1: 1
E.混合气体中乙二醛的体积分数不再发生变化
(2)乙醛(CH3CHO)液相硝酸氧化法
11.0g40%的乙醛溶液和40%的硝酸,按一定比例投入氧化反应釜内,在Cu(NO3)2催化下,控制温度在38~40℃时,反应10h,再通过萃取等操作除去乙醛、硝酸等,最后经减压浓缩得4.35g40%乙二醛溶液。
①用稀硝酸氧化乙醛制取乙二醛时,有N2O产生。其化学方程式为______________________。
②利用上面数据,计算乙二醛的产率为___________________________。
-
乙二醛(OHC-CHO)是纺织工业常用的一种有机原料,其工业生产方法主要是乙二醇(HOCH2CH2OH)气相催化氧化法和乙醛液相硝酸氧化法,请回答下列相关问题。
(1)乙二醇气相催化氧化法
①乙二醇气相催化氧化的反应为
HOCH2CH2OH(g)+O2(g) OHC-CHO(g)+2H2O(g) △H1 K1
OHC-CHO(g)+2H2O(g) △H1 K1
己知 OHC-CHO(g)+2H2 HOCH2CH2OH(g) △H2 K2
HOCH2CH2OH(g) △H2 K2
H2(g)+l/2O2(g)  H2O(g) △H3 K3
H2O(g) △H3 K3
则△H3= _______(用△H1、△H2表示),相同温度下K1=_______(用K2、K3表示)。
②当原料气中氧气和乙二醇的物质的量之比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示,反应温度超过495℃时,CO2产率升高的主要原因可能是____________。

③在恒容绝热容器中发生反应HOCH2CH2OH(g)+O2(g) OHC-CHO(g)+2H2O(g)(不考虑副反应),一定能说明反应达到平衡状态的是_______(填选项字母)。
OHC-CHO(g)+2H2O(g)(不考虑副反应),一定能说明反应达到平衡状态的是_______(填选项字母)。
A.氧气浓度保持不变 B.气体总物质的量保持不变
C.平衡常数保持不变 D.氧气和乙二醇的物质的量之比保持不变
(2)乙醛液相硝酸氧化法
乙醛液相硝酸氧化法是在催化剂的作用下,用稀硝酸氧化乙醛制取乙二醛,该法与乙二醇气相 催化氧化法相比明显的缺点是__________________。(任写一条)
(3)乙二醛电解氧化制备乙醛酸(OHC-COOH)的生产装置如下图所示,通电后,阳极产生的Cl2与乙二醛溶液反应生成乙醛酸,请写出该反应的化学方程式_______________。

-
乙醛酸(OHC-COOH)是一种重要的精细化工产品。以高硅铸铁为惰性电极材料,用恒电势电解NaBr溶液间接氧化乙二醛(OHC-CH0)制备乙醛酸: 。装置如图所示。下列说法不正确的是
。装置如图所示。下列说法不正确的是

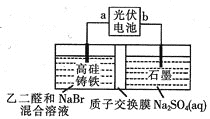
A.电极b为负极,高硅铸铁不损耗
B.阳极的电极反应式为
C.电池正常工作时,左室电解质溶液中 保持不变
保持不变
D.电解过程中,右室溶液的pH逐渐升高
-
硫酸亚铁是一种重要的化工产品,在工业上有重要的用途。某校化学兴趣小组,利用工业烧渣为原料,设计如下制备硫酸亚铁的方案。学生探究烧渣(主要成分为铁的氧化物及少量FeS、SiO2 等)制备绿矾(FeSO4·7H2O)。工艺流程如下所示:
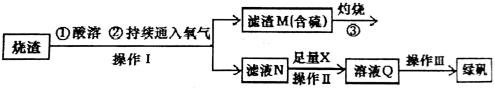
(1)烧渣在进行酸溶时用到了稀硫酸。他们在配制所需的稀硫酸时使用了自来水,有同学提出自来水中含有少量的Cl-,会影响到制出的FeSO4 的纯度。请你设计实验证明已配制的稀硫酸中混有Cl-。
_______________________。
(2)过程③灼烧时产生的气体通入下列溶液中, 溶液不会褪色的是___________
溶液不会褪色的是___________
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.红色的酚酞试液
(3)X 是 , 此时滤液N 中发生反应的离子方程式为 。检验溶液Q 中含有的金属阳离子的实验方法是 。
(4)操作III 的操作步骤为蒸发浓缩、 、过滤( 填操作名称)、  、干燥。
、干燥。
(5)硫酸亚铁可以用于治疗缺铁性贫血症,某严重贫血患者共需补充2.8g铁元素,服用的药品中相当于需要绿矾的质量为_________。






 )
)

 )
)








