-
二氧化硫(SO2)是一种在空间地理、环境科学、地质勘探等领域受到广泛研究的一种气体。

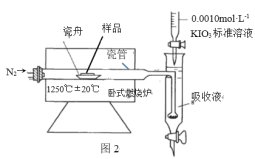
Ⅰ.某研究小组设计了一套制备及检验 SO2 部分性质的装置,如图 1 所示。
(1)仪器 A 的名称______________,导管 b 的作用______________。
(2)装置乙的作用是为了观察生成 SO2的速率,则装置乙中加入的试剂是______________。
(3)①实验前有同学提出质疑:该装置没有排空气,而空气中的 O2 氧化性强于 SO2,因此 装置丁中即使有浑浊现象也不能说明是 SO2 导致的。请你写出 O2 与 Na2S 溶液反应的化学 反应方程式______________。
②为进一步检验装置丁产生浑浊现象的原因,进行新的实验探究。实验操作及现象见表。
| 序号 | 实验操作 | 实验现象 |
| 1 | 向 10ml 1mol·L-1 的 Na2S 溶液中通 O2 | 15min 后,溶液才出现浑浊 |
| 2 | 向 10ml 1mol·L-1 的 Na2S 溶液中通 SO2 | 溶液立即出现黄色浑浊 |
由实验现象可知:该实验条件下 Na2S 溶液出现浑浊现象是 SO2 导致的。你认为上表实验 1 反应较慢的原因可能是______________。
Ⅱ.铁矿石中硫元素的测定可以使用燃烧碘量法,其原理是在高温下将样品中的硫元素转化 为 SO2 , 以 淀 粉 和 碘 化 钾 的 酸 性 混 合 溶 液 为 SO2 吸 收 液 , 在 SO2 吸 收 的 同 时 用 0.0010mol·L-1KIO3 标准溶液进行滴定,检测装置如图 2 所示:
[查阅资料] ①实验进行 5min,样品中的 S 元素都可转化为 SO2
②2IO3-+5SO2+4H2O=8H++5SO42-+I2
③I2+SO2+2H2=2I-+SO42-+4H+
④IO3-+5I-+6H+=3I2+3H2O
(4)工业设定的滴定终点现象是______________。
(5)实验一:空白试验,不放样品进行实验,5min 后测得消耗标准液体积为 V1mL
实验二:加入 1g 样品再进行实验,5min 后测得消耗标准液体积为 V2mL
比较数据发现 V1 远远小于 V2,可忽略不计 V1。 测得 V2 的体积如表
| 序号 | 1 | 2 | 3 |
| KIO3 标准溶液体积/mL | 10.02 | 9.98 | 10.00 |
该份铁矿石样品中硫元素的质量百分含量为______________。
-
二氧化硫(SO2)是一种在空间地理、环境科学、地质勘探等领域受到广泛研究的一种气体。
Ⅰ.某研究小组设计了一套制备及检验SO2部分性质的装置,如图所示:
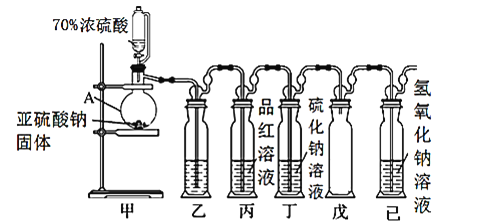
(1)仪器A的名称____________。
(2)装置乙的作用是为了观察生成SO2的速率,则装置乙中加入的试剂是____________。
(3)①实验前有同学提出质疑:该装置没有排空气,而空气中的O2氧化性强于SO2,因此装置丁中即使有浑浊现象也不能说明是SO2导致的。请你写出O2与Na2S溶液反应的化学反应方程式____________。
②为进一步检验装置丁产生浑浊现象的原因,进行新的实验探究。实验操作及现象见表:
| 序号 | 实验操作 | 实验现象 |
| 1 | 向10 mL 1 mol/L Na2S溶液中通O2 | 15 min后,溶液才出现浑浊 |
| 2 | 向10 mL 1 mol/L Na2S溶液中通SO2 | 溶液立即出现黄色浑浊 |
由实验现象可知:该实验条件下Na2S溶液出现浑浊现象是SO2导致的。你认为上表实验1反应较慢的原因可能是____________。
Ⅱ.铁矿石中硫元素的测定可以使用燃烧碘量法,其原理是以氮气为载体,以稀盐酸、淀粉和碘化钾的混合溶液为吸收液,用0.0010 mol·L-1KIO3标准溶液进行滴定。检测装置如图所示:
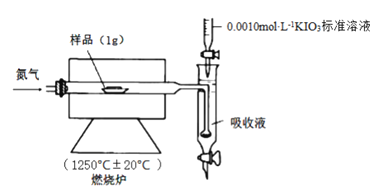
[查阅资料] ①实验进行5min样品中的S元素都可转化为SO2
②2IO3-+5SO2+4H2O=8H++5SO42-+I2
③I2+SO2+2H2O=2I-+SO42-+4H+
④IO3-+5I-+6H+=3I2+3H2O
(4)工业设定的滴定终点现象是____________。
(5)实验一:不放样品进行实验,5 min后测得消耗标准液体积为V1
实验二:加入1 g样品再进行实验,5 min后测得消耗标准液体积为V2
①比较数据发现V1远远小于V2,可忽略不计。则设置实验一的目的是___________。
②测得V2的体积如表:
| 序号 | 1 | 2 | 3 |
| KIO3标准溶液体积/mL | 10.02 | 9.98 | 10.00 |
该份铁矿石样品中硫元素的质量百分含量为____________。
-
ZnO在医药、石化等领域有广泛的用途。研究小组用某闪锌矿(主要成分ZnS,含有FeS、SiO2、MnCO3等杂质)制备氧化锌和硫单质,设计如下流程:
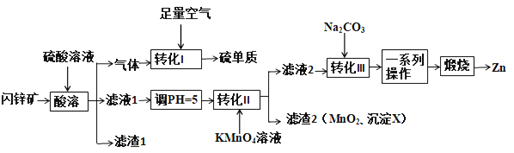
请回答下列问题:
(1)滤渣1的化学式为_______,任写一种该物质的用途:_______________。
(2)沉淀X的化学式为______________。
(3)“转化Ⅱ”中主要反应的离子方程式为___________________________。
(4)若Ksp(ZnCO3)=1.5×10﹣10,溶液中离子浓度≤1.0×10﹣5mol•L﹣1时,认为该离子沉淀完全。则欲使1Lc(Zn2+)=1.5mol•L﹣1溶液中Zn2+沉淀完全,需加入等体积的Na2CO3溶液的物质的量浓度至少为_______________________mol•L﹣1 (写出精确计算结果,溶液混合时体积变化忽略不计)。
(5)“一系列操作”包括过滤、洗涤、干燥。过滤所用的玻璃仪器有______;洗涤沉淀的操作为__________________。
-
ZnO在医药、石化等领域有广泛的用途。研究小组用某闪锌矿(主要成分ZnS,含有FeS、SiO2、MnCO3等杂质)制备氧化锌和硫单质,设计如下流程:

请回答下列问题:
(1)滤渣1的化学式为_______,任写一种该物质的用途:_______________。
(2)沉淀X的化学式为______________。
(3)“转化Ⅱ”中主要反应的离子方程式为___________________________。
(4)若Ksp(ZnCO3)=1.5×10﹣10,溶液中离子浓度≤1.0×10﹣5mol•L﹣1时,认为该离子沉淀完全。则欲使1Lc(Zn2+)=1.5mol•L﹣1溶液中Zn2+沉淀完全,需加入等体积的Na2CO3溶液的物质的量浓度至少为_______________________mol•L﹣1 (写出精确计算结果,溶液混合时体积变化忽略不计)。
(5)“一系列操作”包括过滤、洗涤、干燥。过滤所用的玻璃仪器有______;洗涤沉淀的操作为__________________。
-
二氧化硫是一种大气污染物,研究对NO2、SO2、CO等大气污染气体的处理有重要意义,某化学实验爱好小组欲探究SO2的性质,设计如下方案:
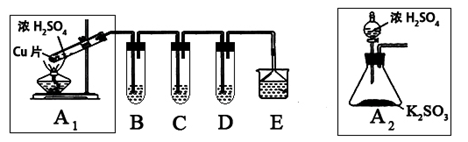
(1)B、C、D分别用于检验SO2的还原性、氧化性和漂白性。其中B、C分别为碘水和硫化氢的水溶液,则D中所盛试剂为_________,B中反应的离子方程式为:_________________。
(2)为了实现绿色实验的目标,某同学重新设计了如上右图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是:________________________________(任写一点即可)。
(3)E中用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子。已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水。
请设计实验证明“吸收液”中存在SO32-和HSO3-,完成下表的实验操作、预期现象和结论:
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1mol/L BaCl2溶液向小烧杯滴加直至过量。 | 若出现白色浑浊,则溶液中存在SO32-或 SO42-。 |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体___________________________________________________________ | _________________________ ______________________________________________ |
| 步骤3:______________________________________________ ___________________________________________________ | _________________________ |
-
SO2是一种大气污染物,但它在化工和食品工业上却有广泛应用。某兴趣小组同学对SO2的实验室制备和性质实验进行研究。
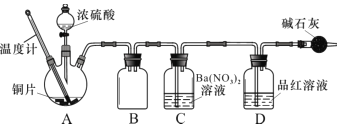
(1)甲同学按照教材实验要求设计如图所示装置制取SO2
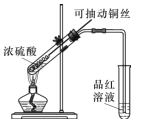
①本实验中铜与浓硫酸反应的化学方程式是 ______,铜丝可抽动的优点是_______。
②实验结束后,甲同学观察到试管底部出现黑色和灰白色固体,且溶液颜色发黑。甲同学认为灰白色沉淀应是生成的白色CuSO4夹杂少许黑色固体的混合物,其中CuSO4以白色固体形式存在体现了浓硫酸的________性。
③乙同学认为该实验设计存在问题,请从实验安全和环保角度分析,该实验中可能存在的问题是________。
(2)兴趣小组查阅相关资料,经过综合分析讨论,重新设计实验如下(加热装置略):
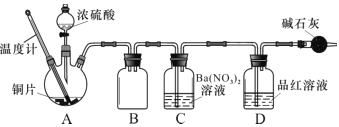
实验记录 A 中现象如下:
| 序号 | 反应温度/℃ | 实验现象 |
| 1 | 134 | 开始出现黑色絮状物,产生后下沉,无气体产生 |
| 2 | 158 | 黑色固体产生的同时,有气体生成 |
| 3 | 180 | 气体放出的速度更快,试管内溶液为黑色浑浊 |
| 4 | 260 | 有大量气体产生,溶液变为蓝色,试管底部产生灰白色固体,品红溶液褪色 |
| 5 | 300 | 同上 |
查阅资料得知: 产物中的黑色和灰白色固体物质主要成分为 CuS、Cu2S 和 CuSO4,其中CuS 和 Cu2S为黑色固体,常温下都不溶于稀盐酸,在空气中灼烧均转化为CuO和SO2。
①实验中盛装浓硫酸的仪器名称为 ____________。
②实验记录表明__________对实验结果有影响,为了得到预期实验现象,在操作上应该____________。
③装置C 中发生反应的离子方程式是 ___________________。
④将水洗处理后的黑色固体烘干后,测定灼烧前后的质量变化,可以进一步确定黑色固体中是否一定含有 CuS其原理为__________(结合化学方程式解释)。
-
SO2是一种大气污染物,但它在化工和食品工业上却有广泛应用。某兴趣小组同学对SO2的实验室制备和性质实验进行研究。
(1)甲同学按照教材实验要求设计如图所示装置制取SO2
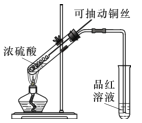
①本实验中铜与浓硫酸反应的化学方程式是 ______,铜丝可抽动的优点是_______。
②实验结束后,甲同学观察到试管底部出现黑色和灰白色固体,且溶液颜色发黑。甲同学认为灰白色沉淀应是生成的白色CuSO4夹杂少许黑色固体的混合物,其中CuSO4以白色固体形式存在体现了浓硫酸的________性。
③乙同学认为该实验设计存在问题,请从实验安全和环保角度分析,该实验中可能存在的问题是________。
(2)兴趣小组查阅相关资料,经过综合分析讨论,重新设计实验如下(加热装置略):
实验记录 A 中现象如下:
| 序号 | 反应温度/℃ | 实验现象 |
| 1 | 134 | 开始出现黑色絮状物,产生后下沉,无气体产生 |
| 2 | 158 | 黑色固体产生的同时,有气体生成 |
| 3 | 180 | 气体放出的速度更快,试管内溶液为黑色浑浊 |
| 4 | 260 | 有大量气体产生,溶液变为蓝色,试管底部产生灰白色固体,品红溶液褪色 |
| 5 | 300 | 同上 |
查阅资料得知: 产物中的黑色和灰白色固体物质主要成分为 CuS、Cu2S 和 CuSO4,其中CuS 和 Cu2S为黑色固体,常温下都不溶于稀盐酸,在空气中灼烧均转化为CuO和SO2。
①实验中盛装浓硫酸的仪器名称为 ____________。
②实验记录表明__________对实验结果有影响,为了得到预期实验现象,在操作上应该____________。
③装置C 中发生反应的离子方程式是 ___________________。
④将水洗处理后的黑色固体烘干后,测定灼烧前后的质量变化,可以进一步确定黑色固体中是否一定含有 CuS其原理为__________(结合化学方程式解释)。
-
某课外研究小组利用粗制氧化铜(含有少量铜)制取胆矾.他们设计了如下两种不同的制备途径:
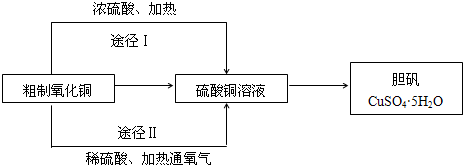
(1)途径1中会产生一种污染环境的气体,该气体的化学式是________.
(2)写出途径2中所有反应的化学方程式________;
(3)金属铜制品长期放置在潮湿的空气中,表面出现一层绿色物质,有关的化学方程式是________.
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是________(填字母).
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 青铜是我国使用最早的合金 | 合金是指多种金属熔合成的金属材料 | Ⅰ错;Ⅱ对;无 |
| B | 精炼铜时,粗铜板作阳极 | 铜具有良好的导电性 | Ⅰ对;Ⅱ对;无 |
| C | 铜锌原电池中,铜是正极 | CuO和Cu2O都是黑色固体 | Ⅰ错;Ⅱ错;无 |
| D | CuO能与水反应生成Cu(OH)2 | 金属氧化物都能与水反应生成相应的金属氢氧化物 | Ⅰ对;Ⅱ对;有 |
-
已知用P2O5作催化剂,加热乙醇可制备乙烯,反应温度为80℃~210℃。某研究性小组设计了如下的装置制备并检验产生的乙烯气体(夹持和加热仪器略去)。
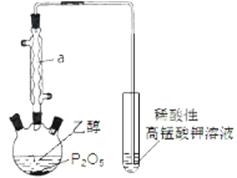
(1)仪器a的名称为 。
(2)用化学反应方程式表示上述制备乙烯的原理 。
(3)已知P2O5是一种酸性干燥剂,吸水放出大量热,在实验过程中P2O5与乙醇能发生作用,因反应用量的不同,会生成不同的磷酸酯,它们均为易溶于水的物质,沸点较低。写出乙醇和磷酸反应生成磷酸二乙酯的化学方程式(磷酸用结构式表示为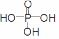 ) 。
) 。
(4)该装置中还缺一种必备仪器,该仪器为 。某同学认为即使添加了该仪器上述装置验证产生了乙烯不够严密,仍须在酸性高锰酸钾溶液之前添加洗气装置,其理由为 。
-
(10分)已知用P2O5作催化剂,加热乙醇可制备乙烯,反应温度为80℃~210℃。某研究性小组设计了如下的装置制备并检验产生的乙烯气体(夹持和加热仪器略去)。


(1)仪器a的名称为_________________
(2)用化学反应方程式表示上述制备乙烯的原理______________________________。
(3)已知P2O5是一种酸性干燥剂,吸水放大量热,在实验过程中P2O5与乙醇能发生作用,因反应用量的不同,会生成不同的磷酸酯,它们均为易溶于水的物质,沸点较低。写出乙醇和磷酸反应生成磷酸二乙酯的化学方程式(磷酸用结构式表示为 )__________________________________________________________。
)__________________________________________________________。
(4)某同学认为用上述装置验证产生了乙烯不够严密,理由是___________________。
(5)某同学查文献得知:40%的乙烯利(分子式为C2H6ClO3P)溶液和NaOH固体混和可快速产生水果催熟用的乙烯,请在上述虚线框内画出用乙烯利溶液和NaOH固体制取乙烯的装置简图(夹持仪器略)。













 )
)