-
金属——工业的脊梁。金属及合金广泛应用于生活、生产和航天军工。
资料1:“嫦娥四号”探测器,简称“四号星”,是“嫦娥三号”的备份星。成功着陆月球 背面的“嫦娥四号”探测器使用了多种材料。
(1)探测器使用的铝合金硬度比纯铝的硬度____________ (填“大”或”小”)。
(2)探测器广泛使用了Al、Fe、Cu。利用它们完成如下实验:
①将未打磨的铝片放入 FeSO4 溶液中,没有明显现象;
②将打磨过的铝片放入 FeSO4 溶液中,铝片表面有明显变化;
③将打磨过的铁片放入 CuSO4 溶液中,铁片表面变红。实验①中无现象是因为铝片表面有一层致密的____________ (填化学式)薄膜。 实验③中发生反应的化学方程式为____________ 。
资料 2:人类赖以生存的环境由自然环境和社会环境组成。自然环境由生物圈、岩石圈、大 气圈、水圈组成,其中水圈和岩石圈中含有丰富的镁元素。工业生产中,可用菱镁矿做原料 制备金属镁,流程如图所示:
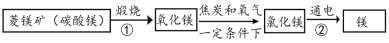
请回答下列问题:
(3)已知反应②中反应物与生成物的化学计量数之比为1:1:1,写出化学方程式为____________。
-
金属﹣工业的脊梁。金属及合金广泛应用于生活、生产和航天军工。
资料:水圈和岩石圈中含有丰富的镁元素。工业生产中,可用菱镁矿做原科制备金属镁,流程如图所示:
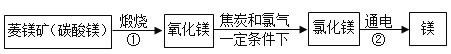
请回答下列问题:
(1)已知①和②属于分解反应,写出②的化学方程式_____。
(2)通过化学反应,以岩石圈的矿石为原料还可以制备很多其他金属,请举一例说明_____(用化学方程式表示其制备原理)。
(3)如图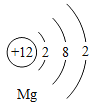 是镁原子结构示意图,镁化学性质活泼,原因是
是镁原子结构示意图,镁化学性质活泼,原因是
-
金属——工业的脊梁
金属及合金广泛应用于生活、生产和航天军工。
资料:水圈和岩石圈中含有丰富的镁元素。工业生产中,可用菱镁矿做原科制'备金属镁,流程如图所示:

请回答下列问题:
(l)已知①和②属于分解反应,化学方程式分别为_________和___________。
(2)通过化学反应,以岩石圈的矿石为原料还可以制备很多其他金属,请举一例说明(用化学方程式表示其制备原理)______________。
(3)下图是镁原子结构示意图,镁化学性质活泼,原因是________。四大圈层中含有下列物质:①硫酸铜;②氯化钠;③硫酸;④氢氧化钙;⑤氧气。其中能和铁反应的物质有(填序号)________。

(4)小梅同学将点燃的镁条伸入盛二氧化碳的集气瓶中,看到镁条剧烈燃烧,发出耀眼白光,瓶壁上有黑色物质生成,她认为这种黑色物质是碳单质。在上述过程中,小梅运用的科学方法有______________。
-
镁是地壳中平均储量丰富的轻金属元素之一,镁合金是目前密度最小的金属结构材料之一,广泛应用于航空航天工业、军工领域、交通领域等.
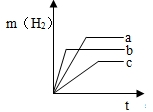
(1)等质量的镁、铝、铁与足量的稀盐酸反应,产生氢气的质量与反应时间的关系如图所示,其中,a是______ (填化学式).
(2)已知镁可以在二氧化硫气体中燃烧,反应的化学方程式:2Mg+SO2 2Mg+S在反应中,______发生氧化反应,该反应的基本类型是:______
2Mg+S在反应中,______发生氧化反应,该反应的基本类型是:______
(3)工业上提炼镁的大致过程如下:
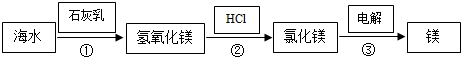
若海水中的镁以氯化镁的形式存在,上述过程①、②的化学方程式依次为:
①______
②______.
-
厉害了,我的国!国人为之骄傲的“嫦娥四号”探测器于2018年12月8日发射成功。燃料、金属材料在火箭发射和日常生产生活中都得到了广泛应用,结合所学化学知识回答下列问题:
(1)三大化石燃料包括:煤、石油和_____,它们都是不可再生能源;
(2)为比较Mn、Pd(钯)、Cu三种金属的活动性顺序,将Mn片、Pd片、Cu片分别加入到稀盐酸中,Mn片表面有气泡产生,Pd片和Cu片没有变化。要确切得出这三种金属的活动性顺序,还需将Pd片加入到_____溶液中,观察现象。
(3)为了解决能源危机,科研工作者们致力于开发新能源,下列属于新能源开发和利用的范畴的是_____(填字母序号)。
A 火力发电 B 风力发电 C 氢燃料客车D 太阳能电池路灯
-
嫦娥四号探测器首次应用多种新型合金材料,根据金属相关知识,回答下列问题。
(1)工业上常用一氧化碳在高温下还原氧化铁来制取铁,其化学反应方程式为______。
(2)实验证明:金属钛在室温时与稀盐酸、稀硫酸都不反应。由此说明钛的金属活动性比铁___(选填“强”或“弱”)。
(3)工业上常用 制备TiO2,则R为___________(填化学式)。
制备TiO2,则R为___________(填化学式)。
(4)已知某些单质与合金的熔点数据如下表所示:
| 单质 | 合金 |
| 铅 | 锡 | 铁 | 硅 | 焊锡(锡、铅) | 硅铁(硅、铁) |
| 熔点/℃ | 327 | 232 | 1535 | 1410 | 183 | 1300 |
根据表中所给数据能得出的结论是________________。
-
铝合金是工业中应用最广泛的一类有色金属结构材料,在航空、航天、汽车、机械制造、 船舶及化学工业中已大量应用。工业经济的飞速发展,对铝合金的需求日益增多,使铝合金的研究也随之深入。已知某铝合金粉末除铝外,还含有铁、铜中的一种或两种。某兴趣小组在老师的指导下,对铝合金粉末中铁、铜的存在情况进行了探究。
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水); Fe、Cu不与氢氧化钠溶液反应。
猜想1:该合金粉末中除铝外,还含有铁。
猜想2:该合金粉末中除铝外,还含有铜。
猜想3:该合金粉末中除铝外,还含有铁、铜。
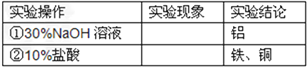
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液。
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的___________,充分反应后过滤,滤渣备用。 | 粉末部分溶解,并有气体放出。 | 合金中一定含有________ 。 |
| ②取步骤①所得滤渣,加过量的___________,充分反应。 | 滤渣部分溶解,并有气体放出,溶液呈浅绿色。 | 合金中一定含有_________ 。 |
【探究结论】猜想 _________成立。
【反思】一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质。写出铝与稀盐酸反应的化学方程式 ___________________。
【拓展与分析】
为了验证铝、铁的金属活动性强弱,小刘同学设计了如下实验方案:把表面积相同的铝丝和铁片同时投入到相同体积的稀盐酸中,比较反应的剧烈程度。请你评价该方案在操作过程中和控制变量上的不足之处。
操作过程中的不足之处___________________。
控制变量上的不足之处________________________。
请你再设计一种不同类型的实验方案,验证铝、铁的金属活动性强弱。________________。
-
铝合金是工业中应用最广泛的一类有色金属结构材料,在航空、航天、汽车、机械制造、船舶及化学工业中已大量应用。工业经济的飞速发展,对铝合金的需求日益增多,使铝合金的研究也随之深入。已知某合金粉末除铝外,还含有铁、铜中的一种或两种。某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究。
查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应。
猜想1:该合金粉末中除铝外,还含有铁。
猜想2:该合金粉末中除铝外,还含有___________(填名称)。
猜想3:该合金粉末中除铝外,还含有铁、铜。
实验探究:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液。
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的_______________,充分反应后过滤,滤渣备用。 | 粉末部分溶解,并有气体放出。 | 合金中一定含有__________。 |
| ②取步骤①所得滤渣,加过量的______________,充分反应。 | 滤渣部分溶解,并有气体放出,溶液呈浅绿色。 | 合金中一定含有__________。 |
探究结论:猜想__________成立。
反思:一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质。写出铝与稀盐酸反应的化学方程式________________________________。
【拓展与分析】
请设计两个不同的实验方案,验证铝、铜的金属活动性强弱。
方案一:__________________。
方案二:_____________。
【总结归纳】由上述实验得出比较金属活动性强弱的方法有:
①_________________;②___________________。
-
我国矿物种类齐全,储量丰富。工业上从从含有金属元素的矿石中提炼金属。其中赤铁矿是炼铁的主要原料。请回答下列问题:
I.铁制品广泛应用于生产、生活中。
(1)铁合金属于________。A.合成材料 B.复合材料 C.金属材料 D.天然材料
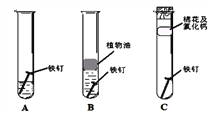
(2)铁钉生锈,属于_____变化(选填“物理”“化学”):下图是探究铁钉在不同条件下发生生锈的实验,其中铁锈蚀最快的是______(选填字母)。
II.赤铁矿(主要成分为Fe2O3)可用于炼铁。
(3)在Fe2O3中,铁、氧元素的质量比为____________。
(4)某钢铁厂每天消耗2000t含Fe2O376%的赤铁矿石,该厂理论上可日产含Fe98%的生铁的质量是________________?(需要写出计算过程计算,结果保留一位小数)
-
我国矿物种类齐全,储量丰富。工业上从从含有金属元素的矿石中提炼金属。其中赤铁矿是炼铁的主要原料。请回答下列问题:
I.铁制品广泛应用于生产、生活中。
(1)下列不属于铁合金的是_____________(选填字母)。
A Fe(OH)3 B 生铁 C不锈钢
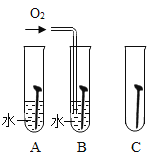
(2)铁钉生锈,属于_____变化(选填“物理”“化学”):右图是探究铁钉在不同条件下发生生锈的实验,其中铁锈蚀最快的是______(选填字母)。
II.赤铁矿(主要成分为Fe2O3)可用于生产催化剂。
(3)在Fe2O3中,氧元素的质量分数为_____________。
(4)赤铁矿经提纯后得到的纯净Fe2O3可用于生产某种工业催化剂(主要成分为FeO和Fe2O3),其反应原理为:2Fe2O3+C 4FeO+CO2↑。现将焦炭和过量的Fe2O3混合均匀,按上述原理充分反应,下图为固体混合物的质量随反应时间的变化曲线。
4FeO+CO2↑。现将焦炭和过量的Fe2O3混合均匀,按上述原理充分反应,下图为固体混合物的质量随反应时间的变化曲线。
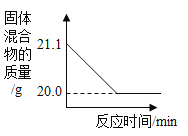
①由图可知:生成CO2气体的质量为_____g。
②反应后固体混合物中FeO的质量分数为_____(请根据化学方程式写出完整的计算步骤)。
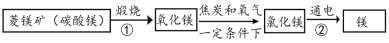

 是镁原子结构示意图,镁化学性质活泼,原因是
是镁原子结构示意图,镁化学性质活泼,原因是






