-
短周期元素 A、B、C、D、E、F 六种元素,它们的原子序数由 A 到 F依次增大。在周期表中,A 的原子半径最小。B 元素的原子最外层电子数是内层电 子数的两倍,C 为地壳中含量最多的元素,D 是原子半径最大的短周期主族元素,D 单质燃烧时呈现黄色火焰,D 的单质在高温下与 C 的单质充分反应,可以得到与 E 单质颜色相同的淡黄色固态化合物。D 与 F 形成的化合物 DF 是常用的调味品。试根 据以上叙述回答:
(1)元素符号:A____________、B____________、C____________、D____________。
(2)E 在元素周期表中的位置:_____________________。
(3)F 离子结构示意图:______________________。
(4)A、B 组成的最简单化合物的名称是_____。
(5)C 、D 按原子个数比 1∶1 组成的一种化合物与水发生反应的化学方程式为_____________________。
(6) 能说明 E 的非金属性比 F 的非金属性_____( 填“强”或“弱”) 的事实是____(举一例)。
高一化学推断题中等难度题查看答案及解析
-
有X、Y、Z、W四种短周期元素,原子序数依次增大。X元素原子的半径最小。Z、W在周期表中处于邻位置,它们的单质在通常状况下均为无色气体。Y原子的最外层电子数是次外层子数的2倍。请回答:
(1)Z2的电子式为___________,YW2的结构式为____________。
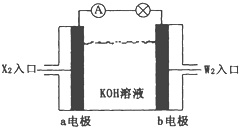
(2)将X2、W2按上图所示通入某燃料电池中,其中,b电极的电极反应式为__________________。若有16gW2参加反应,转移的电子数是____________。
(3)由X、Y、Z、W四种元素组成的无机酸酸式盐_______(化学式),与足量的NaOH溶液在加热条件下反应的离子方程式为________________________________________。
高一化学综合题中等难度题查看答案及解析
-
X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+4、+5、 +7,核电荷数按照Y、Z、X、W的顺序增大.已知Y与Z的原子次外层的电 子数均为2,W、X的原子次外层的电子数为8。
(1)写出各元素的名称:X Y Z W
(2)Y、Z的氢化物更稳定的是 (用化学式表示)
(3)写出Y在元素周期表中的位置:
(4)写出X与Z的最高价氧化物对应水化物反应的化学方程式:
(5)Z元素的气态氢化物和其最高价氧化物对应的水化物的化学反应方程式:
高一化学推断题困难题查看答案及解析
-
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序________。
(2)ZW2的电子式是________。
(3)实验室制备Y的最高价氧化物的水化物的离子方程式是________
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是________
(5)0.1mol的单质W与50mL 1.5mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是________。
高一化学填空题困难题查看答案及解析
-
(12分)X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)写出元素符号:X________ 、Y________、Z________、W________
(2)ZW2的电子式是________,它在常温下呈液态,形成晶体时,属于________晶体。
(3)工业生产单质Y的原理是________(用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是________。
(5)0.1mol的单质W与50mL 1.5mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是________。
高一化学填空题简单题查看答案及解析
-
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序 .
(2)ZW2的电子式是 .
(3)实验室制备Y的最高价氧化物的水化物的离子方程式是
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是
(5)0.1mol的单质W与50mL 1.5mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br﹣的物质的量之比是 .
高一化学推断题困难题查看答案及解析
-
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序 .
(2)ZW2的电子式是 .
(3)实验室制备Y的最高价氧化物的水化物的离子方程式是
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是
(5)0.1mol的单质W与50mL 1.5mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br﹣的物质的量之比是 .
高一化学推断题困难题查看答案及解析
-
有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。已知A和B原子具有相同的电子层数,且A元素的最高正价与最低负价和为零,C是同周期中原子半径最大的元素,D是同周期中离子半径最小的元素。C的单质在加热条件下与B的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物F。试根据以上叙述回答:
(1)D元素在周期表中位置为_____________________;
(2)画出E的离子结构示意图_____________;写出ABE分子的结构式____________;
(3)工业上常用在微波条件下用A单质与EB2反应来解决其产生的环境问题,写出该化学方程式:___________________________________________;
(4)用电子式表示C2E的形成过程__________________________________________;
(5)1 mol F与A元素的最高价氧化物反应时转移的电子数为_________。
高一化学推断题中等难度题查看答案及解析
-
有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。已知A和B原子具有相同的电子层数,且A元素的最高正价与最低负价和为零,C是同周期中原子半径最大的元素,D是同周期中离子半径最小的元素。C的单质在加热条件下与B的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物F。试根据以上叙述回答:
(1)D元素在周期表中位置为_____________________;
(2)画出E的离子结构示意图_____________;写出ABE分子的结构式____________;
(3)工业上常用在微波条件下用A单质与EB2反应来解决其产生的环境问题,写出该化学方程式:___________________________________________;
(4)用电子式表示C2E的形成过程__________________________________________;
(5)1 mol F与A元素的最高价氧化物反应时转移的电子数为_________。
高一化学推断题中等难度题查看答案及解析
-
(13分)有A、B、C、D、E五种短周期元素, 它们的原子序数依次增大。 已知A和B原子具有相同的电子层数, 且A的最外层电子数是次外层电子数的两倍, C是该周期中原子半径最大的元素, C的单质在加热下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物,E与D相邻。 试根据以上叙述回答:
(1)元素名称: A ________ C __________ E________
(2)写出AB2与过量氢氧化钠溶液反应的离子方程式________;
写出 C2B2与AB2反应的化学方程式
________;
(3)画出D的原子结构示意图________,
用电子式表示化合物 C2D 的形成过程________;
(4)D、E的气态氢化物的稳定性________大于________(填化学式)。
高一化学填空题简单题查看答案及解析