-
无水硫酸铜(CuSO4)为白色或灰白色粉末。其水溶液显蓝色,呈弱酸性。可用作杀菌剂和电解精炼铜时的电解液。某化学课外活动小组通过设计硫酸铜受热分解的探究实验,测定气体产物的成分(已知硫酸铜完全分解,固体产物仅含CuO)。实验装置如图所示,回答下列问题
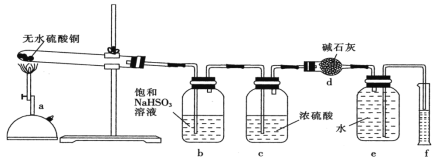
(1)实验前需进行的操作是_________,仪器a的名称是_____,加热时试管外壁必须干燥,要先均匀加热,再集中加热,其目的是__________。
(2)实验结束时根据f中量筒是否收集到水,确定气体产物中有无_______(填化学式)。
(3)装置c的作用是_________。
(4)装置d中的化学方程式为____,_____。有小组成员建议在装置d后增加连接一个干燥管,其原因是_______。
(5)按完善装置的实验结束前后测得相关数据如下:(填化学式)。
| 实验前无水硫酸铜的质量/g | 实验后装置d增加的质量/g | 量筒中水的体积折算成标准状况下气体的体积/mL |
| 6.4 | 2.56 | 224 |
通过计算,写出CuSO4受强热分解的化学方程式:______。
-
下列各种变化中,不属于化学变化的是
A.加热胆矾得到白色的无水硫酸铜粉末
B.电解熔融氧化铝的过程。
C.向沸水中滴入饱和氯化铁溶液,制取氢氧化铁胶体
D.向鸡蛋溶液中滴入饱和硫酸钠溶液,盐析出白色沉淀
-
下列过程属于化学变化的有( )
①白色的硫酸铜粉末久置于空气中变成蓝色
②淀粉遇碘变蓝
③在蜂、蚁蜇咬处涂稀氨水或小苏打溶液可以减轻疼痛
④电解氯化钠溶液.
A.4个
B.3个
C.2个
D.1个
-
硫酸铜是一种常见的无机化合物,可形成CuSO4 .5H2O、CuSO4 .H2O等多种结 晶水合物,它可用作杀菌剂,还可用于电镀和电解精炼铜。冋答下列问题:
(1)CuSO4 .5H2O的俗名是________ 。
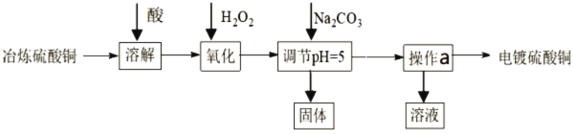
(2)工业利用“冶炼硫酸铜”(主要成分CuSO4含少量Fe2+、AsO2-、Ca2+等杂质)提纯 制备“电镀硫酸铜”(CuSO4 .H2O)的生产流程如下:

溶解所用的酸最适宜的是_____ ,氧化的产物中有比H3AsO4和______,调节pH时生成固体的主要成分除FeAsO4、Fe((OH)) 3外还有______,生成FeAsO4反应的离子方程是________,操作a需经过蒸发浓缩、____、过滤、洗涤、干燥等步骤,其中洗涤的过程中常用无水乙醇,其作用是______________________。
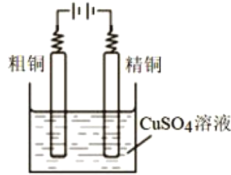
(3)用CuSO4溶液电解精炼铜的装置如图所示,粗铜中含 锌、银、铂杂质,阳极发生的电极反应式_______: 目前世界正在 大力开展用Cu+的络合物作电解质溶液制备纯铜的研究,电解Cu+的 络合物与电解CuSO4溶液相比较,优点是________________,
-
硫酸铜是一种常见的无机化合物,可形成CuSO4 .5H2O、CuSO4 .H2O等多种结 晶水合物,它可用作杀菌剂,还可用于电镀和电解精炼铜。冋答下列问题:
(1)CuSO4 .5H2O的俗名是________ 。
(2)工业利用“冶炼硫酸铜”(主要成分CuSO4含少量Fe2+、AsO2-、Ca2+等杂质)提纯 制备“电镀硫酸铜”(CuSO4 .H2O)的生产流程如下:
溶解所用的酸最适宜的是_____ ,氧化的产物中有比H3AsO4和______,调节pH时生成固体的主要成分除FeAsO4、Fe((OH)) 3外还有______,生成FeAsO4反应的离子方程是________,操作a需经过蒸发浓缩、____、过滤、洗涤、干燥等步骤,其中洗涤的过程中常用无水乙醇,其作用是______________________。
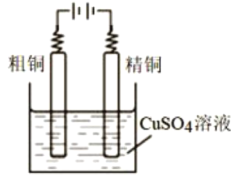
(3)用CuSO4溶液电解精炼铜的装置如图所示,粗铜中含 锌、银、铂杂质,阳极发生的电极反应式_______: 目前世界正在 大力开展用Cu+的络合物作电解质溶液制备纯铜的研究,电解Cu+的 络合物与电解CuSO4溶液相比较,优点是________________,
-
下列变化一定属于化学变化的是 ( )
①铁在空气中缓慢被氧化 ②SO2使品红溶液褪色
③无水硫酸铜由白色粉末变成蓝色品体 ④导电
⑤爆炸 ⑥工业制O2
⑦白磷转化为红磷 ⑧久置浓硝酸变成黄色
A.①②③⑦⑧ B.①②③⑤⑦ C.①③④⑥⑧ D.②③④⑦⑧
-
下列变化一定属于化学变化的是( )
①铁在空气中缓慢被氧化
②SO2使品红溶液褪色
③无水硫酸铜由白色粉末变成蓝色晶体
④导电
⑤爆炸
⑥工业制O2
⑦白磷转化为红磷
⑧久置浓硝酸变成黄色.
A.①②③⑦⑧
B.①②③⑤⑦
C.①③④⑥⑧
D.②③④⑦⑧
-
为证明CuSO4溶液显蓝色与Cu2+离子有关而与SO42-离子无关,某同学设计下列实验,其中对实验目的没有意义的是
①观察硫酸溶液呈无色
②观察硫酸铜粉末呈白色
③稀释CuSO4溶液,溶液变成浅蓝色
④往CuSO4溶液中滴加足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色
⑤往CuSO4溶液中滴加足量Ba(NO3)2溶液,生成白色沉淀,过滤,滤液仍显蓝色
A.只有② B.只有③ C.②和③ D.①②⑤
-
当向蓝色的CuSO4溶液中逐滴加入氨水时,观察到首先生成蓝色沉淀,而后沉淀又逐渐溶解成为深蓝色的溶液,向深蓝色溶液中通入SO2气体,又生成了白色沉淀:将白色沉淀加入稀硫酸中,又生成了红色粉末状固体和SO2气体,同时溶液呈蓝色,根据上述实验现象分析推测,下列描述正确的是( )
A.Cu2+和Ag+相似,能与NH3结合生成铜氨络离子
B.白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解反应
C.白色沉淀为+1价铜的某种亚硫酸盐,在酸性条件下,Cu+只被氧化
D.反应过程中消耗的SO2与生成的SO2的物质的量相等
-
当向蓝色的CuSO4溶液中逐滴加入氨水时,观察到首先生成蓝色沉淀,而后沉淀逐渐溶解成深蓝色溶液,向深蓝色溶液中通入SO2气体,又生成了白色沉淀,将白色沉淀加入稀硫酸中,又生成了红色粉末状固体和SO2,同时溶液呈蓝色。根据实验现象分析推测,下列描述正确的有
A.蓝色沉淀为Cu(OH)2,深蓝色溶液中所含Cu2+浓度较大
B.白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解
C.白色沉淀为+1价铜的某种亚硫酸盐,在酸性条件下发生了自身的氧化还原反应
D.反应过程中消耗的SO2与生成的SO2的物质的量相等




