-
过氧化钙是一种新型的、环境友好的多功能无机化工产品,它是一种非常稳定的过氧化物,常温下干燥不分解,有较强的漂白、杀菌、消毒作用且对环境无污染。下面是某学习小组模拟用大理石(含少量FeO固体)和过氧化氢为原料来制备过氧化钙以及对其含量测定分析过程。
Ⅰ.碳酸钙的制备

1.步骤①加入试剂A的目的是__________。
2.操作②所需要的玻璃仪器_____________。
Ⅱ.过氧化钙制备
制备步骤
(1)将以上制得的碳酸钙置于烧杯中,逐滴加入6mol·L-1的盐酸,直至烧杯中剩余极少量的碳酸钙固体未溶,将溶液加热煮沸,趁热过滤除去未溶的碳酸钙。
(2)另外量取30mL6%的过氧化氢,加入到15ml浓氨水中,将制得的氯化钙溶液和过氧化氢-氨水混合液置于冰水中冷却,观察白色的过氧化钙晶体的生成。
(3)抽滤,用5mL无水乙醇洗涤2~3次,将晶体抽干。
(4)将抽干后的过氧化钙晶体放在表面皿上,于烘箱内在105℃下烘1h,最后取出冷却,称重。
问题讨论
3.步骤(1)中将溶液煮沸的作用是_________。
4.步骤(2)中反应的化学方程式为__________。
5.步骤(3)中将过滤得到的白色晶体,使用乙醇洗涤的目的是_______。
过氧化钙含量的测定
(1)实验步骤
按下面装置图将量气管与水准管用橡皮管连接,量气管上方的三通活塞,使量气管与大气相通,向水准管内注入水,并将水准管上下移动,以除去橡皮管内的空气。

①精确称取0.40g(精确到0.01g)无水过氧化钙加入试管中,转动试管使过氧化钙在试管内均匀铺成薄层。把试管连接到量气管上,塞紧橡皮塞。悬转活塞使量气管通向试管,调整水准管,记下量气管内液面的初读数。
②用小火缓缓加热试管,过氧化钙逐渐分解放出氧气,调整水准管,记下量气管内液面的终读数,并记录实验时的温度和大气压力。计算出产品中过氧化钙的百分含量。
(2)问题讨论
6.写出上述实验中 “调整水准管”的操作__________。
7.若测得氧气的体积为44.8mL(已经折算成标准状况下),则该研究小组制备的过氧化钙的纯度为____。
-
硫酸钠-过氧化氢-氯化钠加合物(xNaSO4·yH2O2·zNaCl)又称固体双氧水,是一种新型精细化工产品,具有漂白、杀菌、消毒等作用。为探究该加合物的组成,某化学兴趣小组设计并进行了如下实验:
第一步:准确称取6.945g样品,配制成250.00ml无色溶液A
第二步:准确量取25.00ml溶液A于锥形瓶中,加适量稀硫酸酸化后,用0.0400mol/LKMnO4标准溶液滴定至终点,消耗溶液KMnO420.00ml
第三步:另取25.00ml溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.932g.
请回答下列问题:
(1)欲配制无色溶液A,所需要的仪器除药匙、分析天平、玻璃棒、胶头滴管外,还应有________。
(2)配平下列离子方程式______MnO4-+_____H2O2+_________=______Mn2++_____O2↑+______。
(3)滴定前,KMnO4标准溶液应盛装于中(填仪器名称),滴定终点现象为________。
(4)第三步能否通过加入AgNO3溶液的方法来测定?为什么
(5)滴定前,滴定管用蒸馏水洗净后,未用KMnO4标准溶液润洗,则Y值______________(填“偏
高 偏低 无影响”)
(6)通过计算确定样品的组成为________。
-
(13分)过氧化钙是一种新型的多功能无机化工产品,常温下是无色或淡黄色粉末,易溶于酸。难溶于水、乙醇等溶剂。某实验小组在实验室用钙盐制取Ca02·8H20沉淀(该反应是一个放热反应)。

(1)仪器X的名称是 。将装置A与B连接后要检查气密性,检查气密性的方法为
(2)仪器B的作用是 。
(3)写出A中发生反应的化学方程式: 。
(4)制取CaO2·8H20一般在0~5℃的低温下进行,原因是 .生成CaO2·8H20的 化学方程式为 。
(5)2.76 g CaO2·8H20样品受热脱水过程的热重曲线(样品质量随温度变化的曲线,140℃时完全脱水,杂质受热不分解)如图所示。
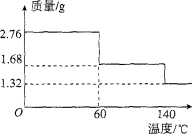
①试确定60℃时CaO2·xH20中x= 。
②该样品中CaO2的质量分数为 。
-
过氧化钙是重要的化工原料,易溶于酸、难溶于水、乙醇等溶剂,温度在350℃以上容易分解。其主要用作杀菌剂、防腐剂、解酸剂、油类漂白剂等。农业上用作种子及谷物的无毒性消毒剂及鱼池的增氧剂。
(1)过氧化钙工业上常用以下合成路线进行合成。
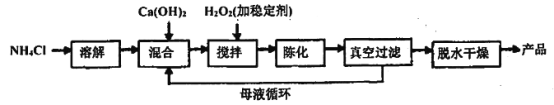
已知:氯化铵的作用是提高Ca2+的浓度。
①反应温度需要控制在常温下产率最高,温度过高或过低都会使产率降低的原因是___________________,母液的主要溶质是__________。
②整个过程的总化学方程式为_____________________________________________。
(2)实验室也可利用反应Ca(s)+O2(g) CaO2(s),在纯氧条件下制取CaO2。其装置示意图如下:
CaO2(s),在纯氧条件下制取CaO2。其装置示意图如下:
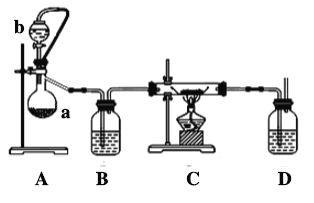
请回答下列问题:
①仪器a的名称为________,仪器a上方橡皮管的作用是______________,D装置中的试剂为________。
②根据完整的实验装置进行实验,实验步骤如下:检验装置的气密性后,装入药品;打开分液漏斗活塞,通入一段时间气体,加热药品;待反应结束后,操作顺序为____________(填序号);拆除装置,取出产物。
a 停止通入氧气并关闭分液漏斗的活塞 b 熄灭酒精灯 c 反应管冷却至室温
(3)利用如图装置测定反应2CaO2 2CaO+O2↑产品中CaO2含量时,停止反应且冷却至25℃后的装置如图所示。A装置中存在的错误是___________,若B装置直接读数确定25℃、1个标准大气压下气体的体积,则测量结果_______(填“偏大”、“偏小”或“无影响”)。
2CaO+O2↑产品中CaO2含量时,停止反应且冷却至25℃后的装置如图所示。A装置中存在的错误是___________,若B装置直接读数确定25℃、1个标准大气压下气体的体积,则测量结果_______(填“偏大”、“偏小”或“无影响”)。

-
过氧化氢(H2O2)俗名双氧水,常温下是一种无色的液体,它难电离,易分解。作为一种经典化工产品,工业上早在一百多年前便开始生产。随着社会需求的增长,尤其是生态环境保护的需要,过氧化氢近年来更受人们的器重,并被称为“绿色氧化剂”。为了储存、运输、使用的方便,工业上采用醇析法将其转化成固态的过碳酸钠晶体(化学式为:2Na2CO3·3H2O2),俗称固体双氧水,该晶体具有Na2CO3和H2O2的双重性,常用作洗涤剂和消毒剂。根据所学化学的相关知识,回答下列问题:
(1)H2O2的电子式______________,该消毒剂的消毒原理与_________相同。
(2)过碳酸钠溶液可以去油污,写出其溶液呈弱碱性离子方程式________________。
(3)该洗涤剂中的有效成分可以将废水中的氰化钠(NaCN)转化为两种无毒的物质,反应的离子方程式为_____。
(4)如果这种洗涤剂在含有铁离子的水中使用,不仅会削弱洗涤剂的去油污的能力,甚至完全失去杀菌作用,结合离子方程式和相应文字表述说明原因___________________。
-
过氧化氢(H2O2)俗称双氧水。是一种重要的化工产品,具有漂白、氧化、消毒、杀菌等多种功效,广泛应用于纺织、造纸、化工、电子、轻工、污水处理等工业。回答下列问题:
(1) H2O2的电子式为_______________。
(2)用H2O2与稀硫酸的混合溶液可溶出印刷电路板金属粉末中的铜。
已知:Cu(s)+2H+ (aq)==Cu2+(aq) + H2(g) ∆H= +64 kJ/mol
2H2O2(1) ==2H2O(l)+O2(g) ∆H =-196 kJmol
H2(g) + l/2O2(g) ==H2O(l) ∆H =-286 kJ/mol
则在稀硫酸溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为:__________________。
(3)工业上常用电解硫酸氢铵水溶液的方法制备过氧化氢,其原理为:首先2NH4HSO4 (NH4)2S2O8+ H2↑,然后由(NH4)2 S2O8水解得到H2O2和另一产物。则:
(NH4)2S2O8+ H2↑,然后由(NH4)2 S2O8水解得到H2O2和另一产物。则:
①电解时阳极的电极反应式为___________________;
②(NH4)2 S2O8水解时发生反应的化学方程式为 ____________________。
(4)现甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素(仅一个条件改变)。甲小组有如下实验设计方案。
| 实验编号 | 温度 | 催化剂 | 浓度 |
| 甲组实验I | 25℃ | 三氧化二铁 | 10mL 5% H2O2 |
| 甲组实验II | 25℃ | 二氧化锰 | 10 mL 5% H2O2 |
甲、乙两小组得出如下图数据。
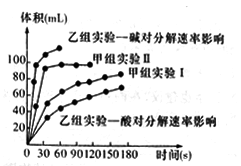
①甲小组实验得出的结论是______________________。
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析,相同条件下H2O2在________(填“酸”或“碱”)性环境下放出气体速率较快;由此,乙组提出可以用BaO2固体与硫酸溶液反应制H2O2,其反应的离子方程式为_______________;支持这一方案的理由是_______________________。
③已知过氧化氢还是一种极弱的二元酸:H2O2 H++HO2-(Ka1=2.4×10-12)。当稀H2O2溶液在碱性环境下分解时会发生反应H2O2+OH-
H++HO2-(Ka1=2.4×10-12)。当稀H2O2溶液在碱性环境下分解时会发生反应H2O2+OH- HO2-+H2O,该反应中,正反应速率为V正=k正•c(H2O2)• c(OH- ),逆反应速率为v逆=k逆•c(H2O) • c(HO2-),其中k正、k逆为速率常数,则k正与k逆的比值为_________(保留3位有效数字)。
HO2-+H2O,该反应中,正反应速率为V正=k正•c(H2O2)• c(OH- ),逆反应速率为v逆=k逆•c(H2O) • c(HO2-),其中k正、k逆为速率常数,则k正与k逆的比值为_________(保留3位有效数字)。
-
近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌于一体的新型高效多功能水处理剂。干燥的高铁酸钾受热易分解,但在198 ℃以下是稳定的。高铁酸钾在水处理过程中涉及的变化过程有( )
①蛋白质的变性 ②蛋白质的盐析 ③胶体聚沉 ④盐类水解 ⑤焰色反应 ⑥氧化还原反应
A. ①②③④ B. ①③④⑥
C. ②③④⑤ D. ②③⑤⑥
-
近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌于一体的新型高效多功能水处理剂,干燥的高铁酸钾在198 ℃以下是稳定的,受热易分解。高铁酸钾在水处理过程中涉及的变化过程有( )
①蛋白质的变性②蛋白质的盐析③胶体聚沉④盐类水解
⑤焰色反应⑥氧化还原反应
A.①②③④ B.①③④⑥ C.②③④⑤ D.②③⑤⑥
-
近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌于一体的新型高效多功能水处理剂,干燥的高铁酸钾在198 ℃以下是稳定的,受热易分解。高铁酸钾在水处理过程中涉及的变化过程有
①蛋白质的变性 ②蛋白质的盐析 ③胶体聚沉 ④盐类水解 ⑤焰色反应 ⑥氧化还原反应
A. ①②③④ B. ①③④⑥
C. ②③④⑤ D. ②③⑤⑥
-
近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面。高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌于一体的新型高效多功能水处理剂。干燥的高铁酸钾受热易分解,在198℃以下是稳定的。高铁酸钾在水处理过程中涉及的变化过程有( )
①蛋白质的变性 ②蛋白质的盐析 ③胶体聚沉 ④盐类水解 ⑤焰色反应 ⑥氧化还原反应
A.①②③④ B.①③④⑥ C.②③④⑤ D.②③⑤⑥







