-
在恒温恒压下,向体积为2 L密闭容器中充入4mol SO2和2mol O2,发生如下反应:2SO2(g)+O2(g)⇌2SO3(g)△H<0。2min后,反应达到平衡,生成SO3为2mol。
求:(1)0~2 min内v(SO3)______________?
(2)平衡后容器中SO2的浓度_____________?
(3)在此温度下该反应的平衡常数______________?
-
在恒温恒压下,向密闭容器中充入4mol SO2和2mol O2,发生反应2SO2(g)+O2(g) 2SO3(g) ΔH<0。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量Q kJ。则下列分析正确的是( )
2SO3(g) ΔH<0。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量Q kJ。则下列分析正确的是( )
A.在该条件下,反应前后的压强之比为6∶5.3
B.若反应开始时容器体积为2L,则v(SO3)=0.35mol·L-1·min-1
C.若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4mol
D.若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量大于Q kJ
-
在恒温恒压下,向体积为2 L密闭容器中充入4mol SO2和2mol O2,生如下反应:2SO2(g)+O2(g)⇌2SO3(g)△H<0。2min后,反应达到平衡,生成SO3为2mol。则0~2 min内v(SO3)__________________,平衡后容器中SO2的浓度________________,SO2的转化率为___________________,在此温度下该反应的平衡常数____________________________。
-
恒温下,将a mol O2与bmol SO2的混合气体通入一个固定容积的密闭容器中,发生如下反应:O2(g) + 2SO2(g) 2SO3(g)
2SO3(g)
(一)①若反应达平衡时,n(O2) = 4mol,n(SO3) = 4mol,计算a的值为____。
②平衡时总体积在标准状况为313.6L,原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始)∶n(平) =____。
③达到平衡时,O2和SO2的转化率之比,α(O2)∶α (SO2)=____。
(二)若起始将6mol O2、b mol SO2和1 molSO3通入上反应容器中,起始反应向正方向进行,使反应达到平衡时容器中气体的物质的量为12mol。则b的取值范围是____。
-
(8分)在537℃、101KPa 时,往容积可变的密闭容器中充入2mol SO2、 1mol O2,此时容器的体积为200L。向容器中加入催化剂(固体)并保持恒温恒压,发生反应:2SO2(g)+O2(g) 2SO3(g)达到平衡时,平衡气体中SO3的体积分数为91%。试回答下列问题:
2SO3(g)达到平衡时,平衡气体中SO3的体积分数为91%。试回答下列问题:
(1)保持上述温度和压强不变,若向容器中只充入2mol SO3并加入固体催化剂。则平衡时,SO2的体积分数是________,容器的体积为________L。
(2)若温度和容器的容积不变,则平衡时的容器内气体的压强为________KPa。
(3)温度仍保持537℃,容器体积保持200L不变(恒容)。充入a molSO2、b molO2,并加入固体催化剂,反应达平衡时,SO3的体积分数仍为0.91,体系压强为101KPa。若a:b=2:1,则a=________。
-
恒温恒容的密闭容器中盛有2mol SO3,发生反应2SO3(g)  2SO2(g)+O2(g),一定条件下平衡时SO2所占的体积百分数为M,若相同条件相同容器中,最初放入4 mol SO3,则平衡时,SO2的体积百分数为N,下列结论正确的是
2SO2(g)+O2(g),一定条件下平衡时SO2所占的体积百分数为M,若相同条件相同容器中,最初放入4 mol SO3,则平衡时,SO2的体积百分数为N,下列结论正确的是
A.M=N B.M>N C.M<N D.无法比较
-
将4mol SO2与2mol O2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2(g)+O2(g)⇌2SO3(g),测得平衡时混合物总的物质的量为5mol,求:
(1)平衡时SO3的浓度;
(2)平衡时SO2的转化率.
-
将4mol SO2与2mol O2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2(g)+O2(g)⇌2SO3(g),测得平衡时混合物总的物质的量为5mol,求:
(1)平衡时SO3的浓度;
(2)平衡时SO2的转化率.
-
已知体积为2L的恒容密闭容器中发生反应:2SO2(g) + O2(g) 2SO3(g),请根据化学反应的有关原理同答下列问题
2SO3(g),请根据化学反应的有关原理同答下列问题
(1)一定条件下,充入2mol SO2(g)和2mol O2(g),20s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速 率为_____________________。
率为_____________________。
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号)___________。
①混合气体的密度不变 ②混合气体的平均相对分子质量不变
③ v正(SO2)=2v正(O2) ④各气体的浓度都不再发生变化
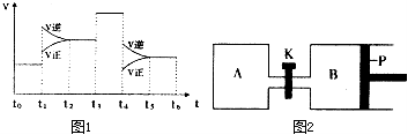
(3)图1表示该反应的速率(v)随时间(t)的变化的关系.则下列不同时间段中,SO3 的百分含量最高的是( )
A、t2→t3 B、t0→t1 C、t5→t6 D、t3→t4
据图分析:你认为t3时改变的外界条件可能是__________;
(4)图2中P是可自由平行滑动的活塞.在相同温度时,向A容器中充入4mol SO3(g),关闭K,向B容器中充入2mol SO3(g),两容器分别发生反应.已知起始时容器A和B的体积均为aL。试回答:
①反应达到平衡时容器B的体 积
积 为1.2a L,容器B中SO3转化率为___________。
为1.2a L,容器B中SO3转化率为___________。
②若打开K,一段时间后重新达到平衡,容器B的体积为___________L(连通管中气体体积忽略不计,且不考虑温度的影响)。
-
在温度不变的条件下,恒容密闭容器中发生如下反应2SO2(g)+O2(g)⇌2SO3(g),下列叙述能够说明反应已经达到平衡状态的是( )
A.容器中SO2、O2、SO3共存
B.单位时间内生成2mol SO2的同时消耗2mol SO3
C.容器中SO2、O2、SO3的物质的量之比为1:1:1
D.反应容器中压强不随时间变化
2SO3(g) ΔH<0。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量Q kJ。则下列分析正确的是( )
