-
硫酸铁铵[NH4Fe(SO4)2▪xH2O]是一种重要铁盐,能在水中解离出NH4+、Fe3+、SO42-。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流 程如下:
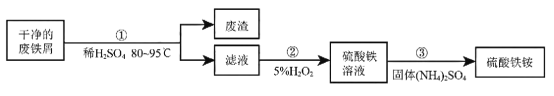
回答下列问题:
(1)步骤①发生反应的方程式是_____________。经检验,废渣是片状石墨,它与金刚石的物理性质有很大差异的原因是___________________。
(2)完成步骤②中的反应2FeSO4+H2O2+____________=Fe2(SO4)3+ 2H2O
(3)如废铁屑表面已生锈(铁锈的主要成分为Fe2O3▪xH2O),则步骤①还会发生另外两步反应:
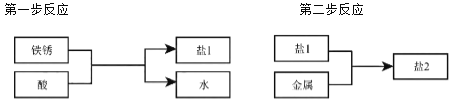
第二步反应中反应物与生成物的化学计量数之比为1:1:3,写出第二步反应的化学方程式: _____ 。
(4)由该实验可知,干净的表面未生锈的废铁屑属于________ (填“纯净物”或“混合物”)。
(5)将步骤③中得到的样品经干燥后加热,失掉全部结晶水,剩余固体的质量为原晶体质量的55.2%,则硫酸铁铵晶体的化学式为_______ (填序号)。
a. NH4Fe(SO4)2▪3H2O
b. NH4FeSO4)▪6 H2O
c. NH4Fe(SO4)2▪9 H2O
d. NH4FeSO4)▪12 H2O
(6)完成鉴别硫酸铁和硫酸铁铵两种固体的实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
| _____ | _____ | _____ |
-
硫酸铁铵[NH4Fe(SO4)2]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如图。请根据流程图回答下列问题。

(1)步骤③的化学方程式为 ,在这个化学变化过程中,化合价发生改变的元素为:_____。
,在这个化学变化过程中,化合价发生改变的元素为:_____。
(2)步骤④发生化合反应,写出该反应的化学方程式_____。
(3)步骤①会产生有毒的SO2,图中最适合吸收SO2防止造成空气污染的装置是_____。
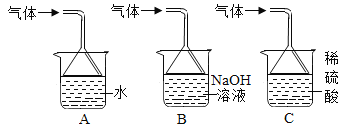
-
用工业废铁屑(含有油污)生产 NH4Fe(SO4)2·xH2O 的主要流程如下:
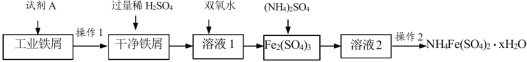
(1)加入试剂 A 的目的是除去油污。试剂 A 可以选择_______(选填序号)。
a Na2CO3 b 洗洁精 c 稀盐酸
(2)稀硫酸加入后应维持温度在 80℃~95℃之间,目的是_______。
(3)加入双氧水后反应方程式为_________。操作 2 包括:蒸发浓缩、_________、过滤、洗涤等。
-
硫酸铝铵晶体(NH4Al(SO4)2·xH2O)是一种用途广泛的含铝化合物。兴趣小组在科研人员指导下,设计实验研究硫酸铝铵晶体受热分解的产物。
(查阅资料)①SO2可与稀KMnO4溶液反应使其褪色。
②SO3+H2O=H2SO4。
③硫酸铝铵热分解可得到纳米氧化铝。
④碱石灰是CaO和NaOH的混合物。
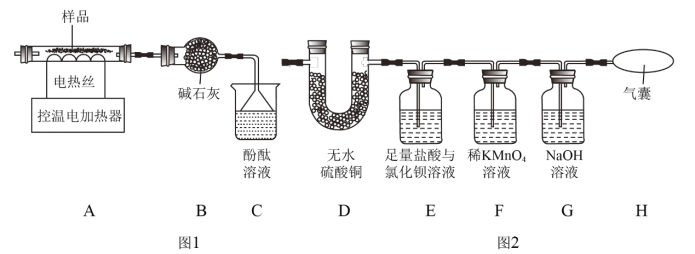
(1)硫酸铝铵晶体分解产物的定性探究
①装置C中观察到酚酞溶液变红色,由此可知分解的产物中有_____(写化学式)。
②某同学认为硫酸铝铵晶体受热分解的产物中还有H2O、SO2、SO3和N2。为进行验证,用图1中的装置A和图2所示装置连接进行实验。实验中,装置D中现象是_____,证明有H2O生成;装置E中现象是_____,证明有SO3生成;而装置F中现象是_____、H最终没有胀大,证明没有SO2和N2生成。
(2)硫酸铝铵晶体成分及分解产物的定量探究为确定硫酸铝铵晶体的组成,称取45.3g样品在空气中持续加热,测定剩余固体质量随温度变化的曲线如图所示。
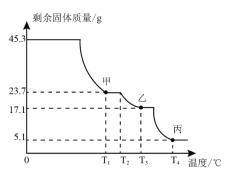
①固体甲是T1℃刚好完全失去结晶水的产物,则x=_____。
②T3℃时固体乙的成分是_____(填字母)。
A Al2(SO4)3
B Al(OH)3
C Al2(SO4)3和Al(OH)3
-
(2009•南充)解离(又叫电离)时生成的阳离子全部是H+的化合物叫做酸.例如硫酸的解离可表示为:H2SO4→2H++SO42-.根据下列四种物质的解离:HBr→H++Br-;HClO4→H++ClO4-;NaHSO4→Na++H++SO42-;CH3COOH→H++CH3COO-,其中不属于酸的是( )
| A.HBr | B.HClO4 | C.NaHSO4 | D.CH3COOH |
-
解离(又叫电离)时生成的阳离子全部是H+的化合物叫做酸.例如硫酸的解离可表示为:H2SO4→2H++SO42-.根据下列四种物质的解离:HBr→H++Br-;HClO4→H++ClO4-;NaHSO4→Na++H++SO42-;CH3COOH→H++CH3COO-,其中不属于酸的是( )
A.HBr
B.HClO4
C.NaHSO4
D.CH3COOH
-
解离(又叫电离)时生成的阳离子全部是H+的化合物叫做酸。例如硫酸的解离可表示为:H2SO4→2H++SO42-.根据下列四种物质的解离:H2S→2H++S2-;HClO4→H++ClO4-;NaHSO4→Na++H++SO42-;CH3COOH→H++CH3COO-,其中不属于酸的是( )
A.  B.
B.  C.
C.  D.
D. 
-
硫酸铝铵晶体制取的探究
硫酸铝铵是一种用途广泛的含铝化合物。以某铝土矿(主要成分Al2O3,含少量SiO2、Fe2O3杂质)为原料制硫酸铝铵晶体((NH4)aAlb(SO4)c•xH2O)的流程如下:
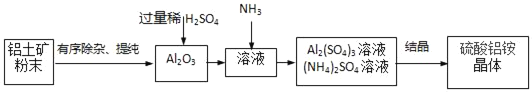
有关上述流程的说法正确的是_____。
a“有序除杂、提纯”中有先加过量稀盐酸再过滤,该做法的目的是除去SiO2
b稀硫酸过量的目的只是保证Al2O3溶解完全
-
已知明矾[KAl(SO4)2•12H2O]在水中可解离出K+、Al3+和SO42-,某学习小组为探究明矾中何种离子起净水作用,做如下实验,请你完成实验报告:
| 实验操作 | 实验现象 | 结论 |
| 在一杯浑浊的水中加少量Al2(SO4)3,静置 | ______ | Al2(SO4)3起净水作用 |
| 在一杯浑浊的水中加少量KCl,静置 | 烧杯中的水仍然浑浊 | ______ |
有同学认为以上方案中只是证明了Al2(SO4)3可以净水,K+没有净水作用,但Al3+和SO42-能否净水,不够完善.请你仔细分析以上实验报告并将你完善实验所用的试剂及目的填入下表中:
-
已知明矾的化学式为[K2SO4•Al2(SO4)3•24H2O]是农村常用的一种净水剂,它在水中能解离出自由移动的K+、Al3+、SO42-,甲同学为了探究明矾中哪种离子具有净水作用,设计了如下探究实验,请填写下表中的空白:
| 实验步骤 | 实验现象 | 结论 |
| 在一杯浑浊的水中加少量氯化钾,搅拌后静置 | 烧杯中的水仍然浑浊 | ________ |
| 在一杯浑浊的水中加少量硫酸铝,搅拌后静置 | 烧杯中的水变澄清 | ________ |
| 在一杯浑浊的水中加少量氯化铝,搅拌后静置 | ________ | 氯化铝能净水 |
根据上述实验方案你认为明矾中有净水作用的离子是________(写符号)
乙同学看到甲的方案后,认为该方案还不完善,他对甲同学的方案进行了补充完善.请你把乙同学补充的方案中要达到的目的和所使用的试剂填入下表:
| 实验目的 | 使用的试剂 |
| ________ | ________ |







