用工业废铁屑(含有油污)生产 NH4Fe(SO4)2·xH2O 的主要流程如下:
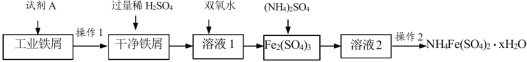
(1)加入试剂 A 的目的是除去油污。试剂 A 可以选择_______(选填序号)。
a Na2CO3 b 洗洁精 c 稀盐酸
(2)稀硫酸加入后应维持温度在 80℃~95℃之间,目的是_______。
(3)加入双氧水后反应方程式为_________。操作 2 包括:蒸发浓缩、_________、过滤、洗涤等。
九年级化学流程题中等难度题
用工业废铁屑(含有油污)生产 NH4Fe(SO4)2·xH2O 的主要流程如下:

(1)加入试剂 A 的目的是除去油污。试剂 A 可以选择_______(选填序号)。
a Na2CO3 b 洗洁精 c 稀盐酸
(2)稀硫酸加入后应维持温度在 80℃~95℃之间,目的是_______。
(3)加入双氧水后反应方程式为_________。操作 2 包括:蒸发浓缩、_________、过滤、洗涤等。
九年级化学流程题中等难度题
用工业废铁屑(含有油污)生产 NH4Fe(SO4)2·xH2O 的主要流程如下:

(1)加入试剂 A 的目的是除去油污。试剂 A 可以选择_______(选填序号)。
a Na2CO3 b 洗洁精 c 稀盐酸
(2)稀硫酸加入后应维持温度在 80℃~95℃之间,目的是_______。
(3)加入双氧水后反应方程式为_________。操作 2 包括:蒸发浓缩、_________、过滤、洗涤等。
九年级化学流程题中等难度题查看答案及解析
用工业碳酸钙(含有少量Al2O3、Fe2O3)生产医药CaCl2•2H2O的主要流程如下:

(1)加入试剂A的目的是除去溶液1中少量AlCl3、FeCl3 . 试剂A可以选择________ (选填序号).
a.Na2CO3 b.Ba(OH)2 c.Ca(OH)2
(2)阶段一的目的是________ .
(3)操作1、2中,所用玻璃仪器有________、玻璃棒、烧杯、胶头滴管.操作3包括:蒸发浓缩、________、过滤、洗涤等.
九年级化学流程题简单题查看答案及解析
硫酸铁铵[NH4Fe(SO4)2▪xH2O]是一种重要铁盐,能在水中解离出NH4+、Fe3+、SO42-。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流 程如下:
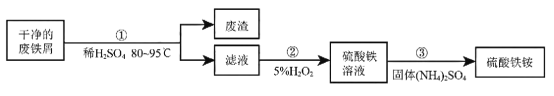
回答下列问题:
(1)步骤①发生反应的方程式是_____________。经检验,废渣是片状石墨,它与金刚石的物理性质有很大差异的原因是___________________。
(2)完成步骤②中的反应2FeSO4+H2O2+____________=Fe2(SO4)3+ 2H2O
(3)如废铁屑表面已生锈(铁锈的主要成分为Fe2O3▪xH2O),则步骤①还会发生另外两步反应:
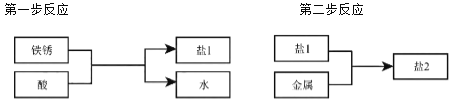
第二步反应中反应物与生成物的化学计量数之比为1:1:3,写出第二步反应的化学方程式: _____ 。
(4)由该实验可知,干净的表面未生锈的废铁屑属于________ (填“纯净物”或“混合物”)。
(5)将步骤③中得到的样品经干燥后加热,失掉全部结晶水,剩余固体的质量为原晶体质量的55.2%,则硫酸铁铵晶体的化学式为_______ (填序号)。
a. NH4Fe(SO4)2▪3H2O
b. NH4FeSO4)▪6 H2O
c. NH4Fe(SO4)2▪9 H2O
d. NH4FeSO4)▪12 H2O
(6)完成鉴别硫酸铁和硫酸铁铵两种固体的实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
| _____ | _____ | _____ |
九年级化学流程题困难题查看答案及解析
碱式碳酸铜可用于生产木材防腐剂等。工业上可用微蚀刻废液(含有一定量Cu2+、H+、SO42-、H2O2和微量Fe3+)制备高纯度碱式碳酸铜,其制备过程如下:
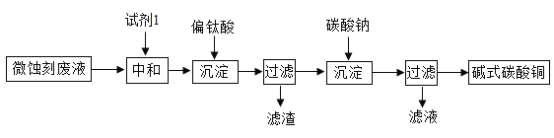
(1)加入试剂1的目的是除去废液中的酸性物质,试剂1最好选用__________(填序号)。
aFe2O3bCaCO3cCuO
(2)加入Na2CO3沉淀前须除去Fe3+,否则Fe2(SO4)3会与Na2CO3反应,产生一种气体,同时生成NaFe3(OH)6(SO4)2沉淀,影响产品质量,反应的化学方程式为:6Na2CO3+3Fe2(SO4)3+6H2O=2NaFe3(OH)6(SO4)2+6CO2↑+5__________ 。
(3)加入Na2CO3沉淀时,反应液pH对产品中的SO42- 含量以及反应液中Cu2+沉淀效率的影响如下图所示,第二次沉淀时溶液pH最好控制在_________。
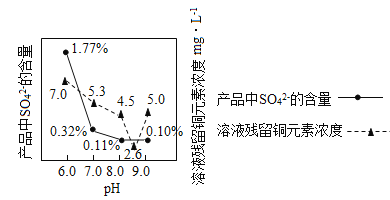
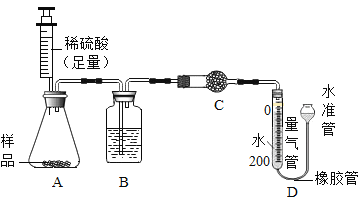
(4)所制得的碱式碳酸铜的组成可表示为:xCuCO3·yCu(OH)2·zH2O。某研究小组设计如图实验装置测定其中CuCO3的质量分数(不考虑植物油中溶解CO2产生的影响)。
实验步骤如下:
a.连接装置并________;
b.准确称量样品的质量1.2g;
c.装药品,调节量气装置两边液面相平,读取量气管刻度为10mL;
d.向锥形瓶内加入50mL(足量)的稀硫酸,充分反应;
e.冷却到室温;
f.再次调节量气装置两边液面相平,读取量气管刻度为172mL。
①请将上述实验步骤补充完整;
②装置B的作用是 _________,C中的试剂是 _____________(填字母序号);
a碱石灰 b浓硫酸 c无水硫酸铜
③步骤f中调节液面相平的操作是将水准管 _____________(填“缓慢上移”或“缓慢下移”)。
④若标准状况下,每44g二氧化碳的体积为22.4L。根据实验数据计算产品中CuCO3的质量分数_______(写出计算过程。结果保留到0.1%)
⑤若其他操作均正确,仅因下列因素可使测定结果偏小的是_______________(填字母序号);
A量气管中未加植物油 B步骤c中平视刻度,步骤f中俯视读数
C硫酸的用量不足 D步骤f中没有调节量气装置两边液面相平,直接读数
九年级化学流程题困难题查看答案及解析
(11分)医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙为原料(含量为97.5%,含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙的主要流程如下:
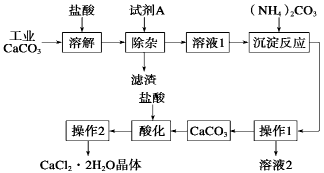
(1)除杂操作时加入试剂A,调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+。试剂A是Ca(OH)2,还可以选择 。
a.NaOH b.NH3 c.Na2CO3
(2)请指出下列操作的名称:操作1 ;操作2蒸发浓缩、 ;操作1中所用的玻璃仪器有漏斗、玻璃棒、 。
(3)酸化操作是加入过量盐酸,调节溶液的pH为4.0,目的之一是为了将少量的 转化为CaCl2。
(4)写出加入碳酸铵所发生的反应的方程式: +(NH4)2CO3=CaCO3↓+2NH4Cl
写出溶液2的一种用途 。
(5)测定样制得品中Cl-含量的方法是:称1.5g样品,溶解,滴加过量的 AgNO3 溶液,过滤、洗涤、干燥,称得沉淀质量为2.87g,证明沉淀洗净的标准是:取最后一次洗涤的滤液,滴加 试剂,若 现象,则已经洗净。
(6)计算上述样品中CaCl2·2H2O的质量分数为: 。若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有: 。
九年级化学填空题中等难度题查看答案及解析


九年级化学填空题中等难度题查看答案及解析
将CuSO4和Na2SO4的固体混合物进行分离主要流程如下:
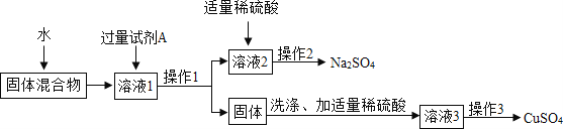
(1)加试剂A的目的是将CuSO4转化为沉淀。试剂A可以选择_____溶液(填序号)。
a.BaCl2 b.NaOH c.Ca(OH)2
则加入试剂A后,发生化学反应的方程式为_____。
(2)操作1所用玻璃仪器有_____、玻璃棒、烧杯。
(3)控制溶液2中所加稀硫酸为适量的方法是_____(填序号)。
a.溶液2中预先滴入石蕊 b.加入稀硫酸时用传感器测溶液pH
(4)操作1之后所得固体表面的杂质除了Na2SO4之外,还含有_____,确认固体被洗净的操作是:向最后一次洗涤后的滤液中滴入_____溶液,若无现象,则证明固体已被洗净。
九年级化学流程题中等难度题查看答案及解析
(8分)Na2SO4是制造纸张、药品、染料稀释剂的重要原料。某Na2SO4样品中含有少量CaCl2和MgCl2,实验室提纯Na2SO4的流程如下图所示。
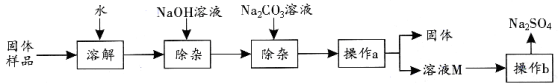
(1)加入NaOH溶液主要除去的阳离子是 (填离子符号),其反应的化学方程式为 。
(2)若加入的NaOH溶液和Na2CO3溶液都过量,可在后续的流程中加入适量的 (填名称)除去。
(3)操作a的名称是 ,该操作中需要用到的玻璃仪器有烧杯、玻璃棒、 。
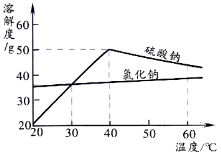
(4)若溶液M中的溶质是Na2SO4和NaCl,根据下图的溶解度曲线可知,操作b应为:先将溶液M ,再降温结晶、过滤。降温结晶的最佳温度范围是 ℃以下,这是因为 。
九年级化学填空题中等难度题查看答案及解析
利用海水晒盐的工业流程主要如下:
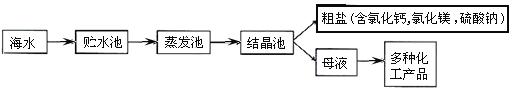
[提出问题]
怎样将析出的粗盐中含有CaCl2、MgCl2和Na2SO4都除去?
[设计实验]
方案一:工业上利用某种饱和溶液浸洗上述杂质的方法,这种饱和溶液是①________饱和溶液;
方案二:在实验室中,有人设计如下实验流程:
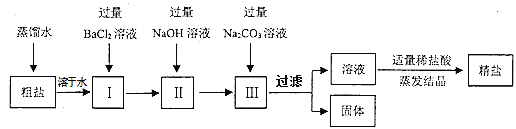
在上述方案中:
(1)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是②__________;
(2)上述流程中,过滤出的固体成分是③__________________(写化学式);
[反思交流]
(1)通过粗盐的成分可知,其中含有Cl—和SO42-,你证明这两种混合离子的方法是:将粗盐溶于水,配成溶液,然后④__________;
(2)通过上述方法,总结检验混合离子的方法是:先选试剂,后排顺序。这里的排顺序原则是指⑤_______________;
[拓展应用]
工业上得到精盐后,用给氯化钠水溶液通电的方法制取火碱,同时还生成两种气体单质,这两种单质化合后的生成物溶于水又能得到盐酸。写出给氯化钠水溶液通电的化学方程式⑥_____________
九年级化学流程题简单题查看答案及解析
利用海水晒盐的工业流程主要如下:
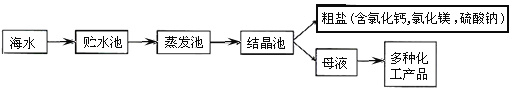
[提出问题]
怎样将析出的粗盐中含有CaCl2、MgCl2和Na2SO4都除去?
[设计实验]
方案一:工业上利用某种饱和溶液浸洗上述杂质的方法,这种饱和溶液是①________饱和溶液;
方案二:在实验室中,有人设计如下实验流程:
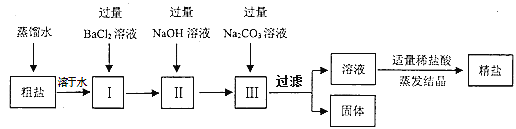
在上述方案中:
(1)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是②__________;
(2)上述流程中,过滤出的固体成分是③__________________(写化学式);
[反思交流]
(1)通过粗盐的成分可知,其中含有Cl—和SO42-,你证明这两种混合离子的方法是:将粗盐溶于水,配成溶液,然后④__________;
(2)通过上述方法,总结检验混合离子的方法是:先选试剂,后排顺序。这里的排顺序原则是指⑤_______________;
[拓展应用]
工业上得到精盐后,用给氯化钠水溶液通电的方法制取火碱,同时还生成两种气体单质,这两种单质化合后的生成物溶于水又能得到盐酸。写出给氯化钠水溶液通电的化学方程式⑥_____________
九年级化学流程题简单题查看答案及解析