
A.t1~t2速度变化的主要原因是反应放热使溶液温度升高
B.t1~t2速度变化的主要原因是反应物的量较多
C.t2~t3速度变化的主要原因是压强逐渐减小
D.t2时恰好完全反应
九年级化学选择题中等难度题

九年级化学选择题中等难度题

九年级化学选择题中等难度题查看答案及解析
已知升温、提高浓度、加大压强和使用催化剂均可以提高化学反应的速率。潘瑞同学发现把除去氧化膜的镁条投入盛有稀盐酸的试管中,试管外壁用手一摸感到发烫,而且产生氢气的速率变化情况和反应进行的时间的关系如右图所示, 则下列关于速率变化的主要原因说法正确的是:
A.t1~t2速度变化的主要原因是反应放热使溶液温度升高
B.t1~t2速度变化的主要原因是反应物的量较多
C.t2~t3速度变化的主要原因是盐酸的浓度逐渐减小
D.t2时恰好完全反应
九年级化学选择题中等难度题查看答案及解析
已知升温、提高浓度、加大压强和使用催化剂均可以提高化学反应的速率。潘瑞同学发现把除去氧化膜的镁条投入盛有稀盐酸的试管中,试管外壁用手一摸感到发烫,而且产生氢气的速率变化情况和反应进行的时间的关系如右图所示, 则下列关于速率变化的主要原因说法正确的是:
A.t1~t2速度变化的主要原因是反应放热使溶液温度升高
B.t1~t2速度变化的主要原因是反应物的量较多
C.t2~t3速度变化的主要原因是盐酸的浓度逐渐减小
D.t2时恰好完全反应
九年级化学选择题中等难度题查看答案及解析
已知升温、提高浓度、加大压强和使用催化剂均可以提高化学反应的速率。潘瑞同学发现把除去氧化膜的镁条投入盛有稀盐酸的试管中,试管外壁用手一摸感到发烫,而且产生氢气的速率变化情况和反应进行的时间的关系如右图所示, 则下列关于速率变化的主要原因说法正确的是:
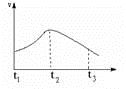
A. t1~t2速度变化的主要原因是反应放热使溶液温度升高
B. t1~t2速度变化的主要原因是反应物的量较多
C. t2~t3速度变化的主要原因是盐酸的浓度逐渐减小
D. t2时恰好完全反应
九年级化学单选题中等难度题查看答案及解析
已知升温、提高浓度、加大圧强和使用催化剂均可以提高化学反立的速率.现把除去氧化膜的镁条投入盛有稀盐酸的试管中,试管外壁用手摸感到发烫,而且生成氢气的速率变化情况和反应进行的吋间的关系如右图所示,则下列说法不正确的是( )
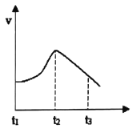
A. 反应过程中溶液的pH逐渐増大
B. t1-t2速度变化的主要原因是反应放出的热量使溶液温度升高
C. t2-t3速度变化的主要原因是盐酸的浓度逐渐减小
D. t2时恰好完全反应
九年级化学单选题简单题查看答案及解析
升温、增大浓度、加大压强和使用催化剂均可以提高化学反应速率。现把镁条投入盛有稀盐酸的试管中,试管外璧发烫。产生氢气的速率变化情况(v)和反应进行的时间(t) 的关系如图所示,则下列说法错误的是( )
A. 反应过程中溶液的pH逐渐增大 B. t1~t2速率变化的主要原因是反应物的量较多
C. t2~t3速率变化的主要原因是盐酸的浓度逐渐减小 D. t1~t2速率变化的主要原因是反应放热使溶液温度升高
九年级化学单选题困难题查看答案及解析
升温、增大浓度、加大压强和使用催化剂均可以提高化学反应速率。现把镁条投入盛有稀盐酸的试管中,试管外璧发烫。产生氢气的速率变化情况(v)和反应进行的时间(t) 的关系如图所示,则下列说法错误的是( )
A. 反应过程中溶液的pH逐渐增大 B. t1~t2速率变化的主要原因是反应物的量较多
C. t2~t3速率变化的主要原因是盐酸的浓度逐渐减小 D. t1~t2速率变化的主要原因是反应放热使溶液温度升高
九年级化学单选题困难题查看答案及解析
将一段去除氧化镁的镁条放入一定量的盐酸中,有气泡产生,充分反应后静置,发现试管中有白色沉淀产生。为探究白色沉淀的成分,9 (1)班兴趣小组同学在老师的指导下进行如下实验:
| 试管(盛有等体积等浓度的盐酸) | ① | ② | ③ | ④ |
| 镁条质量(g) | 1 | 1.5 | 2 | 2.5 |
| 实验现象 | 快速反应,试管发热,镁条全部消失 | |||
| 白色沉淀量(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
(1)4支试管中盛有等体积等浓度的盐酸的原因________________。
(得出结论)(2)镁条与盐酸反应产生白色沉淀的量与________________有关。
(提出问题)白色沉淀是什么物质?
(查阅资料)在氯化镁溶液中,镁能与水常温下反应生成氢氧化镁和氢气。
(猜想与假设)
甲:白色沉淀可能是碳酸镁
乙:白色沉淀可能是生成的氯化镁增多析出的晶体
丙:白色沉淀可能是剩余的镁
丁:白色沉淀可能是氢氧化镁
(3)其他同学认为甲的猜想是错误的,原因是________________
(实验验证)
| 序号 | 操作步骤 | 实验现象 | 结论 |
| 1 | 取第一份白色不溶物于试管中,加入蒸馏水,震荡 | (4)沉淀________________溶解(选填会或不会) | 乙同学猜想不成立 |
| 2 | 取第二份白色不溶物于试管中,加入稀盐酸 | (5)________________ | 丙同学猜想不成立 |
| 3 | ①取第三份白色不溶物于试管中,加入稀硝酸 ②向所得溶液加入几滴硝酸银溶液 | ①白色沉淀不溶解 ②出现大量白色沉淀 | ①丁同学猜想不成立 ②白色不溶物一定含(6)________________元素 |
(7)在老师的帮助下,同学们得出白色沉淀物是Mg2(OH)2Cl2反应的化学方程式为2Mg+2HCl+2H2O=Mg2(OH)2Cl2+2X则X为________________。
(拓展延伸)
小钢同学认为上述实验验证3的设计不严密,在实验验证3之前应该对不溶物进行洗涤,目的是________________。
九年级化学实验题中等难度题查看答案及解析
某课外活动小组就催化剂对化学反应速率的影响进行了有关探究,已知二氧化锰可作为过氧化氢分解产生氧气的催化剂。同学在用过氧化氢溶液与二氧化锰制取氧气的过程中,发现反应的速率慢,产生的气泡少。为此,他们进行了如下探究:
(猜想与假设)
①分解速度慢可能与过氧化氢溶液的浓度有关。
②分解速度慢可能与二氧化锰的质量有关。
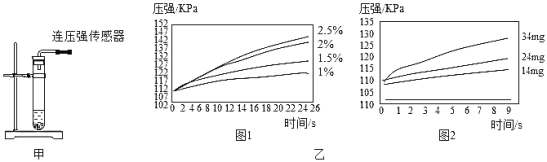
(进行实验)根据图甲进行如下实验。
实验1:用26mg 二氧化锰与5mL不同浓度的过氧化氢溶液进行实验,压强变化如乙图1。
实验2:用5mL 1.5%过氧化氢溶液与不同质量的二氧化锰进行实验,压强变化如乙图2。
(解释与结论)
(1)过氧化氢溶液制取氧气的文字表达式为__________________。
(2)实验1得到的结论是过氧化氢溶液的浓度越_____________,分解速度越快。实验2得到的结论是二氧化锰的质量越_______________,分解速度越慢。
(3)小组同学通过查阅资料得知:同一个反应的催化剂可能有多种。
(查阅资料)除二氧化锰外,氧化铜、氧化铁也可以作为氯酸钾分解的催化剂。
(进行实验)取等质量的氯酸钾按下表进行实验:测定氯酸钾分解产生氧气的温度。
| 实验编号 | 实验药品 | 分解温度 |
| 氯酸钾 | 580 | |
| 氯酸钾、二氧化锰(质量比1:1) | 350 | |
| 氯酸钾、氧化铜(质量比1:1) | 370 | |
| 氯酸钾、氧化铁(质量比1:1) | 390 |
(分析数据、得出结论)
(1)由实验______与实验对比,证明氧化铁可作为氯酸钾分解的催化剂。
(2)实验所用的三种物质中,催化效果最好的是______________。
(反思)证明氧化铜是该反应的催化剂,还要验证它在化学反应前后的质量和____没有改变。
九年级化学科学探究题中等难度题查看答案及解析
甲、乙两同学对镁与盐酸反应进行系列研究。甲、乙两同学取一根镁条,首先用砂纸打磨除去_____,观察到镁条的颜色_____。
研究Ⅰ:镁与盐酸反应过程中的能量变化以及反应速率的变化。
(1)反应中试管外壁发烫,说明镁与稀盐酸反应是_____反应(填“吸热”或“放热”),反应的化学方程式是_____。
(2)实验测得镁片产生气体的速率(v)与时间(t)的关系如图所示,则t1﹣t2内反应速率逐渐加快的主要原因是_____;

反思:t2﹣t3内反应速率逐渐减慢的主要原因是_____;
研究Ⅱ:反应后所得溶液的酸碱性探究。
(3)用pH试纸测定反应后所得溶液的酸碱度,发现pH略小于7。
甲同学:猜想Ⅰ:稀盐酸过量;猜想Ⅱ:氯化镁溶液呈弱酸性。用pH试纸测定酸酸碱度的方法是_____。为验证猜想Ⅱ正确,可以通过查阅资料,也可以取纯净的_____溶液并测定其酸碱度。
(4)乙同学将镁片(有剩余)投入适量稀盐酸,待不再产生气泡时立即测量pH,却发现所得溶液pH大于7,溶液冷却到室温后pH小于7.查阅资料发现①Mg+2H2O=Mg(OH)2↓+H2↑,②20℃时SMg(OH)2=0.009g,80℃时 SMg(OH)2=0.0108g。根据资料,乙同学实验中pH发生变化的原因是_____。
九年级化学科学探究题困难题查看答案及解析