高纯氧化钙是用于电子工业的重要无机化工原料。用硝酸钙溶液制备高纯氧化钙的工艺流程如下:
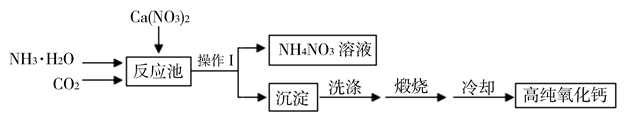
(1)写出操作Ⅰ的名称_____________。
(2)写出煅烧时反应的化学方程式 _____________________________。
(3)该工艺流程中可循环使用的物质是_____________(写名称)。
(4) 冷却需在干燥环境中进行,否则制得的氧化钙中会混有的杂质是_________(写化学式)。
九年级化学信息分析题中等难度题
高纯氧化钙是用于电子工业的重要无机化工原料。用硝酸钙溶液制备高纯氧化钙的工艺流程如下:

(1)写出操作Ⅰ的名称_____________。
(2)写出煅烧时反应的化学方程式 _____________________________。
(3)该工艺流程中可循环使用的物质是_____________(写名称)。
(4) 冷却需在干燥环境中进行,否则制得的氧化钙中会混有的杂质是_________(写化学式)。
九年级化学信息分析题中等难度题
高纯氧化钙是用于电子工业的重要无机化工原料。用硝酸钙溶液制备高纯氧化钙的工艺流程如下:

(1)写出操作Ⅰ的名称_____________。
(2)写出煅烧时反应的化学方程式 _____________________________。
(3)该工艺流程中可循环使用的物质是_____________(写名称)。
(4) 冷却需在干燥环境中进行,否则制得的氧化钙中会混有的杂质是_________(写化学式)。
九年级化学信息分析题中等难度题查看答案及解析
高纯氧化钙是用于电子工业重要的无机化工原料。用硝酸钙溶液制备高纯氧化钙的工艺流程如下,已知:反应池中发生反应的化学方程式为:CO2+2NH3•H2O+Ca(NO3)2═2NH4NO3+X↓+H2O(该流程中硝酸钙完全反应)
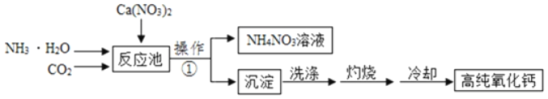
请回答下列问题:
(1)操作①需要用到的玻璃仪器有烧杯、_____、玻璃棒,其中玻璃棒的作用是_____。
(2)该工艺流程中可循环使用的物质是_____。
(3)灼烧过程中,发生的反应的化学方程式为_____。
(4)冷却需在干燥的环境中进行,否则制得的高纯氧化钙中会混有的杂质是_____(填化学式),原因是_____(用化学方程式表示)。
九年级化学流程题中等难度题查看答案及解析

九年级化学解答题中等难度题查看答案及解析
高纯氧化钙是用于电子工业重要的无机化工原料。用硫酸钙浓溶液制备高纯氧化钙的工艺流程如下:

反应池中发生反应的化学方程式为:CO2+2NH3﹒H2O+Ca(NO3)2=2NH4NO3+CaCO3↓+H2O
请回答下列问题:
(1)过滤操作中玻璃棒的作用是。
(2)过滤后所得沉淀表面可能含有的可溶性杂质有(写一种即可)。
(3)该工艺流程中可循环使用的物质是。
(4)冷却需在干燥的环境中进行,否则制得的高纯氧化钙中会混有的杂质是。
(5)上述流程中的副产物NH4NO3可用作氮肥,氮肥的主要作用是。
A. 促进植物生长,叶色浓绿
B. 增强作物的抗寒、抗旱能力
C. 增强作物的抗病虫害、和抗倒伏能力
九年级化学填空题中等难度题查看答案及解析
高纯氧化钙是用于电子工业的重要无机化工原料,用生石灰(主要成分为CaO)制备高纯氧化钙的工艺流程如下:
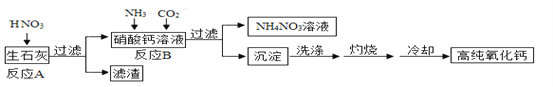
请回答下列问题:
(1)过滤操作中玻璃棒的作用是_______________;
(2) 反应B的化学方程式为________________________;
(3)灼烧时发生反应的化学方程式为_________, 该工艺流程中可循环使用的物质是 _________;
(4)冷却需在密闭和干燥的环境中进行,否则制得的高纯氧化钙中会混有的两种杂质名称分别 是 ___________ 和__________ 。
九年级化学流程题困难题查看答案及解析
高纯氧化钙是用于电子工业的重要无机化工原料,用生石灰(主要成分为CaO)制备高纯氧化钙的工艺流程如下:
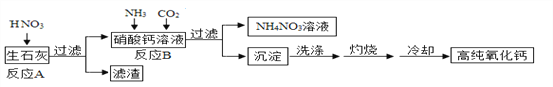
请回答下列问题:
(1)过滤操作中玻璃棒的作用是_______________;
(2) 反应B的化学方程式为________________________;
(3)灼烧时发生反应的化学方程式为_________, 该工艺流程中可循环使用的物质是 _________;
(4)冷却需在密闭和干燥的环境中进行,否则制得的高纯氧化钙中会混有的两种杂质名称分别 是 ___________ 和__________ 。
九年级化学流程题困难题查看答案及解析
以焦炭和碳酸钙为原料生产碳化钙( CaC2 ),并制备重要工业原料乙炔( C2 H2 )气体, 其工艺流程如下图:
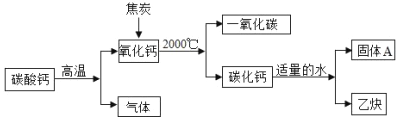
(1)写出碳酸钙分解的化学方程式_____。
(2)将氧化钙和焦炭反应的化学方程式补充完整, CaO + C CaC2 CO ;生成的 CO 不能排放到空气中,是因为_____。
(3)猜想:固体 A 的成分可能是氢氧化钙或碳酸钙。
设计实验证明猜想。
| 实验 | 现象 | 结论 |
| _____ | _____ | 固体A的成分不是碳酸钙 |
九年级化学流程题中等难度题查看答案及解析
无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:
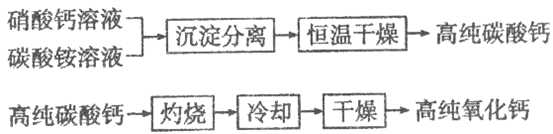
请回答下列问题:
(1)硝酸钙与碳酸铵在溶液中反应,其基本反应类型为___________。
(2)高纯氧化钙生产过程中,“干燥”的主要目的是为了防止__________________ (用化学方程式表示)。
(3)生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是_______。
九年级化学流程题困难题查看答案及解析
(8分) 医用氯化钙常用于合成药物。以工业碳酸钙(含少量Fe3+等杂质)为原料生产二水合氯化钙(CaCl2·2H2O)的流程如下图所示。
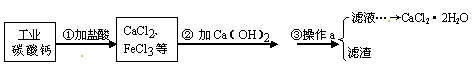
(1)操作a的名称为,实验室进行该操作时玻璃棒的作用是________,滤渣的化学成分有________(写化学式)。
(2)第②步中是否发生化学变化?________(填“是”或“否”)。如果是,请写出其中发生的反应化学方程式________。
(3)青少年正处于生长发育阶段,需要摄入足够的钙,写出一个合理的补钙方法:________
________。
九年级化学填空题中等难度题查看答案及解析
工业上生产电石并制备重要工业原料乙炔
流程如下:
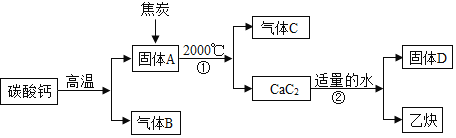
资料:.碳酸钙高温分解可得两种氧化物。
.乙炔的相对分子质量是26,一个乙炔分子有四个原子构成。
.B、C组成的元素相同,C有毒。
(1)写出A、B、C的化学式:A______B______C______。
(2)反应①化学方程式为______。
(3)将一定量的乙炔完全燃烧,生成
水和
二氧化碳,则乙炔的化学式为______。
(4)若向D的澄清溶液中通入二氧化碳,有白色浑浊现象,则反应②的化学方程式为______。
九年级化学流程题中等难度题查看答案及解析