工业上用硫铁矿烧渣(主要成分是Fe3O4、Fe2O3等)、煤粉作原料制备FeCO3的主要流程如下:

(1)焙烧炉中,发生的主要反应为:
① 3C+2O2 2CO+CO2② Fe2O3+CO
2FeO+CO2 ③ Fe3O4+CO
3FeO+CO2
上述反应中的各物质,碳元素呈现 种化合价。
(2)酸浸槽中,FeO转化为FeSO4,加入的物质X是 。
(3)主反应器中,生成FeCO3的反应物为 。
九年级化学填空题中等难度题
工业上用硫铁矿烧渣(主要成分是Fe3O4、Fe2O3等)、煤粉作原料制备FeCO3的主要流程如下:

(1)焙烧炉中,发生的主要反应为:
① 3C+2O2 2CO+CO2② Fe2O3+CO
2FeO+CO2 ③ Fe3O4+CO
3FeO+CO2
上述反应中的各物质,碳元素呈现 种化合价。
(2)酸浸槽中,FeO转化为FeSO4,加入的物质X是 。
(3)主反应器中,生成FeCO3的反应物为 。
九年级化学填空题中等难度题
工业上用硫铁矿“烧渣”(主要成分是Fe3O4、 Fe2O3)、煤粉作原料制备FeCO3的主要流程如下:
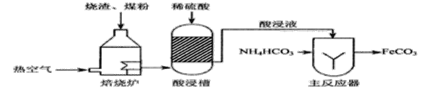
(1)焙烧所得的非气态物用稀硫酸“酸浸”时,会产生少量可燃性气体,生成该气体的化学方程式为_________________。
(2)主反应器中,溶液温度控制在35℃以下的主要原因是__________。
(3)医疗上用碳酸亚铁(FeCO3)给病人食用,可用于防治_____________。
九年级化学流程题困难题查看答案及解析
工业上用硫铁矿烧渣(主要成分是Fe3O4、Fe2O3等)、煤粉作原料制备FeCO3的主要流程如下:

(1)焙烧炉中,发生的主要反应为:
① 3C+2O2 2CO+CO2② Fe2O3+CO
2FeO+CO2 ③ Fe3O4+CO
3FeO+CO2
上述反应中的各物质,碳元素呈现 种化合价。
(2)酸浸槽中,FeO转化为FeSO4,加入的物质X是 。
(3)主反应器中,生成FeCO3的反应物为 。
九年级化学填空题中等难度题查看答案及解析
自来水厂常用氯气杀菌消毒,用明矾、氯化铁等净化水。以硫铁矿(主要成分是FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的流程如图:
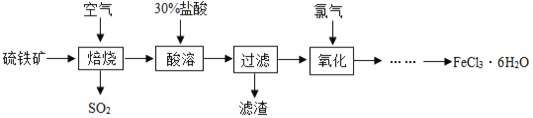
(1)已知“焙烧”阶段就是硫铁矿的燃烧,生成物是Fe2O3和SO2,写出该反应的化学方程式 _________________,硫铁矿进行燃烧前要将其粉碎,其目的是____________。
(2)大量排放出的SO2能形成_________,危害环境,可将含SO2的废气通入氨水中,氨水的pH______7,反应后生成的亚硫酸铵[(NH4)2SO3]在农业上可做__________肥。
(3)①流程中用30%盐酸“酸溶”焙烧后的残渣,写出化学方程式_________;
②在“酸溶”时是否可以用硫酸代替盐酸?________(填“可以”或“不可以”),原因是____;
③若在实验室欲用38%(密度为1.18 g/ml)的盐酸配制30%的盐酸,则需要的玻璃仪器有烧杯、胶头滴管、________、________等。
(4)实际上“焙烧”阶段很难做到将硫铁矿完全反应,因“酸溶”后的混合物中有FeCl2,将其在“氧化”阶段与氯气(Cl2)反应生成FeCl3,写出化学方程式__________________。
九年级化学流程题困难题查看答案及解析
自来水厂常用氯气杀菌消毒,用明矾、氯化铁等净化水。以硫铁矿(主要成分是FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的流程如图:
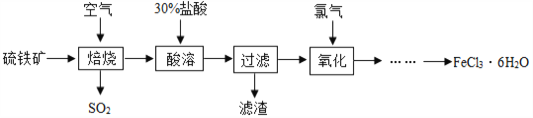
(1)已知“焙烧”阶段就是硫铁矿的燃烧,生成物是Fe2O3和SO2,写出该反应的化学方程式 _________________,硫铁矿进行燃烧前要将其粉碎,其目的是____________。
(2)大量排放出的SO2能形成_________,危害环境,可将含SO2的废气通入氨水中,氨水的pH______7,反应后生成的亚硫酸铵[(NH4)2SO3]在农业上可做__________肥。
(3)①流程中用30%盐酸“酸溶”焙烧后的残渣,写出化学方程式_________;
②在“酸溶”时是否可以用硫酸代替盐酸?________(填“可以”或“不可以”),原因是____;
③若在实验室欲用38%(密度为1.18 g/ml)的盐酸配制30%的盐酸,则需要的玻璃仪器有烧杯、胶头滴管、________、________等。
(4)实际上“焙烧”阶段很难做到将硫铁矿完全反应,因“酸溶”后的混合物中有FeCl2,将其在“氧化”阶段与氯气(Cl2)反应生成FeCl3,写出化学方程式__________________。
九年级化学流程题困难题查看答案及解析
自来水厂常用氯气杀菌消毒,用明矾、氯化铁等净化水。以硫铁矿(主要成分是FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的流程如图:
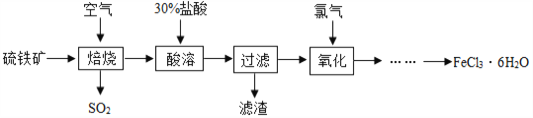
⑴已知“焙烧”阶段就是硫铁矿的燃烧,生成物是Fe2O3和SO2,写出该反应的化学方程式_________,硫铁矿进行燃烧前要将其粉碎,其目的是________。
⑵大量排放出的SO2能形成________,危害环境,可将含SO2的废气通入氨水中,氨水的pH____7,反应后生成的亚硫酸铵[(NH4)2SO3]在农业上可做________肥。实验室使用氢氧化钠溶液来吸收SO2(SO2 + 2NaOH = Na2SO3 + H2O)。现有6.4gSO2,至少需要10%的氢氧化钠溶液的质量是多少_______?(写出计算过程)
⑶①流程中用30%盐酸“酸溶”焙烧后的残渣,写出化学方程式_____________________。
②在“酸溶”时是否可以用硫酸代替盐酸?______(填“可以”或“不可以”),原因是_____。
③若在实验室欲用38%(密度为1.18 g/ml)的盐酸配制30%的盐酸,则需要的玻璃仪器有烧杯、胶头滴管、________、________等。
⑷实际上“焙烧”阶段很难做到将硫铁矿完全反应,因“酸溶”后的混合物中有FeCl2,将其在“氧化”阶段与氯气(Cl2)反应生成FeCl3,写出化学方程式_________________。
九年级化学流程题中等难度题查看答案及解析
碳酸亚铁(FeCO3)可用于制作补铁药物,以下是用硫铁矿烧渣(主要成分为Fe2O3、SiO2 等)为原料制备碳酸亚铁的生产流程示意图: 已知 40℃以上,(NH4)2CO3易分解。
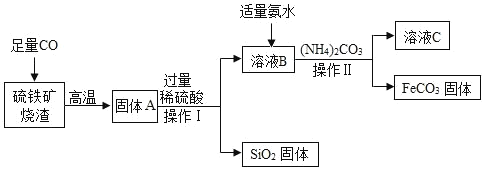
(1)操作Ⅰ的名称为_____该操作所用到的玻璃仪器有烧杯、玻璃棒和_____。
(2)写出向硫铁矿中通入 CO 的化学方程式_____。
(3)加入(NH4)2CO3后,该反应必须控制的条件是温度_____。
(4)写出溶液 B 中主要成分的阴离子符号_____。
(5)从溶液C中可回收一种化工产品(NH4)2SO4,请写出它的一种用途用作_____。
九年级化学流程题中等难度题查看答案及解析
我国重点推动城乡供水与水生态环境改善等水务工作。氯化铁是常见的水处理剂。以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3•6H2O)的工艺流程如下:
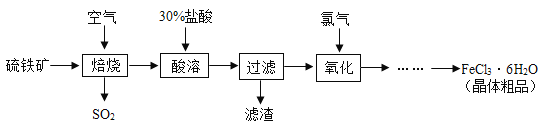
回答下列问题:
(1)硫铁矿在空气中焙烧流程中生成氧化铁和二氧化硫,请将硫铁矿和空气反应的化学方程式补充完整:4FeS2+11X=2Fe2O3+8SO2,则物质X的化学式为__。
(2)大量排放出的二氧化硫能形成___,危害环境。可将含二氧化硫的废气通入呈碱性的氨水中吸收二氧化硫,则氨水的PH___7(填写“大于”、“小于”或“等于”)。
(3)在实验室中,欲用38%(密度为1.18g/mL)的盐酸配制30%的盐酸,则需要的玻璃仪器主要有___、___(填两种仪器名称)。
(4)上述流程中需用30%的盐酸“酸溶”焙烧后的残渣(主要成分是氧化铁),写出该反应的化学方程式为:_____。
(5)利用结晶方法制备氯化铁晶体时,使用了玻璃棒,其作用是________________。
九年级化学流程题中等难度题查看答案及解析
高纯氧化铁(Fe2O3)又称“引火铁”,可作催化剂,在现代工业上有广泛应用前景。以下是用赤铁矿(含少量不溶于水的SiO2等)为原料,制备高纯氧化铁的生产流程图。(资料:FeCO3难溶于水)
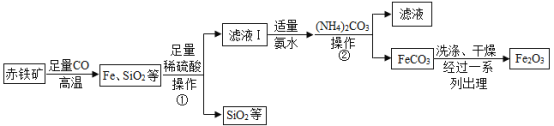
(1)写出高温时赤铁矿中的Fe2O3与CO发生反应的化学方程式___________________________。
(2)上述流程图中第2步实验加入足量稀硫酸后观察到的现象为:固体部分溶解,________________。
(3)操作②用到的玻璃仪器有________________。
(4)上述流程中加入碳酸铵时发生反应的基本反应类型是________________。
九年级化学推断题中等难度题查看答案及解析
工业上用菱锰矿[主要成分为MnCO3,含FeCO3、Cu2(OH)2CO3、SiO2等杂质]为原料来制取二氧化锰,其生产流程示意图如下:
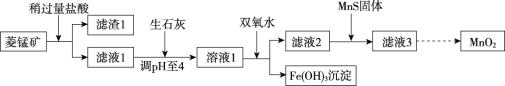
回答下列问题:
(1)将滤液与滤渣分离的操作是______。
(2)向菱锰矿中加入盐酸,MnCO3、FeCO3、Cu2(OH)2CO3都溶解并转化为MnCl2、FeCl2、CuCl2。盐酸与MnCO3反应的化学方程式为________。
(3)加入生石灰将溶液pH调至4,此时溶液呈________(填“酸性”或“碱性”)。
(4)加入双氧水将铁元素转化为Fe(OH)3沉淀,其反应为: 2FeCl2 + H2O2 + 4H2O = 2Fe(OH)3↓ + 4HCl,该反应化合价发生变化的元素是氧和_______。
(5)加入Na2S、MnS等硫化物,均可将MnCl2中混有的CuCl2转化为CuS沉淀除去,但实际生产中选用MnS,其原因是________。
九年级化学流程题困难题查看答案及解析
工业上用菱锰矿[主要成分为MnCO3,含FeCO3、Cu2(OH)2CO3、SiO2等杂质]为原料来制取二氧化锰,其生产流程示意图如下:

回答下列问题:
(1)加盐酸之前,需要将菱锰矿粉碎,目的是________
(2)操作②是______,此操作过程中用的玻璃仪器有玻璃棒、______、 _______,其中玻璃棒的作用是________。
(3)向菱锰矿中加入盐酸,MnCO3、FeCO3、Cu2(OH)2CO3都溶解并转化为MnCl2、FeCl2、CuCl2。盐酸与MnCO3反应的化学方程式为_______________。滤渣1主要成分是二氧化硅,需要洗涤,洗涤的目的是________________,可以通过在最后一次洗涤液中滴加________(填化学式)溶液,若无明显现象,则已洗涤干净。
(4)加入双氧水将铁元素转化为Fe(OH)3沉淀,其反应为:2FeCl2 + H2O2 + 4H2O = 2Fe(OH)3↓ + 4HCl,该反应化合价发生变化的元素是氧和________(填元素名称)。
(5)加入Na2S、MnS等硫化物,均可将MnCl2中混有的CuCl2转化为CuS沉淀除去,但实际生产中选用MnS,其原因是________。
九年级化学流程题困难题查看答案及解析