-
已知A、B、C、D都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他3种元素既不在同一周期又不在同一主族。B原子的L层p轨道中有5个电子;C是周期表中1-18列中的第14列元素;D原子的L层电子数与最外层电子数之比为4:1,其d轨道中有一对成对电子。请回答:
(1)A与C形成的共价化合物的分子式是 ,中心原子杂化类型是__ ,分子的立体结构是 ,是 分子(填“极性”或“非极性”)
(2)B与C比较,电负性较小的是 (填元素符号);B与C形成的化合物晶体类型是 。
(3)D位于元素周期表中第 族,D2+的结构示意图是 ,它的+3价离子的电子排布式为 。
(4)A与B形成的化合物分子极易溶于水,其原因 是 。
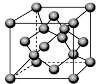
(5)由C原子构成的晶体中微粒间作用力是 ,右图是由C单质构成的晶体的一个晶胞,若设该晶胞的边长为a cm,NA表示阿伏加德罗常数,则该晶体的密度是 g/cm3.(只要求列出算式)。
高二化学填空题困难题查看答案及解析
-
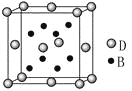
已知A、B、C、D、E是元素周期表中1~36号元素,其原子序数依次增大,且A、B、C、D为主族元素。A与另外四种元素既不在同一周期,也不在同一主族。B和C同主族,D和E同周期;元素E是周期表中的第7列元素,D的最外层电子数与最内层电子数相同,D跟B可形成离子化合物,其晶胞结构(其中B原子在晶胞内部)如图。
请回答下列问题:
(1)C-的电子排布式为_______;E元素原子的价电子排布式为________。
(2)元素B与氮元素可以形成化合物NB3,其中N-B键的化学键类型为________,根据价层电子对互斥理论可以判断NB3的空间构型为________,NB3分子中N原子的杂化方式为________杂化。
(3)A、B形成的化合物AB的相对分子质量比A、C形成的化合物AC的相对分子质量小,但AB的沸点比AC高,其原因是_________________________。
(4)从晶胞图可以得出:D与B形成的离子化合物的化学式为______________。
(5)含有D元素的化合物焰色反应为______色,焰色反应的原理是__________。
高二化学推断题中等难度题查看答案及解析
-
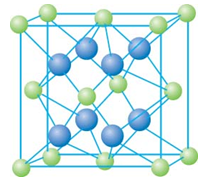
(13分) 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素。D的原子序数比E小5,D跟B形成的晶体其晶胞结构如图,图中小球代表D,大球代表B。
请回答:
(1)A元素的名称是________________;
(2)B元素的轨道表示式是________________,C的原子结构示意图是________________,B与A形成的化合物比C与A形成的化合物沸点高,其原因是__________________________________________________________;
(3)E属于元素周期表中第________周期,第________族的元素,其元素名称是________;属于元素周期表中的________区(填元素分区),它的+2价离子的电子排布式为________________;
(4)从图中可以看出,D跟B形成的离子化合物的化学式为________________;该离子化合物晶体的密度为a g•cm-3,则晶胞的体积是________________(只要求列出算式)。
高二化学填空题简单题查看答案及解析
-
已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大.A与其他4种元素既不在同一周期又不在同一族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第8列元素.D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如图.请回答:
(1)A与B形成的化合物在固态时的晶体类型是______;A与B形成的化合物比A与C形成的化合物熔点要______(填高、低)
(2)写出C的单质与水反应的离子方程式______;
(3)如图所示,D跟B形成的离子化合物的化学式为______;鉴别该离子化合物是否为晶体,最可靠的科学方法是______,该离子化合物晶体的密度为ag•cm-3,B、D两元素的相对原子质量分别为b、c,则晶胞的体积是______cm3(只要求列出算式).
高二化学解答题中等难度题查看答案及解析
-
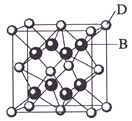
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图。
请回答:
(1)A元素的名称是 ;
(2)B的元素符号是 ,C的元素符号是 ,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是
(3)E属元素周期表中第 周期,第 族的元素,其元素名称是 , 它的+2价离子的电子排布式为 :
(4)从图中可以看出,D跟B形成的离子化合物的化学式为 ;该离子化合 物晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出算式)。
高二化学填空题中等难度题查看答案及解析
-
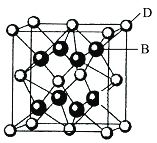
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1~18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物,其晶胞结构如图。
请回答:
(1)A元素的名称是______。
(2)B的元素符号是__________,C的元素符号是______。
(3)E属元素周期表中第________周期第______族的元素,其元素名称是______,它的+2价离子的电子排布式为________。
(4)从图中可以看出,D跟B形成的离子化合物的化学式为______;该离子化合物晶体的密度为a g·cm-3,则晶胞的体积是______(只要求列出算式)。
高二化学综合题困难题查看答案及解析
-
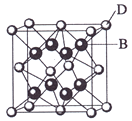
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图。
请回答:
(1)A元素的名称是 ;
(2)B的元素符号是 ,C的元素符号是 ,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是
(3)E属元素周期表中第 周期,第 族的元素,其元素名称是 , 它的+2价离子的电子排布式为 :
(4)从图中可以看出,D跟B形成的离子化合物的化学式为 ;该离子化合 物晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出算式)。
高二化学填空题中等难度题查看答案及解析
-
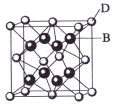
(10分)已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大。A与其他4种元素既不在同一周期又不在同一族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第8列元素。D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如图。请回答:
(1)基态E3+离子核外有 种运动状态不同的电子。
(2)写出B的单质与水反应的离子方程式 ;
(3)如图所示,D跟B形成的离子化合物的化学式为 ;鉴别该离子化合物是否为晶体,最可靠的科学方法是 。
(4)A与B形成的化合物在气态时存在(AB)2二聚分子,原因是 ;A与B形成的化合物比A与C形成的化合物熔点要____(填高或低)
高二化学填空题中等难度题查看答案及解析
-
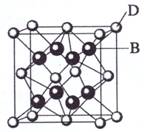
(10分)已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大。A与其他4种元素既不在同一周期又不在同一族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第8列元素。D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如右图。请回答:
(1)A与B形成的化合物在固态时的晶体类型是________;A与B形成的化合物比A与C形成的化合物熔点要____(填高、低)
(2)
写出C的单质与水反应的离子方程式;
(3)如图所示,D跟B形成的离子化合物的化学式为________;鉴别该离子化合物是否为晶体,最可靠的科学方法是________,该离子化合物晶体的密度为ag·cm-3,B、D两元素的相对原子质量分别为b、c,则晶胞的体积是________cm3(只要求列出算式)。
【解析】在前36号元素中,符合周期表中1—18列中的第8列元素的是铁,即E是铁,则D是Ca。根据D跟B形成离子化合物晶胞结构可判断,该离子化合物是DB2,则B是F或Cl。因为B和C属同一主族,且原子序数前者小于后者,所以B只能是F,C是Cl,A与其他4种元素既不在同一周期又不在同一族,所以A是H。
(1)HF属于分子晶体,由于HF中含有氢键,所以HF的沸点高于氯化氢的。
(2)氯气溶于水生成盐酸和次氯酸。
(3)鉴别离子化合物是否为晶体,最可靠的科学方法是射线衍射法。在该晶胞中含有的该离子是8×1/8+6×1/2=4,则F-是8,所以晶胞的体积是(8b+4c)/a NA。
高二化学填空题简单题查看答案及解析
-
A、B、C、D、E是相邻三个周期中的五种元素,它们的原子序数依次增大,B、C、D属同一周期,A、E在周期表中处于同一纵行。已知:
①除A外,各元素原子的内层均已填满电子,其中B的最外层有4个电子;
②A与B,B与C都能生成气态非极性分子的化合物;
③D与E生成离子化合物,其离子的电子层结构相同。
回答:
(1)A为________元素,B为________元素,C为________元素,D为________元素。
(2)C元素在周期表中属________周期________族元素,其原子电子排布式为________。
(3)B与C形成的非极性分子的电子式是________。其中共价键类型及数目是________。(填σ键或π键)
高二化学填空题中等难度题查看答案及解析