-
工业上常利用电石制乙炔气体(C2H2)时产生的灰浆和残渣制备化工原料KClO3和超细CaCO3。
电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:

其中电石与水反应生成氢氧化钙和乙炔,该反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑ 残渣中主要成分是Ca(OH)2 和CaCO3。
Ⅰ.制备KClO3的流程如下:

(1)向灰浆浊液中通入Cl2 ,得到Ca(ClO3)2、CaCl2溶液。反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5。写出此反应的化学方程式 。
(2)有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
上述流程中加入KCl粉末,KCl与 (填化学式)发生了复分解反应,得到KClO3晶体。你认为能得到KClO3 晶体的原因是 。
(3)洗涤时,可以选用下列 作洗涤剂(填字母编号)。
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):

(4)流程中溶液A可循环使用,其主要成分的化学式是 。
-
工业上常利用电石制乙炔气体(C2H2)时产生的灰浆和残渣制备化工原料KClO3和超细CaCO3。电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:

其中电石与水反应生成氢氧化钙和乙炔,该反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑ 残渣中主要成分是Ca(OH)2 和CaCO3。
Ⅰ.制备KClO3的流程如下:

(1)向灰浆浊液中通入Cl2 ,得到Ca(ClO3)2、CaCl2溶液。反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5。写出此反应的化学方程式_________________。
(2)有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
上述流程中加入KCl粉末,KCl与_____________(填化学式)发生了复分解反应,得到KClO3晶体。你认为能得到KClO3 晶体的原因是____________。
(3)洗涤时,可以选用下列______________作洗涤剂(填字母编号)。
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):

(4)流程中溶液A可循环使用,其主要成分的化学式是__________。
-
工业上常利用电石制乙炔气体 时产生的灰浆和残渣制备化工原料
时产生的灰浆和残渣制备化工原料 和超细
和超细 .
.
 电石制乙炔气体
电石制乙炔气体 时产生灰浆和残渣的过程如下:电石
时产生灰浆和残渣的过程如下:电石 灰浆
灰浆 残渣,其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式 ______,残渣中主要成分是
残渣,其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式 ______,残渣中主要成分是 和 ______ .
和 ______ .
Ⅰ 制备
制备 的流程如图:
的流程如图:

 向灰浆浊液中通入
向灰浆浊液中通入 ,得到
,得到 、
、 溶液.反应中
溶液.反应中 与
与 的化学计量数分别为1和
的化学计量数分别为1和 写出此反应的化学方程式 ______ .
写出此反应的化学方程式 ______ .
 有关物质在常温下的溶解度如下:
有关物质在常温下的溶解度如下:
上述流程中加入KCl粉末,KCl与 ______  填化学式
填化学式 发生了复分解反应,得到
发生了复分解反应,得到 晶体.你认为能得到
晶体.你认为能得到 晶体的原因是 ______ .
晶体的原因是 ______ .
 洗涤时,可选用下列洗涤剂 ______
洗涤时,可选用下列洗涤剂 ______  填字母编号
填字母编号 .
.
A KCl饱和溶液  冰水
冰水  饱和
饱和 溶液
溶液
Ⅱ 制备超细
制备超细 的流程如下
的流程如下 注:加入
注:加入 溶液的目的是溶解残渣中的难溶盐
溶液的目的是溶解残渣中的难溶盐 :
:

 向
向 溶液中通入两种气体,生成超细
溶液中通入两种气体,生成超细 的化学方程式 ______
的化学方程式 ______  检验
检验 是否洗涤干净的方法是 ______ .
是否洗涤干净的方法是 ______ .
 流程中溶液A可循环使用,其主要成分的化学式是 ______ .
流程中溶液A可循环使用,其主要成分的化学式是 ______ .
-
有一工业过程:电石(CaC2)
 灰浆
灰浆 残渣
残渣
其中电石与水的反应为:CaC2+2H2O=Ca(OH)2+C2H2↑
(1)残渣中主要成分是Ca(OH)2和______.
工业上利用乙炔(C2H2)产生的灰浆和残渣制备化工原料KClO3和超细CaCO3.
Ⅰ.制备KClO3的流程如下:

(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式______.
(3)有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CalO3 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
上述流程中加入KCl粉末,KCl与______(填化学式)发生了复分解反应,得到KClO3晶体.你认为能得到KClO3晶体的原因是______.
(4)洗涤时,可选用下列______洗涤剂(填字母编号).
A、KCl饱和溶液 B、冰水 C、饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl的目的是溶解残渣中的难溶盐):
(5)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式______.
(6)流程中溶液A可循环使用,其主要成分的化学式是______.
-
工业上利用电石(CaC2)制备高纯碳酸钙的流程如下:
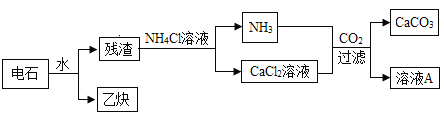
已知:①CaC2+2H2O=Ca(OH)2+C2H2↑;②CaCl2+H2O+CO2+2NH3=CaCO3↓+2NH4Cl。
(1)乙炔(C2H2)是一种常见的然料,当氧气不足时,除了生成水和二氧化碳外,还同时生成碳的另一种常见氧化物,写出乙炔不充分燃烧的化学方程式__________________。
(2)该流程中可循环使用的物质是______________(填名称)。
(3)电石长期露置于空气中,最终所得固体中一定含有碳酸钙,用化学方程式解释存在该物质的原因____________________。因此电石应该___________________保存。
-
工业上利用电石(CaC2)制备高纯碳酸钙的流程如下:

已知:①CaC2+2H2O=Ca(OH)2+C2H2↑
②CaCl2+H2O+CO2+2NH3=CaCO3↓+2NH4Cl
(1)乙炔(C2H2)是一种常见的燃料,写出乙炔完全燃烧的化学方程式______。
(2)该流程中可循环使用的物质是_________(填名称)。
(3)电石长期露置于空气中,最终所得固体中一定含有碳酸钙,用化学方程式解释存在该物质的原因______________;因此电石应该______保存。
-
乙炔(C2H2)是一种极易燃的气体,是生产聚氯乙烯的重要原料。工业上用电石(主要成分为CaC2)制取乙炔的流程如下。
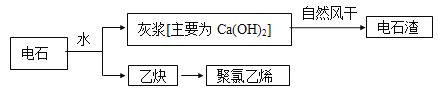
(1)C2H2中碳、氢元素的质量比为______。
(2)电石渣可以处理含硫酸的废水,属于_______反应。
-
某兴趣小组对氯酸钾(KClO3)展开如下探究:
(探究一)工业制备KClO3
以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:
(资料卡片):氯化时,主要反应为6Ca(OH)2 + 6X ═ Ca(ClO3)2 + 5CaCl2 + 6H2O,少量 X与Ca(OH)2反应生成Ca(ClO)2、CaCl2和H2O,Ca(ClO)2 分解为CaCl2和O2。
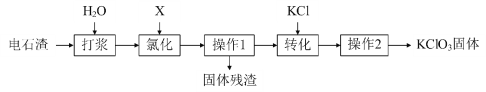
(1)根据资料,X的化学式为______,写出氯化时,X和Ca(OH)2反应生成Ca(ClO)2的化学方程式______。
(2)氯化时,为提高X转化为Ca(ClO3)2的转化率,下列措施可行的是______(填序号)。
A.充分搅拌浆料 B.加足量水使Ca(OH)2完全溶解 C.缓缓通入X
(3)操作1在实验室中的名称是______,需要用到的玻璃仪器有______、______和玻璃棒,玻璃棒的作用是______。氯化过程控制电石渣过量,固体残渣的主要成分为______和______(填化学式)。
(4)操作1后得到溶液中Ca(ClO3)2与CaCl2的化学计量数之比______1:5(填“>”、“<”或“=”)。转化时,加入KCl发生反应的化学方程式为______。
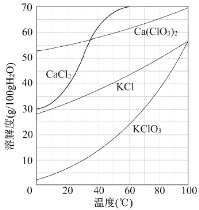
(5)操作2包含一系列实验操作,结合如图分析,主要操作为蒸发浓缩 →______→过滤→洗涤→低温烘干。
(探究二)探究KClO3制氧气
某小组利用如图所示装置对KClO3制氧气进行了探究:

(资料卡片):
①KClO3的熔点约为356℃,MnO2在加热条件下不分解。
②KClO3分解时,传感器得到氧气浓度随温度的变化示意图及使用不同催化剂时的固体残留率示意图如下:
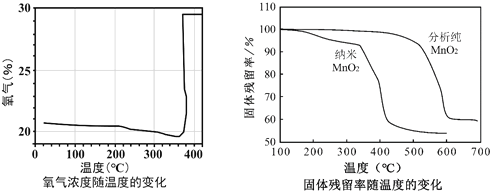
(6)由图可知KClO3分解温度______(填“高于”、“等于”或“低于”)其熔点。
(7)图中,在KClO3分解前,传感器测得氧气浓度降低的原因可能是______。
(8)分析图中,对KClO3分解催化效果更好的催化剂是______。
(9)将3.06gKClO3和MnO2混合物以4:1配比加热至完全反应,可得氧气体积约为多少升____?(写出计算过程,计算时精确到小数点后两位。已知氧气密度约为1.43g / L。)
-
乙炔(C2H2)俗称“电石气”,在常温常压下,是一种无色、无味、密度比空气略小、难溶于水的气体;工业上常用它燃烧产生的高温切割和焊接金属;实验室用块状的电石与水反应制取乙炔.
(1)写出带标号的仪器的名称:①______,②______
(2)实验室制取乙炔应选择的发生装置是______,较易判断收集已满的收集装置是______;
(3)工业上制取的乙炔常带有特殊臭味,可能生成了下列哪种气体______;
A.氢气 B.甲烷 C.一氧化碳 D.硫化氢
(4)在焊接或切割时,乙炔燃烧的化学方程式为______ 2H2O+4CO2

-
工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如图1:
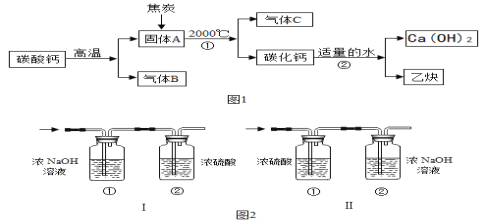
(资料)
(1)CaCO3 CaO(固体)+CO2↑。
CaO(固体)+CO2↑。
(2)浓硫酸是常用的干燥剂,NaOH 溶液能吸收CO2。
(讨论)
(1)C、B组成元素相同,C有毒,反应①的化学方程式为_______。
(测定乙炔组成)资料:一个乙炔分子由四个原子构成。
(2)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过图2的_________
(选填“I”或“II”)装置,并再缓缓通入一段时间 的 N2,并记录实验数据于表中。
| 反应前质量/g | 反应后质量/g |
| 装置① | 125.3 | 127.1 |
| 装置② | 78.2 | 87.0 |
(3)实验中“缓缓通入一段时间 N2”的目的是___________。
(4)计算:乙炔中碳元素的质量为________g,氢元素 的质量为_______g,乙炔的化学式为_________。
(5)反应②的化学方程式___________。
















