-
【化学——选修3:物质结构与性质】
A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素原子的最外层电子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子。请回答下列问题:
(1)当n=2时,AB2属于__________分子(填“极性”或“非极性”),分子中有__________个δ键、__________个π键。A6H6分子中A原子的杂化轨道类型是__________杂化。
(2)当n=3时,A与B形成的晶体属于__________晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是__________(用元素符号表示).
(4)已知某红紫色配合物的组成为CoCl3·5NH3·H2O,该配合物中的中心离子钴离子在基态时的核外电子排布式为____________________。
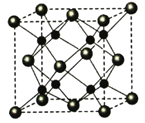
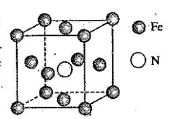
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为__________。

-
元素周期表前四周期A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ms1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有五个未成对电子。
(1)写出E元素名称:________
(2)C基态原子的电子排布图为___________________,若A为非金属元素,则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于________键(填“σ”或“π”)。
(3)当n=2时,BC分子的结构式是 ________;当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是______________。
(4)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是__________________(用元素符号表示)。
(5)E元素原子的价电子排布式是________,在元素周期表中位置是______________,其最高价氧化物的化学式是______________。
-
元素周期表前四周期A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ms1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有五个未成对电子。
(1)E元素原子的价电子排布式是______,在元素周期表中位置是_____,其最高价氧化物的化学式是__________。
(2)C基态原子的电子排布图为_____,若A为非金属元素,则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于_____键(填“σ”或“π”)。
(3)当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是_______。
(4)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,A、B、C、D四种元素的电负性由大到小的顺序是_____(用元素符号表示)。
-
【化学——选修3物质结构与性质】已知A、B、C、D、E、F是元素周期表中前36号元素,它们的原子序数依次增大。A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E是第四周期d区原子序数最大的元素,F+的最外层电子排布全充满。请回答下列问题:
(1)写出E的价层电子排布式 。
(2)A、B、C、D电负性由小到大的顺序为________(填元素符号)。
(3)E(BD)4为无色或黄色挥发性剧毒液体,熔点-19.3℃,沸点43℃。不溶于水,易溶于乙醇、乙醚、苯等有机溶剂,呈四面体构型,该晶体的类型为 ,E与BD之间的作用力为 。
(4)①写出一种与BD32-互为等电子体的分子的化学式 。
②含F2+的溶液与K2SO4、氨水反应可得到化合物 [F(NH3)4]SO4。1 mol配合物离子[F(NH3)4]2+中含σ键的数目为 。
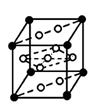
③ E元素与镧(La)元素的合金可做储氢材料,该晶体的晶胞如图所示,晶胞中心有一个E原子,其他E原子都在晶胞面上,则该晶体的化学式为 ;已知该合金的摩尔质量为M g•mol-1,晶胞参数为a pm,用NA表示阿伏伽德罗常数,则该晶胞的密度为 g.cm-3。
-
【化学-选修3:物质结构与性质】
I .已知A、B、C、D、E、F为元素周期表中前四周期且原子序数依次增大的六种元素。其中A、B、C、D核电荷数之和为36, A、C原子的最外层电子数之和等于B原子的次外层电子数,D原子质子数为B原子质子数的两倍,E元素所在主族均为金属,F的价电子数 与C的核电荷数相等。
(1)下列关于上述几种元素的说法正确的是 。
a.B、C、D的原子半径由大到小的顺序为:D>C>B
B.E、F的最外层电子数相等
c.A、B、C、D四种元素中电负性和第一电离能最大的均为B
d.B与C形成的化合物中可能含有非极性键
e.A、C、F位于周期表的s区
(2)B单质有两种同素异形体。其中在水中溶解度较大的是 (填化学式),原因是 。
(3)EA2和A2B熔点较高的是 (填化学式),原因是 。
(4)D与B可以形成两种分子,其中DB2分子中心原子的杂化类型是 。
下列分子或离子中与DB3结构相似的是 。
a.NH3 B.SO32- C. NO3- D. PCl3
(5)已知B、F能形成两种化合物,其晶胞如图所示。则高温时甲易转化为乙的原因为 。
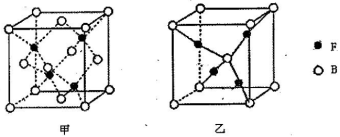
若乙晶体密度为pg/cm3,则乙晶胞的晶胞参数为a = nm。
Ⅱ.金属在化工生产及日常生活中有着广泛的应用,如铁、铬、镓等在现代工业中备受青睐。
(1)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态Cr原子中,未成对电子数有 个, Cr3+的价电子排布式为 。
(2) Zn与Ga的第一电离能从大到小的顺序为 。
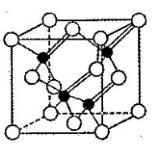
(3)镓与第VA族元素可形成多种新型人工半导体材料, 砷化镓(GaAs)就是其中一种,其晶体结构如右图所示(白色球代表原子)。在GaAs晶体中,距离每个Ga原子最近的As原子有 个,距离每个As原子最近的As原子有 个。
(4)与As同主族的短周期元素是N、P,AsH3 空间构型为 ;一定压强下将AsH3和NH3、PH3的混合气体降温时首先液化的是 ,理由是 。
(5)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如下图所示,则氮化铁的化学为 ;设晶胞边长为acm,阿伏加德罗常数为 ,该晶体的密度为 g•cm-3(用含a和NA的式子表示)。
,该晶体的密度为 g•cm-3(用含a和NA的式子表示)。
-
(10分)【化学——选修3:物质结构与性质】A、B、C、D、E是元素周期表中原子序数依次递增的前四周期元素。A原子最外层电子数为内层电子数的3倍;B的焰色反应呈黄色;C的氢化物是一种强酸,其浓溶液可与A、E的化合物反应生成C的单质;D是一种金属元素,其基态原子中有6个未成对电子。请回答下列问题:
(1)D的基态原子价层电子排布式为__________ 。
(2)C的氢化物的沸点比其上一周期同族元素的氢化物低,是因为__________。
(3)A、C电负性大小顺序是_______(用元素符号表示),C的最高价含氧酸根的空间构型为__________,其中心原子的杂化类型为___________。
(4)A、B形成的化合物的晶胞如图所示,该晶胞的化学式为_________,其中A离子的配位数为__________,该晶体类型为___________。

(5)该晶胞的边长为a pm(NA表示阿伏伽德罗常数),则该晶胞的密度为______g/cm3(列出算式)。
-
[化学﹣﹣选修物质结构与性质]
下表为长式周期表的一部分,其中的序号代表对应的元素.

(1)写出上表中元素⑨原子的外围电子排布式 .
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为 杂化;元素⑦与⑧形成的化合物的晶体类型是 .
(3)元素④的第一电离能 > ⑤(填写“>”、“=”或“<”)的第一电离能;元素④与元素①形成的X分子的空间构型为 .请写出与元素④的单质互为等电子体分子、离子的化学式 (各写一种).
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是 .
(5)④的最高价氧化物对应的水化物稀溶液与元素⑦的单质反应时,元素④被还原到最低价,该反应的化学方程式为 .
(6)将过量的X通入含有元素⑩的蓝色硫酸盐溶液中,反应的离子方程式为 ;元素⑩的某种氧化物的晶体结构如图所示,其中实心球表示元素⑩原子,则一个晶胞中所包含的氧原子数目为 .

-
[化学——选修3:物质结构与性质]
X、Y、Z、W、Q为前四周期的五种元素,且原子序数依次增大。已知X、Y、Z、W均为非金属元素,XW2分子与Y3-为等电子体,元素W和元素Z为同族元素,Q的最外层电子数为2,次外层电子数等于Y和W2 -最外层电子数之和,根据以上信息回答下列问题:
(1)上述五种元素中电负性最大的是___(填元素符号,下同),Y的第一电离能大于Z的第一电离能原因___________________________________。
(2)XW2的电子式为______________。
(3)Q的价电子排布式为_____________,Y3-的分子构型为______________。
(4)下列关于WZ2结构的说法正确的是___________(填序号)。
a.WZ2为直线形非极性分子 b.WZ2为直线形极性分子
c.WZ2中W为sp3杂化 d.WZ2中W为sp2杂化
(5) W有两种常见的含氧酸,较高价的酸性比较低价的______,理由______________。
(6)α-QW的晶胞是立方体,用X射线衍射法测得该晶体晶胞边长=520.0pm,26℃测得该晶体的密度为4.1g/cm3,请列式计算一个晶胞中含有的Q、W离子数。(5.23≈140.6)
-
【化学选修3:物质结构与性质】(15分)
(1)目前,利用金属或合金储氢的研究已取得很大进展,如图是一种镍基合金储氢后的晶胞结构图。
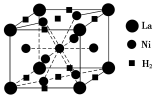
①Ni在元素周期表中的位置是 ,其基态原子的外围电子排布式 是 。
②该合金储氢后,含1 mol La的合金可吸收H2的物质的量为 。
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态的电子排布式可表示为 。
②BH—4的空间构型是 (用文字描述)。
(3)液氨是富氢物质,是氢能的理想载体,利用N2+3H2 2NH3实现储氢和输氢。下列说法正确的是 (多项选择)。
2NH3实现储氢和输氢。下列说法正确的是 (多项选择)。
a.NH3分子中N原子采用sp3杂化
b.相同压强时,NH3沸点比PH3高
c.[Cu(NH3)4]2+离子中,N原子是配位原子
d.CN—的电子式为:
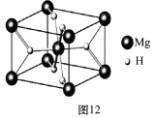
(4)MgH2是金属氢化物储氢材料,其晶胞结构如图12所示,已知该晶体的密度ag·cm-3,则晶胞的体积为 cm3〔用含a、NA的代数式表示(NA表示阿伏伽德罗常数)〕。
-
[化学—选修3:物质结构与性质](15分)A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、 D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是 (填元素符号),其中C原子的核外电子排布式为__________。
(2)单质A有两种同素异形体,其中沸点高的是 (填分子式),原因是 ;A和B的氢化物所属的晶体类型分别为 和 。
(3)C和D反应可生成组成比为1:3的化合物E, E的立体构型为 ,中心原子的杂化轨道类型为 。
(4)化合物D2A的立体构型为 ,中心原子的价层电子对数为 ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为 。
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm, F 的化学式为 :晶胞中A 原子的配位数为 ;列式计算晶体F的密度(g.cm-3) 。