-
某研究小组为测定某软锰矿中MnO2的质量分数,查阅资料获得如下信息:KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化,反应过程表示为:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O,MnO2+C2O42-+4H+=Mn2++2CO2↑+2H2O
小组成员采用滴定的方法测定软锰矿中MnO2的质量分数,设计实验如下:准确称取2.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液转移到100mL容量瓶中并定容;从中分别取出20.00mL待测液置于锥形瓶中,再用0.0200mol·L-1KMnO4标准溶液进行滴定,记录最终读数。数据如下:
测定次序
第一次
第二次
第三次
第四次
初始读数(mL)
0.40
0.10
0.90
0.00
最终读数(mL)
25.05
20.10
21.00
19.90
试回答下列问题:
(1)0.0200mol·L-1KMnO4标准溶液应置于 (选填“酸式”或“碱式”)滴定管中;滴定终点如何判断 。
(2)你能否帮助该研究小组求得软锰矿中MnO2的质量分数 (选填“能”或“否”)。若回答“能”,请给出计算结果 (保留小数点后两位);若回答“否”,试说明原因 。
(3)若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是 。
A.溶液转移至容量瓶中,未将烧杯、玻棒洗涤
B.滴定前尖嘴部分有一气泡,滴定终点时消失
C.定容时,俯视刻度线
D.滴定前仰视读数,滴定后俯视读数
E.锥形瓶水洗之后未用待测液润洗
高二化学填空题困难题查看答案及解析
-
已知:KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化。
测定软锰矿中MnO2质量分数的方法是:称取1.20 g软锰矿样品,加入2.68 g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却,滤去杂质,将所得滤液转移到250mL容量瓶中并定容。从中取出25.00 mL待测液放入锥形瓶中,再用0.0200 mol/L KMnO4标准溶液进行滴定,当滴入20.00 mL KMnO4溶液时恰好完全反应。
回答下列问题:
(1)在酸性条件下,MnO2将Na2C2O4氧化的离子方程式为_____________。
(2)0.0200mol/LKMnO4标准溶液应选用图中的________(填“甲”或“乙”)滴定管;将锥形瓶置于滴定管下方进行滴定时,眼睛注视__________直至滴定终点;判断到达滴定终点的现象是____________。

(3)软锰矿中MnO2的质量分数为_______________。
(4)若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是_____(填选项)。
A.溶液转移至容量瓶中,未将烧杯、玻璃棒洗涤
B.滴定前尖嘴部分有一气泡,滴定终点时消失
C.定容时,俯视刻度线
D.滴定前仰视读数,滴定后俯视读数
高二化学实验题中等难度题查看答案及解析
-
(12分)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组拟用KMnO4溶液滴定的方法,测定该补血剂中铁元素的含量,进行了如下实验:
[查阅资料]
在酸性条件下,用KMnO4标准溶液进行氧化还原滴定,可以测定Fe2+的含量。反应的离子方程式是:Fe2++MnO4-+H+ —— Fe3++Mn2++H2O(未配平)
[准备实验用品]
①仪器:a.电子天平,b.滴定管,c.100mL量筒,d.烧杯,e.漏斗,f.250mL容量瓶,g.锥形瓶,h.玻璃棒,i.药匙,j.烧瓶,k.铁架台(带滴定管夹),l.胶头滴管。
②试剂:a.硫酸亚铁补血剂药片,b.高锰酸钾晶体,c.酚酞溶液,d.KSCN溶液,
e.稀硫酸,f.稀盐酸,g.蒸馏水。
[实验步骤]
①称取0.474 g KMnO4晶体,配成250.00 mL水溶液;
②取5片除去糖衣(非还原糖)后的硫酸亚铁补血剂药片(1.500 g),研细后加稀硫酸溶解,配成100.00 mL水溶液。
③用酸式滴定管取待测“补血剂”溶液20.00mL于某容器中。
④盛装标准KMnO4溶液,静置后,读取数据,记录为KMnO4标准溶液体积的初读数。
⑤滴定,并记录KMnO4标准溶液的终读数。再重复滴定2次。
[实验记录]
滴定次数
实验数据
1
2
3
V(样品)/mL
20.00
20.00
20.00
V(KMnO4)/mL(初读数)
0.00
0.20
0.00
V(KMnO4)/mL(终读数)
15.85
15.22
14.98
[交流与讨论]
(1)准备的实验用品中,不需要的仪器有(填序号)________;不需要的试剂有(填序号)________。
(2)本实验所用的KMnO4标准溶液的物质的量浓度为________。
(3)课外小组里有位同学设计了下列四种滴定方式(夹持部分略去),引起了同学们的讨论,最后取得共识,认为最合理的是________(填字母序号)。
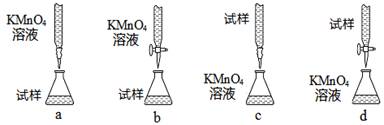
(4)判断滴定终点的依据是________。
(5)根据实验数据,计算该补血剂中铁元素的含量 。
高二化学实验题简单题查看答案及解析
-
某实验小组查阅资料得知:
5C2O42—+2MnO4—+16H+====10CO2↑+2Mn2++8H2O
欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数。该小组称量1.34 g草酸钠样品溶于稀硫酸中,然后用0.200 mol·L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应)。
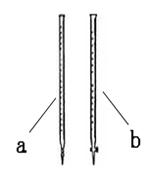
(1)滴定时用______(填a或b)。
(2)滴定管盛装KMnO4标准溶液。滴定前______(填“是”或“否”)滴加指示剂,滴定终点的现象是____________________。
(3)达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为______________。
高二化学实验题中等难度题查看答案及解析
-
(8分)某小组查阅资料得知:C2O42-+MnO4-+H+→ CO2↑+Mn2++H2O(未配平),欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数。该小组称量1.34 g草酸钠样品溶于稀硫酸中,然后用0.200 mol·L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应)。
(1)滴定前是否要滴加指示剂?________(填“是”或“否”),请说明理由________。
(2)滴定时用________(填a或b)滴定管盛装KMnO4标准溶液。
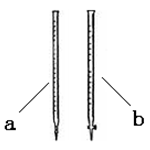
(3)达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为________。
高二化学实验题简单题查看答案及解析
-
乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体中x值.通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
该组同学设计了滴定的方法测定x值.
①称取1.260g纯草酸晶体,将其酸制成100.00mL水溶液为待测液.
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00mL;
请回答:
(1)滴定时,将KMnO4标准液装在右图中的______(填“甲”或“乙”)滴定管中.
(2)本实验滴定达到终点的标志是______.
(3)通过上述数据,计算出x=______.
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会______(填“偏大”、“偏小”或“不变”,下同).
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会______.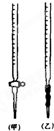
高二化学解答题中等难度题查看答案及解析
-
乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体中x值.通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
该组同学设计了滴定的方法测定x值.
①称取1.260g纯草酸晶体,将其酸制成100.00mL水溶液为待测液.
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00mL;
请回答:
(1)滴定时,将KMnO4标准液装在右图中的______(填“甲”或“乙”)滴定管中.
(2)本实验滴定达到终点的标志是______.
(3)通过上述数据,计算出x=______.
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会______(填“偏大”、“偏小”或“不变”,下同).
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会______.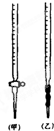
高二化学解答题中等难度题查看答案及解析
-
乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体中x值.通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
该组同学设计了滴定的方法测定x值.
①称取1.260g纯草酸晶体,将其酸制成100.00mL水溶液为待测液.
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00mL;
请回答:
(1)滴定时,将KMnO4标准液装在右图中的______(填“甲”或“乙”)滴定管中.
(2)本实验滴定达到终点的标志是______.
(3)通过上述数据,计算出x=______.
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会______(填“偏大”、“偏小”或“不变”,下同).
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会______.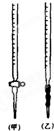
高二化学解答题中等难度题查看答案及解析
-
某化学学习小组的同学欲探究测定草酸晶体中x的值.通过查阅资料该小组同学得知:草酸易溶于水,其水溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.该组同学利用该反应原理设计了滴定的方法测定x值.
①称取1.260g纯草酸晶体,将其制成100.00mL水溶液为待测液.
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,实验记录有关数据如下:
请回答:滴定次数 待测草酸溶液体积(mL) 0.1000mol/LKMnO4标准溶液体积(mL) 滴定前刻度 滴定后刻度 第一次 25.00 0.00 10.02 第二次 25.00 0.22 11.32 第三次 25.00 1.56 11.54
(1)滴定时,将KMnO4标准液装在右图中的______(填“甲”或“乙”)滴定管中.
(2)本实验滴定达到终点的标志可以是______.
(3)通过上述数据,计算出x=______.
(4)①若滴定终点时俯视滴定管刻度,则由此测得的x值会______(填“偏大”、“偏小”或“不变”,下同).
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会______.高二化学解答题中等难度题查看答案及解析
-
乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x值。通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O
该组同学设计了滴定的方法测定x值。
① 称取1.260 g纯草酸晶体,将其酸制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③ 用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL;
请回答:
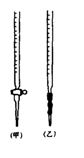
⑴ 滴定时,将KMnO4标准液装在右图中的 (填“甲”或“乙”)滴定管中。
⑵ 本实验滴定达到终点的标志可以是 。
⑶ 通过上述数据,计算出x= 。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会 (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 。
高二化学实验题简单题查看答案及解析