-
为了更深刻地认识卤素的性质,某化学小组对卤素及其化合物的制备和性质进行如下探究实验,根据实验回答问题。
[实验一]氯气的制备
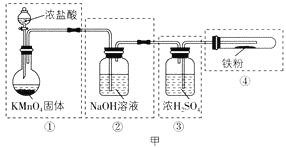
(1)该小组拟用图甲实验装置来制备纯净、干燥的氯气,并完成与金属铁的反应(夹持仪器略去)。每个虚线框表示一个单元装置,请用文字描述将下列装置的错误之处改正:___。
[实验二]探究氯化亚铁与氧气反应的产物
已知氯化亚铁的熔点为674℃,沸点为1023℃;三氯化铁在100℃左右时升华,极易水解。在500℃条件下氯化亚铁与氧气可能发生下列反应:12FeCl2+3O2 2Fe2O3+8FeCl3、4FeCl2+3O2
2Fe2O3+8FeCl3、4FeCl2+3O2 2Fe2O3 +4Cl2,该化学小组选用图乙部分装置(装置可以重复选用)进行氯化亚铁与氧气反应产物的探究。
2Fe2O3 +4Cl2,该化学小组选用图乙部分装置(装置可以重复选用)进行氯化亚铁与氧气反应产物的探究。
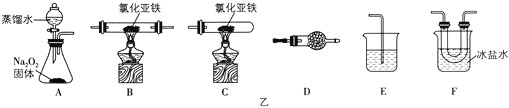
(2)实验装置的合理连接顺序为A→___→E。
(3)简述将装置F中的固体配成溶液的操作方法:___。
[实验三]卤素化合物之间反应的实验条件控制探究
(4)在不同实验条件下KClO3可将KI氧化为I2或KIO3。该小组同学设计的一组实验的数据记录如下表(实验控制在室温下进行):
| 试管标号 | 1 | 2 | 3 | 4 |
| 0.20mol•L-1KI溶液/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4溶液/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 | | | | |
①该组实验的目的是___。
②2号试管反应完全后,取少量试管中的溶液,滴加淀粉溶液后显蓝色,假设还原产物只有KCl,写出反应的离子方程式:___。
-
为了更深刻地认识卤素的性质,某化学小组对卤素及其化合物的制备和性质进行如下探究实验,根据实验回答问题。
[实验一]氯气的制取
(1)该小组拟用下图实验装置来制备纯净、干燥的氯气,并完成与金属铁的反应(夹持仪器略去,下同)。每个虚线框表示一个单元装置,请用文字描述将下列装置的错误之处改正___________。
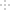
[实验二]探究氯化亚铁与氧气反应的产物
已知氯化亚铁的熔点为674℃,沸点为1023℃;三氯化铁在100℃左右时升华,极易水解。在500℃条件下氯化亚铁与氧气可能发生下列反应,12FeCl2+3O2 2Fe2O3+8FeCl3、4FeCl2+3O2
2Fe2O3+8FeCl3、4FeCl2+3O2 2Fe2O3+4Cl2,该化学小组选用下图部分装置(装置可以重复选用)进行氯化亚铁与氧气反应产物的探究。
2Fe2O3+4Cl2,该化学小组选用下图部分装置(装置可以重复选用)进行氯化亚铁与氧气反应产物的探究。

(2)实验装置的合理连接顺序为:A→_____________→E。
(3)假设加热装置中的完全反应,则反应后剩余固体的化学式是_______________。请设计实验方案验证你的假设____________________。
(4)简述将F中的固体配成溶液的操作方法__________________。
[实验三]卤素化合物之间反应实验条件控制探究
(5)在不同实验条件下KClO3可将KI 氧化为I2 或KIO3。下面是该小组设计的一组实验数据记录表(实验控制在室温下进行):
| 试管标号 | 1 | 2 | 3 | 4 |
| 0.20 mol· L-1KI 溶液/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0. 10 | 0. 10 | 0.10 | 0.10 |
| 6.0 mol· L-1 H2SO4溶液/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 | | | | |
①该组实验的目的是_______________。
②2号试管反应完全后,取少量2号试管中的溶液滴加淀粉溶液后显蓝色,假设还原产物只有KCl,写出反应的离子方程式____________________。
-
某化学兴趣小组进行有关卤素及其化合物的制备和性质探究实验,请同学们参与他们的实验并回答下列问题。
【实验一】氯气的制备与性质
(1)用下图所示的实验装置来制备纯净、干燥的氯气,并完成它与金属铁的反应。每个虚线框表示一个单元装置,其中有错误的是_____(填字母序号)。
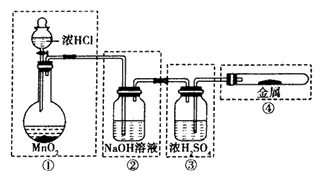
A.只有②和④ B.只有② C.只有①和③ D.②③④
【实验二】卤素化合物的性质实验探究
已知氯化亚铁的熔点674℃、沸点1023℃;三氯化铁在100℃左右时升华,易溶于水并且有强烈的吸水性。在500℃条件下氯化亚铁与氧气可能发生多种反应,如:12FeCl2+3O2 2Fe2O3+8FeCl3、4FeCl2+3O2
2Fe2O3+8FeCl3、4FeCl2+3O2 2Fe2O3+4Cl2等。该兴趣小组选用以下部分装置(夹持装置省略,装置不可重复选用)进行氯化亚铁与氧气反应产物的探究。
2Fe2O3+4Cl2等。该兴趣小组选用以下部分装置(夹持装置省略,装置不可重复选用)进行氯化亚铁与氧气反应产物的探究。
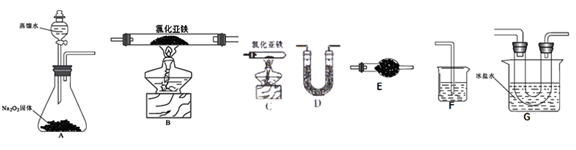
(2)实验装置的合理连接顺序为:A→____________→F。
(3)A装置中反应的化学方程式为________________。
(4)当加热装置中充分反应后,余下的固体是_________;本套实验装置的主要缺点是_____________。
(5)利用反应生成的FeCl3设计实验证明Fe(OH)3是弱碱,实验方案为____________。
【实验三】卤素化合物反应实验条件控制探究
(6)在不同实验条件下KClO3可将KI氧化为I2或KIO3。该小组设计了一系列实验来研究反应条件对反应物的影响,其中某一实验的数据记录如下(实验控制在室温下进行):
| 试管标号 | 1 | 2 | 3 | 4 |
| 0.20mol·L-1KI溶液/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol/L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 | | | | |
①该组实验的目的是________________________。
②设计1号试管实验的作用是_______________________。
③若2号试管实验现象为“反应后溶液呈黄色”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为__________________。
-
某化学小组对卤素及其化合物的制备和性质进行如下探究实验,根据实验回答问题。
I.探究氯化亚铁与氧气反应的产物
已知氯化亚铁的熔点为674℃,沸点为1023℃;三氯化铁在100℃左右时升华,极易水解。在500℃条件下氯化亚铁与氧气可能发生下列反应:12FeCl2+3O2 2Fe2O3+8FeCl3,4FeCl2+3O2
2Fe2O3+8FeCl3,4FeCl2+3O2 2Fe2O3+4Cl2。该化学小组选用如图部分装置(装置可以重复选用)进行氯化亚铁与氧气反应产物的探究。
2Fe2O3+4Cl2。该化学小组选用如图部分装置(装置可以重复选用)进行氯化亚铁与氧气反应产物的探究。
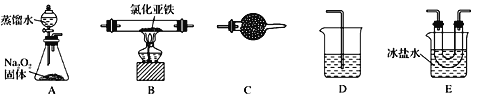
(1)实验装置的合理连接顺序为:A→__________→D,装置E的作用是___________。
(2)D中发生反应的离子方程式_______。
(3)某化学兴趣小组在控制在500℃下发生反应,一段时间后的产物进行了如下实验探究:
①对B中反应剩余固体的成分开展实验探究,并作出以下两种假设:
假设一:产物为Fe2O3;
假设二:产物为________(填化学式)。
以下针对上述假设一,展开实验研究,请完善下面表格:
| 实验操作 | 预期现象与结论 |
| 取少量固体样品于一支洁净的试管中,加入足量的蒸馏水。 | ______,则假设一成立,否则,假设一不成立。 |
②对固体产物(标准状况下)成分含量进行了如下实验探究:B中反应剩余固体的质量经测定为m1g ,E中生成物的质量经测定为m2g。B中反应剩余固体按探究①的实验步骤进行操作,并最终得到干燥纯净的固体质量为m3g。则固体产物中Fe2O3所占的质量分数为______。
Ⅱ.卤素化合物之间反应实验条件控制探究
(4)室温下,KClO3可将KI氧化为I2或KIO3。下面是该小组设计的一组实验数据记录表:
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20 mol·L-1KI溶液/ mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0 mol·L-1H2SO4溶液/ mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
| 反应完全后,滴加2滴淀粉溶液 | 无色 | 蓝色 | 蓝色较2浅 | 无色 |
①根据实验数据,结合所学化学知识,下列说法正确的是______
A.该实验目的是探究其它条件相同时,酸的浓度对反应产物的影响
B.实验1和实验4说明硫酸浓度太低或太浓,KClO3与KI均不反应
C.实验2的现象说明在该硫酸浓度下KClO3将KI氧化为I2
D.实验3蓝色较2浅的原因是在该硫酸浓度下淀粉部分水解
②2号试管反应完全后,假设还原产物只有KC1,写出反应的离子方程式___________。
-
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
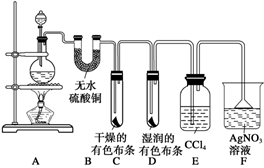
(1)下列方法中,可制得氯气的正确组合是________。
①MnO2和浓盐酸混合共热
②KMnO4和浓盐酸混合 ③氯酸钠和浓盐酸混合 ④K2Cr2O7和浓盐酸混合
A.①②③ B.①②④ C.①② D.全部可以
(2)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积(标准状况下)总是小于1.12 L的原因是。
(3)①装置B的作用是________,现象是________。
②装置C和D出现的不同现象说明的问题是________。
③装置E的作用是________
目前我国饮用水消毒主要用氯——通氯气,加漂白粉或漂白精。
(1) 漂白粉或漂白精长期放置于空气中会变质失效,其化学方程式是__________________。
(2)目前我国广泛采用经过干燥空气稀释的氯气,通入填有固体亚氯酸钠(NaClO2)的柱内
制得ClO2,这一反应的化学方程式是:_________________________________________。
-
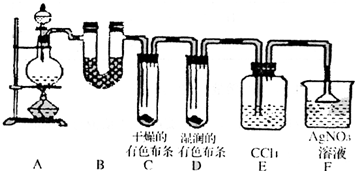
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题.
(1)下列方法中,可制得氯气的正确组合是______.
①MnO2和浓盐酸混合共热②MnO2、NaCl和浓硫酸混合共热
③次氯酸钠和浓盐酸混合④K2Cr2O7和浓盐酸混合
⑤KClO3和浓盐酸混合共热⑥KMnO4和浓盐酸混合
A.①②⑥;B.②④⑥;C.①④⑥;D.全部可以
(2)若用含有0.2mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12L的原因是______
(3)①装置B的作用是______,现象是______.
②装置C和D出现的不同现象说明的问题是______.
③装置E的作用是______.
④写出装置F中发生反应的离子方程式______.
(4)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种.为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置.你认为该装置应加在______与______之间(填装置字母序号),装置中应放入______.
-
某校化学实验兴趣小组为了探究在实验室制备 Cl2 的过程中有水蒸气和 HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置 ( 支撑用的铁架台省略 ),按要求回答问题.
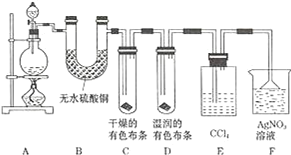
(1)下列方法中,可制得氯气的正确组合是___.(已知酸性条件下,K2Cr2O7、KClO3的氧化性均强于Cl2;酒精灯可以不用)
①MnO2 和浓盐酸混合共热; ②次氯酸钠和浓盐酸混合;③K2Cr2O7 和浓盐酸混合; ④KClO3 和浓盐酸混合共热;⑤KMnO4和浓盐酸混合;
A 只有① B 只有①⑤ C 只有①③④⑤ D 全部可以
(2)若用含有 0.2mol HCl 的浓盐酸与足量的 MnO2 反应制 Cl2,制得的 Cl2 体积 ( 标准状况下 )总是小于1.12L的原因是___.
(3)装置 B 的作用____,现象是____.
(4)装置 C 和 D 出现的不同现象说明的问题是___、装置 E 的作用是____.
(5)写出装置 F 中发生反应的离子方程式____.
(6)乙同学认为甲同学的实验有缺陷,不能确保最终通入 AgNO3 溶液中的气体只有一种.为了确保实验结论的可靠性,证明最终通入 AgNO3 溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置.你认为该装置应加在__与__之间 ( 填装置字母序号 ),装置中应放入___.
-
(10分)某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.
(1)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12 L的原因是___________________________________________.
(2)①装置B中盛放的试剂名称为________________,作用是____________________________,
现象是____________________________________________________________.
②装置D和E中出现的不同现象说明的问题是_________________________________
③装置F的作用是________________________________________________________.
④写出装置G中发生反应的离子方程式______________________________________
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种.为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置.你认为该装置应加在________与________之间(填装置字母序号),装置中应放入________(填写试剂或用品名称).
-
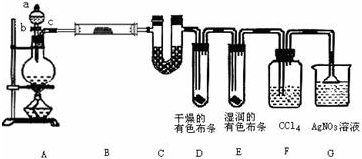
某化学实验小组为了探究在实验室制备Cl2的过程中有 水蒸气和 HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置.按要求回答问题.
(1)如何检查装置A气密性?______写出装置A中反应的离子方程式______ Mn2++Cl2↑+2H2O
-
某小组探究“地康法制氯气”的原理并验证Cl2的性质,设计实验如下(夹持装置略去)请回答下列问题:
Ⅰ.Cl2的制备。
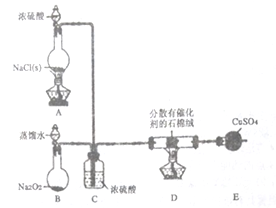
(1)装置B中发生反应的化学方程式为________________。
(2)装置C 的作用除干燥气体外还有______________________。
(3)装置E 中盛放CuSO4 的仪器名称为___________;反应开始后,硫酸铜变蓝,则装置D中发生反应的化学方程式为________________。
Ⅱ.Cl2性质的验证。
该小组用实验Ⅰ中制得的Cl2和如图所示装置(不能重复使用) 依次验证干燥纯净的Cl2无漂白性、湿润的Cl2有漂白性、Cl的非金属性强于S
查阅资料:
①PdCl2溶液捕获CO 时,生成金属单质和两种酸性气体化合物,同时,溶解度大的气体难逸出;
②少量CO2不干扰实验;
③该实验条件下,C与Cl2不反应。
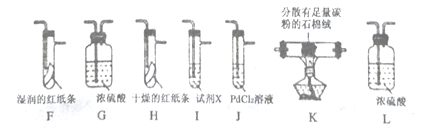
(4)按气流从左到右的方向,装置连接的合理顺序为
E→G→K→ → → → → →尾气处理(填装置字母)。_________
(5)试剂X 的名称为_______________。
(6)装置J中发生反应的化学方程式为______________。
(7)设计实验证明经净化后的Cl2中不含HCl:________________。
2Fe2O3+8FeCl3、4FeCl2+3O2
2Fe2O3+4Cl2,该化学小组选用下图部分装置(装置可以重复选用)进行氯化亚铁与氧气反应产物的探究。











