-
兴趣小组在实验室用制备的氯气与一氧化氮在常温常压下合成亚硝酰氯。
【查阅资料】 亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃) 是一种黄色气体,液体状态呈红褐色,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。对眼睛、皮肤和粘膜有强烈刺激性,具有类似氯气和氮氧化物的毒作用。冰水中加入NaCl可降低温度。
【原料制备】 在实验室分别制备原料气NO和Cl2。
(1)用如下装置制备纯净干燥的气体,请补充下表中各仪器中的试剂。

| 原料制备 | 装置Ⅰ | 装置Ⅰ | 装置Ⅱ |
| 烧瓶中 | 分液漏斗中 |
| 制备纯净Cl2 | MnO2 | ①__________ | ②______ |
| 制备纯净NO | Cu | ③_______ | ④_________ |
【合成亚硝酰氯】 利用制得的NO和Cl2制备NOCl,装置如图所示:
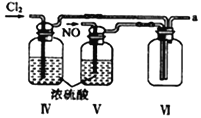
(2)装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是___________________。
(3)装置连顺序为 a→_______________(按气流自左向右方向,用小写字母表示)。
(4)装置Ⅴ的作用是___________________________________。
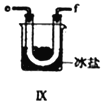
(5)装置Ⅸ在实验时,预期观察到的现象是__________________________________________。
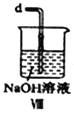
(6)装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为________________________。
【拓展学习】
(7)查阅资料,得知配制王水(浓硝酸与浓盐酸的混酸) 时会生成亚硝酰氯和氯气,该反应的化学方程式为__________________________________。
-
兴趣小组在实验室用制备的氯气与一氧化氮在常温常压下合成亚硝酰氯。
【查阅资料】 亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃) 是一种黄色气体,液体状态呈红褐色,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。对眼睛、皮肤和粘膜有强烈刺激性,具有类似氯气和氮氧化物的毒作用。冰水中加入NaCl可降低温度。
【原料制备】 在实验室分别制备原料气NO和Cl2。
(1)用如下装置制备纯净干燥的气体,请补充下表中各仪器中的试剂。
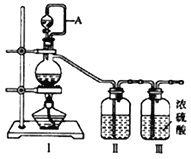
| 原料制备 | 装置Ⅰ | 装置Ⅰ | 装置Ⅱ |
| 烧瓶中 | 分液漏斗中 |
| 制备纯净Cl2 | MnO2 | ①__________ | ②______ |
| 制备纯净NO | Cu | ③_______ | ④_________ |
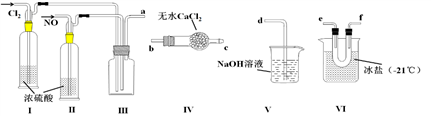
【合成亚硝酰氯】 利用制得的NO和Cl2制备NOCl,装置如图所示:
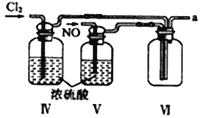
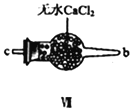
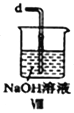
(2)装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是___________________。
(3)装置连顺序为 a→_______________(按气流自左向右方向,用小写字母表示)。
(4)装置Ⅴ的作用是___________________________________。
(5)装置Ⅸ在实验时,预期观察到的现象是__________________________________________。
(6)装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为________________________。
【拓展学习】
(7)查阅资料,得知配制王水(浓硝酸与浓盐酸的混酸) 时会生成亚硝酰氯和氯气,该反应的化学方程式为__________________________________。
-
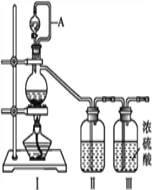
亚硝酰氯(NOCl)是一种黄色气体,熔点为-64.5 ℃,沸点为-5.5 ℃,遇水易水解,可用于合成清洁剂、触媒剂等。实验室可由氯气与一氧化氮在常温常压下制备亚硝酰氯。某同学利用纯净的NO和Cl2制备NOCl,装置如下图所示。(已知:Cl2的熔点为-101 ℃,沸点为-34 ℃;NO的熔点为-163.6 ℃,沸点为-151 ℃)
(1)装置连接顺序为a→_______________________(按气流方向,用小写字母表示)。
(2)装置I和II除可进一步干燥NO和Cl2外,另一个作用是____________________。
(3)装置IV的作用是_________________________________,当使用该装置干燥气体时,通常
是b口进气,c口出气,原因是__________________________________。
(4)装置V中吸收尾气时,NOCl发生反应的化学方程式为_________________________。
(5)在实际实验操作中,Cl2和NO通入比例略大于1:2,这样做的原因是_________________。
(6)已知王水是浓硝酸与浓盐酸的混酸,一定条件下该混酸可生成亚硝酰氯和一种常见有色气体,该反应的化学方程式为____________________________。
-
亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。制备装置如下图所示:(其中Ⅲ、Ⅳ、Ⅴ中都为浓硫酸)
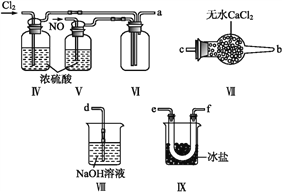
(1)用同一装置Ⅰ、Ⅱ、III分别制备纯净干燥的NO和Cl2,下表中缺少的药品是:
| 装置Ⅰ | 装置Ⅱ |
| 烧瓶中 | 分液漏斗中 |
| 制备纯净Cl2 | MnO2 | 浓盐酸 | ①___ |
| 制备纯净NO | Cu | ②___ | 水 |
(2)A的作用____________________________。
(3)NOCl的电子式_________。
(4)利用制得的NO和Cl2制备NOCl,方程式:2NO + Cl2 = 2NOCl;装置如上图所示:
①装置连接顺序为a→________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________。
③装置Ⅷ中吸收尾气时,Cl2发生反应的离子方程式为________________。
(5)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下该混酸可生成亚硝酰氯和氯气,该反应的化学方程式为__________________。
-
亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:
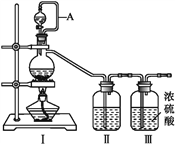
为制备纯净干燥的气体,下表中缺少的药品是:
| 装置Ⅰ | 装置Ⅱ |
| 烧瓶中 | 分液漏斗中 |
| 制备纯净Cl2 | MnO2 | ①___ | ②___ |
| 制备纯净NO | Cu | ③___ | ④___ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
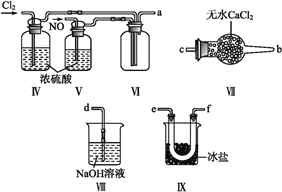
①装置连接顺序为a→________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________。
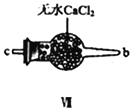
③装置Ⅶ的作用是____________。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下该混酸可生成亚硝酰氯和氯气, 该反应的化学方程式为__________________。
-
亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:
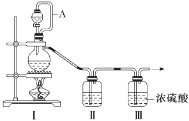
为制备纯净干燥的气体,补充下表中缺少的药品。
| 装置Ⅰ | 装置Ⅱ |
| 烧瓶中 | 分液漏斗中 |
| 制备纯净的Cl2 | MnO2 | ①________ | ②________ |
| 制备纯净的NO | Cu | ③________ | ④________ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
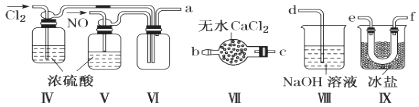
①装置连接顺序为a→________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________________。
③装置Ⅶ的作用是________________________________________________________。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为______________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为_______________________________________。
-
亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:
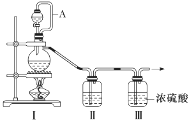
为制备纯净干燥的气体,补充下表中缺少的药品。
| 装置Ⅰ | 装置Ⅱ |
| 烧瓶中 | 分液漏斗中 |
| 制备纯净的Cl2 | MnO2 | ①________ | ②________ |
| 制备纯净的NO | Cu | ③________ | ④________ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
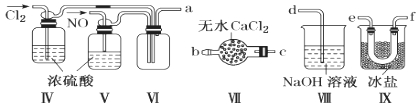
①装置连接顺序为a→________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________________。
③装置Ⅶ的作用是________________________________________________________。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为______________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为_______________________________________。
-
亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:
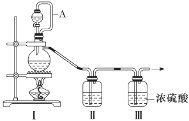
为制备纯净干燥的气体,补充下表中缺少的药品。
| 装置Ⅰ | 装置Ⅱ |
| 烧瓶中 | 分液漏斗中 |
| 制备纯净的Cl2 | MnO2 | ①________ | ②________ |
| 制备纯净的NO | Cu | ③________ | ④________ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
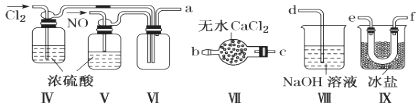
①装置连接顺序为a→________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________________。
③装置Ⅶ的作用是________________________________________________________。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为______________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为_______________________________________。
-
亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:
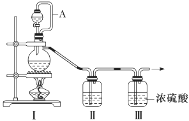
为制备纯净干燥的气体,补充下表中缺少的药品。
| 装置Ⅰ | 装置Ⅱ |
| 烧瓶中 | 分液漏斗中 |
| 制备纯净的Cl2 | MnO2 | ①________ | ②________ |
| 制备纯净的NO | Cu | ③________ | ④________ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
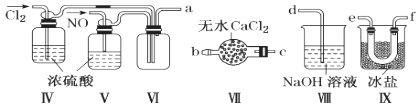
①装置连接顺序为a→________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________________。
③装置Ⅶ的作用是________________________________________________________。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为______________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为_______________________________________。
-
亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:
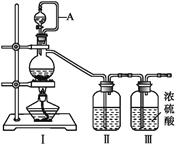
为制备纯净干燥的气体,下表中缺少的药品是:
| 装置Ⅰ | 装置Ⅱ |
| 烧瓶中 | 分液漏斗中 |
| 制备纯净Cl2 | MnO2 | ①___ | ②___ |
| 制备纯净NO | Cu | ③___ | ④___ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
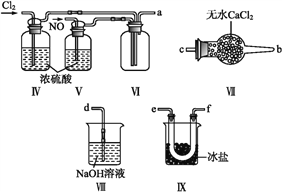
①装置连接顺序为a→________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________。
③装置Ⅶ的作用是____________。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下该混酸可生成亚硝酰氯和氯气, 该反应的化学方程式为__________________。
























