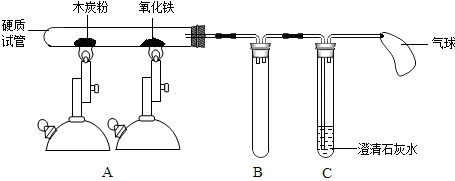
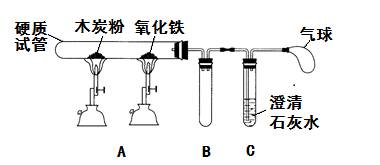
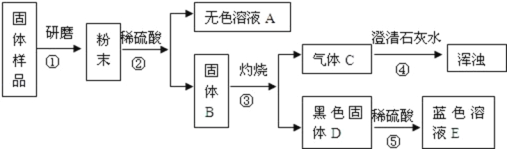
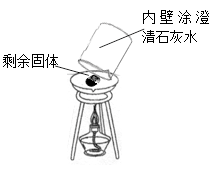
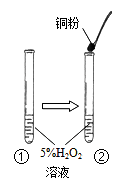
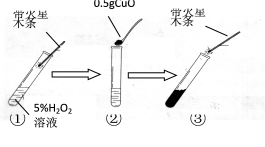
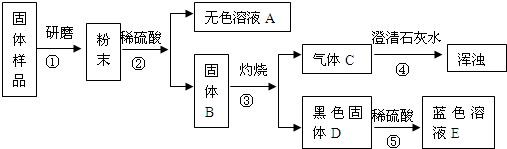
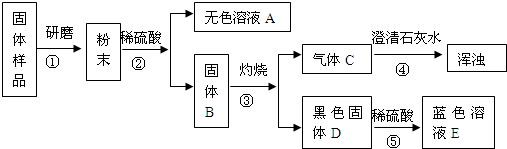
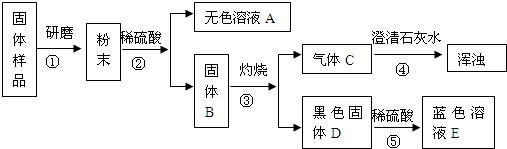
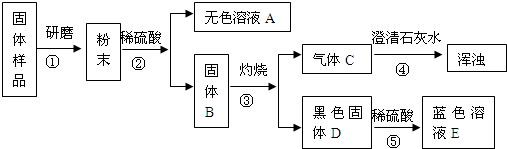
某班同学取用相同总质量的木炭粉和氧化铜的混合物,按图示装置进行实验。实验过程中发现有的小组“黑色固体变红色”这一实验现象不明显。小组同学对此异常现象进行如下探究。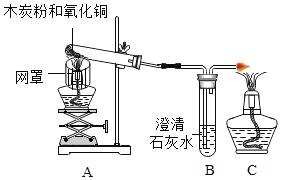
(知识回忆)碳和氧化铜反应的化学方程式为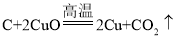 ,理论上碳和氧化铜的质量比为_____。
,理论上碳和氧化铜的质量比为_____。
(作出猜想)产生异常现象可能与所取用木炭粉和氧化铜的质量比有关。
(实验探究)小组同学用总质量相同但质量比不同的木炭粉和氧化铜的混合物(不考虑其中杂质),分别进行实验,部分实验现象记录如下:
| 实验序号1 | m(C):m(CuO) | 实验后A处试管中固体颜色 | C处导管口的现象 |
| 1 | 1:8 | 红色固体中有少量黑色固体 | 尾气燃烧 |
| 2 | 1:9 | 红色固体中有较少量黑色固体 | 尾气燃烧 |
| 3 | 1:10 | 红色固体中有很少量黑色固体 | 尾气不燃烧 |
| 4 | 1:11 | 红色固体中有极少量黑色固体 | _____ |
| 5 | 1:12 | 红色固体中无黑色固体 | 尾气不燃烧 |
| 6 | 1:13 | 红色固体中有较多黑色固体 | 尾气不燃烧 |
(交流讨论)
(1)推测实验4中“C处导管口的现象”是_____。
(2)上述探究可得出,实验时所用木炭粉和氧化铜的质量比控制在1:10~1:12之间,可观察到黑色固体明显变红,同时还可减少_____(填化学式)排放,防止空气污染。
(3)检验实验6反应后A处试管中黑色固体物质,可滴加的试剂是_____,观察到的现象是_____。
(反思评价)分析发现,实验5中m(C):m(CuO)比值与理论值不符,实验后却无黑色固体残留。请用化学方程式解释实验中过量的黑色固体消失的原因:_____(写一个即可)。
九年级化学科学探究题中等难度题