-
下列关于晶格能的说法中正确的是( )
A.晶格能指形成1 mol离子键所放出的能量
B.晶格能指破坏1 mol离子键所吸收的能量
C.晶格能指1 mol离子化合物中的阴、阳离子由相互远离的气态离子结合成离子晶体时所放出的能量
D.晶格能的大小与晶体的熔点、硬度都无关
高二化学单选题简单题查看答案及解析
-
有关晶格能的叙述不正确的是( )
A.1mol气态金属阳离子离子和1mol气态阴离子离子结合生成1mol离子晶体时释放出的热能为离子晶体的晶格能
B.晶格能通常取正值
C.晶格能越大,形成的离子晶体越稳定
D.晶格能越大,物质的硬度反而越小
高二化学单选题简单题查看答案及解析
-
已知反应A+B=C+D的能量变化如图所示(E1、E2均为正值),下列说法正确的是
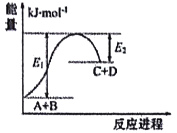
A. 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
B. 该反应吸收的能最为(E1-E2)
C. A和B的总能量一定高于C和D的总能量
D. 该反应只有在加热条件下才能进行
高二化学单选题简单题查看答案及解析
-
下列说法或表示方法正确的是
A. 吸热反应中,新化学键形成吸收能量;放热反应中,新化学键形成放出能量
B. 等质量的硫蒸气和硫磺(S)分别完全燃烧,后者放出的热量多
C. 相同体积、浓度均为0.1 mol/L的盐酸和醋酸溶液分别与足量的NaOH稀溶液反应,前者放出热量多
D. 氢气的燃烧热为285. 8 kJ·mol-1,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)==2H2O(l) △H=-285.8 kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
下列说法不正确的是( )
A. 含有离子键和共价键的化合物一定是离子化合物
B. Na投入到水中,有共价键的断裂与形成
C. 液态水转变为气态水需要吸热,说明旧键断裂吸收的能量大于新键形成放出的能量
D. N2和NCl3两种分子中,每个原子的最外层都具有8电子稳定结构
高二化学选择题中等难度题查看答案及解析
-
Ⅰ. (1)下列条件的改变能增大活化分子百分数的是_____________。
A.增大压强 B.增大反应物的浓度
C.升高温度 D.使用催化剂
(2)破坏(或形成)1 mol化学键所吸收(或放出)的能量称为键能。已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P 198、Cl-Cl 243、P-Cl 331。
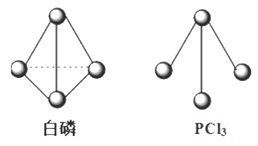
则反应P4(s,白磷)+6Cl2(g)=4PCl3(s)的反应热△H=__________kJ·mol-1。
Ⅱ.2SO2(g)+O2(g)
2SO3(g)反应过程的能量变化如图所示。

已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99 kJ·mol-1。请回答下列问题:
(1)图中C表示___________,E表示______________;该反应通常用V2O5作催化剂,加V2O5会使图中B点降低,理由是____________ ;
(2)图中△H=_________kJ·mol-1。
高二化学填空题中等难度题查看答案及解析
-
下列说法正确的是( )
A.生成物的总能量大于反应物的总能量时,该反应一定是吸热反应
B.形成化学键所吸收的总能量大于破坏化学键所放出的总能量时,该反应是吸热反应
C.硫与铁粉在加热条件下反应生成硫化亚铁,固该反应是吸热反应
D.反应热与反应物、生成物的状态有关;与化学反应方程式的计量系数无关高二化学选择题中等难度题查看答案及解析
-
下列说法正确的是( )
A. 由H原子形成1 mol H—H键要吸收热量
B. N2性质非常稳定,是因为N2分子中含有氮氮三键,要破坏氮氮三键需吸收更多的能量
C. 在稀溶液中,酸与碱发生中和反应生成H2O时所释放的热量称为中和热
D. 伴有能量变化的物质变化都是化学变化
高二化学单选题简单题查看答案及解析
-
某一化学反应在不同催化剂条件下的能量变化曲线如图所示。下列说法正确的是

A.化学催化比酶催化的效果好
B.反应物总能量低于生成物总能量
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.使用不同催化剂可以改变反应的反应热
高二化学选择题中等难度题查看答案及解析
-
下列说法或表示方法中正确的是( )
A.吸热反应中,新化学键形成吸收能量;放热反应中,新化学键形成放出能量
B.等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多
C.相同体积浓度均为0.1 mol/L 盐酸和醋酸溶液分别与足量的NaOH稀溶液反应,前者放出热量多
D.氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)===2H2O(l) ΔH=-285.8 kJ/mol
高二化学选择题简单题查看答案及解析