-
按F、Cl、Br、I顺序递增的是
A. 最外层电子数 B. 第一电离能
C. 非金属性 D. 原子半径
高二化学单选题简单题查看答案及解析
-
按F、Cl、Br、I顺序递增的是( )
A. 外围电子 B. 第一电离能 C. 电负性 D. 原子半径
高二化学单选题中等难度题查看答案及解析
-
金属钠元素、钴元素在工业上有重要的应用。请回答下列问题:
(1)Ca大于Co的是________(填标号)
A. 最外层电子数 B. 原子半径
C. 第一电离能 D. 未成对电子数
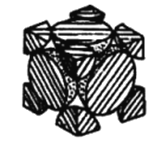
(2)经X射线衍射法测定发现,晶体钴在417℃以上堆积方式的剖面图如图所示,则该堆积方式属于_____,若该堆积方式下的晶胞参数为a cm,则钴原子的半径为______pm。
(3)Co3+氧化性极强,在水溶液中易被还原成Co2+,而在氨水中可稳定存在,其原因是________。
(4)已知:配合物中,配位体中含有一个配位原子的配体称为单齿配体;一个配体中有两个或两个以上配位原子的配体称为多齿配体。[Co(NO3—)4]2—中Co2+的配位数为4,该配离子中各元素第一电离能由大到小的顺序_______(填元素符号),1mol该离子中含σ键数目为_________。
(5)①Co的某配合物化学式为CoCl3·3NH3,为八面体结构,其中极性分子有___种。
②该配合物在热NaOH溶液中发生反应产生沉淀,并释放出气体,该反应的化学方程式_________。
(6)NaCl晶体在50~300GPa的高压下和Cl2反应,可以形成一种新晶体,其立方晶胞如下图所示(大球为Cl,小球为Na)。
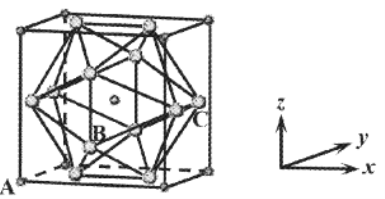
①若A的原子坐标为(0,0,0),C的原子坐标为(1,
,
),则B的原子坐标为________。
②晶体中,Cl构成的多面体包含_____个三角形的面,与Cl紧邻的Na个数为______。
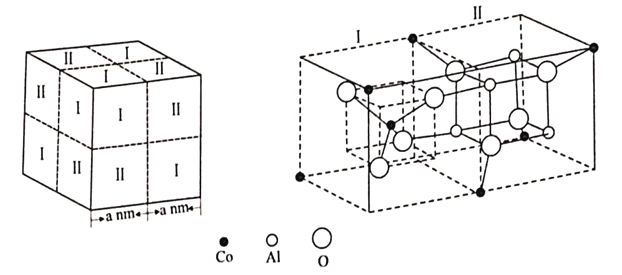
(7)钴蓝晶体结构如下图,该立方晶胞由I型和II型小立方体各4个构成,其化学式为_____,晶体中Al3+占据O2—形成的_____面体空隙,NA为阿伏伽德罗常数的值,设化学式对应的摩尔质量为Mg/mol,则钴蓝晶体的密度计算式为_________g/cm3。
高二化学综合题困难题查看答案及解析
-
按C、N、O、F的顺序,其性质表现为递减的是( )
A.最外层电子数 B.原子半径
C.非金属性 D.单质的氧化性
高二化学单选题简单题查看答案及解析
-
短周期金属元素甲-戊在元素周期表中的相对位置如表所示,下列判断正确的是
甲
乙
丙
丁
戊
A.原子半径:丙<丁<戊 B. 第一电离能:甲>丙
C.电负性:丙>丁>戊 D. 最外层电子数:甲>乙
高二化学选择题中等难度题查看答案及解析
-
随着原子序数的递增,不呈周期性变化的是
A.元素的相对原子质量 B.元素化合价
C.元素原子的最外层电子排布 D.元素原子半径
高二化学单选题简单题查看答案及解析
-
如图表示1~18号元素(原子)的结构或性质随核电荷数递增的变化.该图中,纵坐标表示( )
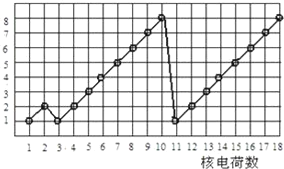
A.原子半径 B.电子层数 C.最高化合价 D.最外层电子数
高二化学单选题中等难度题查看答案及解析
-
下列说法正确的是
A.在所有元素中,氟的第一电离能最大
B.处于最低能量的原子叫做基态原子
C.原子半径最小的氢元素的电负性最大
D.最外层电子数为8的都是稀有气体元素的原子
高二化学单选题简单题查看答案及解析
-
元素性质呈周期性变化的决定因素是
A.元素相对原子质量依次递增
B.元素的最高正化合价呈周期性变化
C.元素原子最外层电子排布呈周期性变化
D.元素金属性或非金属性呈周期性变化
高二化学选择题中等难度题查看答案及解析
-
下列各组元素性质递变情况正确的是( )
A. Fe、Cu、Zn原子最外层电子数依次增多
B. N、O、F元素最高正化合价依次升高
C. P、S、Cl第一电离能依次增大
D. Na、K、Rb的金属性依次增强
高二化学选择题中等难度题查看答案及解析