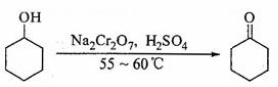-
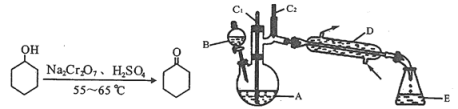
实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略)如下:
有关物质的物理性质见下表。
| 物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
| 环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 1.0 | |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10 mL环己醇的A中,在55 ~ 60℃进行反应。反应完成后,加入适量水,蒸馏,收集95 ~ 100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称为____________________________。
(2)酸性Na2Cr2O7溶液氧化环己醇反应的 ,反应剧烈将导致体系温度迅速上升,副反应增多。
,反应剧烈将导致体系温度迅速上升,副反应增多。
①滴加酸性Na2Cr2O7溶液的操作为____________________________________________;
②蒸馏不能分离环己酮和水的原因是__________________________________________。
(3)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加人无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是________________________________________________;
②B中水层用乙醚萃取的目的是______________________________________________;
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有__________,操作d中,加入NaC1固体的作用是_____________________________。
(4)恢复至室温时,分离得到纯产品体积为6 mL,则环已酮的产率为____________。(计算结果精确到0.1%)
-
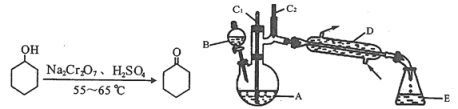
实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略)如下:
有关物质的物理性质见下表。
| 物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
| 环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 1.0 | |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10 mL环己醇的A中,在55 ~ 60℃进行反应。反应完成后,加入适量水,蒸馏,收集95 ~ 100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称为____________________________。
(2)酸性Na2Cr2O7溶液氧化环己醇反应的 ,反应剧烈将导致体系温度迅速上升,副反应增多。
,反应剧烈将导致体系温度迅速上升,副反应增多。
①滴加酸性Na2Cr2O7溶液的操作为____________________________________________;
②蒸馏不能分离环己酮和水的原因是__________________________________________。
(3)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是________________________________________________;
②B中水层用乙醚萃取的目的是______________________________________________;
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有__________,操作d中,加入NaC1固体的作用是_____________________________。
(4)恢复至室温时,分离得到纯产品体积为6 mL,则环已酮的产率为____________。(计算结果精确到0.1%)
-
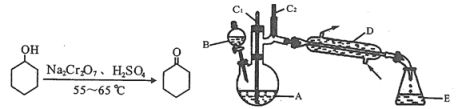
实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略去)如下:
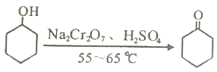
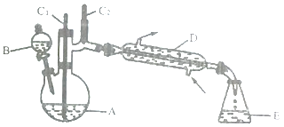
有关物质的物理性质见下表。
| 物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
| 环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 1.0 | |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中,在55~60℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的的名称是为__________________。
(2)酸性Na2Cr207溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多。
①如何滴加酸性Na2Cr2O7溶液__________________________________;
②蒸馏不能分离环己酮和水的原因是_____________________________________。
(3)环己酮的提纯需要经过以下一系列的操作:
a. 蒸馏、除去乙醚后,收集151~156℃馏分
b. 水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c. 过滤
d. 往液体中加入NaCl固体至饱和,静置,分液
e. 加入无水MgSO4固体,除去有机物中少量的水
① 上述提纯步骤的正确顺序是______________________________;
② b中水层用乙醚萃取的目的是______________________________________;
③ 上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有_____________,操作d中,加入NaCl固体的作用是______________________________。
(4)恢复至室温时,分离得到纯产品体积为6mL,则环己酮的产率为______________。
-
实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略去)如下:
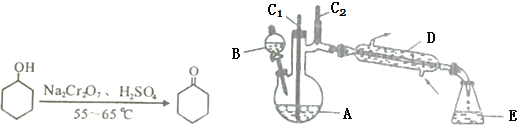
有关物质的物理性质见下表。
| 物质 | 沸点(℃) | 密度(g/cm3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
| 环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 1.0 | |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中,在55~65℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)仪器D的名称为_____。
(2)①滴加酸性Na2Cr2O7溶液时反应的离子方程式为______________;
②蒸馏不能分离环己酮和水的原因是_____。
(3)环己酮需要经过以下操作提纯:
a.往液体中加入NaCl固体至饱和,静置,分液
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.加入无水MgSO4固体,除去有机物中少量的水
d.过滤
e.蒸馏、除去乙醚后,收集151~156℃馏分
①b中水层用乙醚萃取的目的是_____;
②上述操作a、d中使用的玻璃仪器除烧杯、玻璃棒外,还需要的玻璃仪器有____、___,操作a中,加入NaCl固体的作用是_____。
(4)恢复至室温时,分离得到纯产品体积为8mL,则环己酮的产率为____。(保留3位有效数字)
-
实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略去)如下:
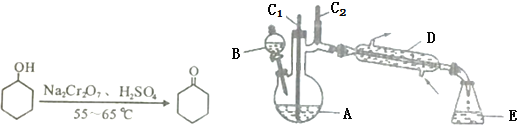
有关物质的物理性质见下表。
| 物质 | 沸点(℃) | 密度(g/cm3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
| 环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 1.0 | |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中,在55~65℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)仪器D的名称为_____。
(2)①滴加酸性Na2Cr2O7溶液时反应的离子方程式为______________;
②蒸馏不能分离环己酮和水的原因是_____。
(3)环己酮需要经过以下操作提纯:
a.往液体中加入NaCl固体至饱和,静置,分液
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.加入无水MgSO4固体,除去有机物中少量的水
d.过滤
e.蒸馏、除去乙醚后,收集151~156℃馏分
①b中水层用乙醚萃取的目的是_____;
②上述操作a、d中使用的玻璃仪器除烧杯、玻璃棒外,还需要的玻璃仪器有____、___,操作a中,加入NaCl固体的作用是_____。
(4)恢复至室温时,分离得到纯产品体积为8mL,则环己酮的产率为____。(保留3位有效数字)
-
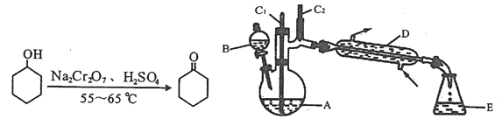
实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略去)如图:
有关物质的物理性质见下表。
| 物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
| 环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 1.0 | |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中,在55~60℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的的名称是为__。
(2)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多。
①如何滴加酸性Na2Cr2O7溶液___;
②蒸馏不能分离环己酮和水的原因是___。
(3)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是___;
②b中水层用乙醚萃取的目的是___;
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有__,操作d中,加入NaCl固体的作用是__。
(4)恢复至室温时,分离得到纯产品体积为6mL,则环己酮的产率为__。
-
实验室制备环己酮的反应原理:
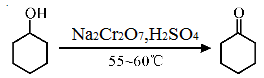
其反应的装置示意图如下(夹持装置、加热装置略去):

环己醇、环己酮、饱和食盐水和水的部分物理性质见下表(注:括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点)
| 物质 | 沸点(℃) | 密度(g·cm-3, 20℃) | 溶解性 |
| 环己醇 | 161.1(97.8) | 0.962 | 能溶于水 |
| 环己酮 | 155.6(95) | 0.948 | 微溶于水 |
| 饱和食盐水 | 108.0 | 1.330 | |
| 水 | 100.0 | 0.998 | |
(1)实验中通过装置B将酸性Na2Cr2O7溶液加到盛有环己醇的A中,在55~60℃进行反应。反应完成后,加入适量水,蒸馏,收集95 ~ 100℃的馏分,得到主要含环己酮粗品和水的混合物。
① 仪器B的名称是 。
② 蒸馏操作时,一段时间后发现未通冷凝水,应采取的正确方法是 。
③ 蒸馏不能分离环己酮和水的原因是 。
(2)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏,收集151~ 156℃馏分,得到精品
b.过滤
c.在收集到的粗品中加NaCl固体至饱和,静置,分液
d.加入无水MgSO4固体,除去有机物中少量水
① 上述操作的正确顺序是 (填序号)。
② 在上述操作c中,加入NaCl固体的作用是 。
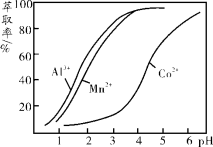
(3)环己酮是一种常用的萃取剂,以环己酮为成分之一的萃取液对金属离子的萃取率与pH的关系如上图。现有某钴矿石的盐酸浸出液, 浸出液含有的阳离子主要有H+、Co2+、Mn2+、Al3+,除去Al3+ 后,再利用萃取法分离出MnCl2以得到较为纯净的CoCl2溶液,pH范围应控制在 。
a.2.0~2.5 b.3.0~3.5 c.4.0~4.5
(4)在实验中原料用量:20mL环己醇、酸性Na2Cr2O7溶液10mL,最终称得产品质量为14.7g,则所得环己酮的产率为 (百分数精确到0.1)。
(5)实验产生的含铬废液易污染环境,可将Cr2O72-转化为Cr3+,再转化为Cr(OH)3沉淀除去,为使Cr3+浓度小于1×10-5mol/L,应调节溶液的pH=___________。(已知该条件下Cr(OH)3的Ksp是6.4×10-31, lg2=0.3 lg5=0.7)
-
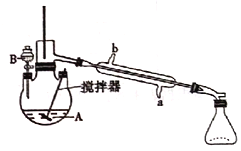
环已酮是工业上的一种重 要有机合成原料和溶剂.实验室制备原理为: 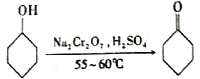 ,其反应的装置示意图如下(夹持装置加热装置略去):
,其反应的装置示意图如下(夹持装置加热装置略去):
已知:
| 物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8) | 0.962 | 能溶于水 |
| 环已酮 | 155.6(95) | 0.948 | 微溶于水 |
(注:括号中的数据表示该有机物与水形成的具有固定组成的恒沸物的沸点)
(1)制备产品。 通过仪器B____ ( 填仪器名称)将酸性Na2Cr2O7和H2SO4混合溶被加到盛有环已醇的三颈烧瓶A中,通过______( 填序号)方法加热到55-60℃进行反应。
a.酒精灯加热 b.油浴加热 c.水浴加热
(2)分离粗品。反应完成后,加入适量水,蒸馏,收集95-100℃的馏分(主要含环已酮粗品和水的混合物),试解释无法分离环己酮和水的原因是____________。
(3)提纯环已酮。
①在收集到的粗品中加NaCl固体至饱和,静置,分液。加入NaCl固体的作用是________。
②加入无水MgSO4固体,除去有机物中________ (填物质名称)。
③过滤,蒸馏,收集151-156℃馏分,得到精品。
(4)下列关于实验的叙述中,错误的是________。
A.冷凝管的冷水应该从b进从a出
B.实验开始时,温度计水银球应插入反应液中,便于控制反应液的温度
C.装置B中也可加入Na2Cr2O7和稀盐酸混合溶液
D.反应过程中,需不断搅拌
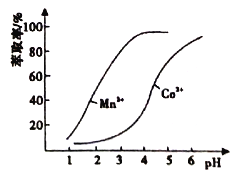
(5)利用环已酮做萃取剂可分离含Co2+、Mn2+的溶液,根据下图信息可判断,将pH范围控制在_______左右时可分离出Mn2+。
-
实验室合成环己酮的反应、装置示意图及有关数据如下:
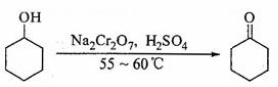
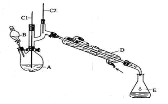
环己醇、环己酮、饱和食盐水和水的部分物理性质见下表:
| 物质 | 沸点(℃) | 密度(g·cm-3, 20℃) | 溶解性 |
| 环己醇 | 161.1(97.8) | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95) | 0.9478 | 微溶于水 |
| 饱和食盐水 | 108.0 | 1.3301 | |
| 水 | 100.0 | 0.9982 | |
括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na2Cr2O7溶液氧化环己醇反应的ΔH<0,反应剧烈将导致体系温度迅速上升,副反应增多。实验中通过装置B将酸性Na2Cr2O7溶液加到盛有环己醇的A中,在55~ 60℃进行反应。反应完成后,加入适量水,蒸馏,收集95 ~ 100℃的馏分,得到主要含环己酮粗品和水的混合物。
①如何滴加酸性Na2Cr2O7溶液 ,用漂粉精和冰醋酸代替酸性Na2Cr2O7溶液也可氧化环己醇制环己酮,用漂粉精和冰醋酸氧化突出的优点是 。
②蒸馏不能分离环己酮和水的原因是 。
(2)环己酮的提纯需要经过以下一系列的操作:a.蒸馏,收集151~ 156℃馏分,b.过滤,c.在收集到的馏分中加NaCl固体至饱和,静置,分液,d.加入无水MgSO4固体,除去有机物中少量水。
①上述操作的正确顺序是 (填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有 。
③在上述操作c中,加入NaCl固体的作用是 。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有 种不同化学环境的氢原子。
-
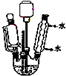
乙酸环己酯具有香蕉及苹果气味,主要用于配制各种饮料、冰淇淋等,实验室制备乙酸环己酯的反应原理、装置示意图和有关数据如下:
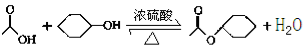
| 
| | 相对分子质量 | 密度/g•cm-3 | 沸点 | 水中溶解性 |
| 乙酸 | 60 | 1.051 | 118.0 | 溶 |
| 环己醇 | 100 | 0.962 | 160.8 | 微溶 |
| 乙酸环己酯 | 142 | 0.969 | 173.5 | 难溶 |
实验步骤:
将12.0g(0.2mol)乙酸、l0.0g(0.1mol)环己醇和15mL环己烷加入装有温度计、恒压滴液漏斗和球形冷凝管的四颈烧瓶中,在搅拌下,慢慢滴加15mL 98%浓硫酸,滴加完后将恒压滴液漏斗换成分水器装置,加热回流90min后,向反应液中依次加入水、10%的NaHCO3溶液、水洗涤,然后加无水MgSO4,放置过夜,加热蒸馏,收集168-174℃的馏分,得到无色透明、有香味的液体产品6.9g
(1)上述反应装置图中存在的一处错误是________。
(2)实验中控制乙酸的物质的量是环己醇的2倍,其目的是_________。
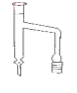
(3)分水器(右图)的作用是__________。
(4)用l0%的NaHCO3溶液洗涤的目的是__________;第二次水洗的目的是__________;加入无水MgSO4的目的是__________。
(5)本次实验的产率为__________。(保留3位有效数字)
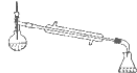
(6)若在进行蒸馏操作时,采用右图装置,会使实验的产率__________(填“偏高”或“偏低”),其原因是__________。








 ,其反应的装置示意图如下(夹持装置加热装置略去):
,其反应的装置示意图如下(夹持装置加热装置略去):