-
生物质能是一种洁净、可再生能源、生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)甲醇的沸点比甲醛的高,其主要原因是_____;
(2)向含Cu2+的水溶液中逐滴加入氨水至过量,观察到溶液由天蓝色最终变为深蓝色,反应过程中涉及的离子方程式为:___、___。写出检验Fe3+生成的配离子的化学式:__,该配离子的配位体是___。
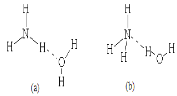
(3)已知NH3·H2O的电离方程式为NH3·H2O⇌NH4++OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构是______(填序号)。
(4)请回答下列问题:
①下列现象和应用与电子跃迁无关的是______。
A.激光 B.焰色反应 C.燃烧放热 D.原子光谱 E.石墨导电
②A、B两种短周期元素,A是原子半径最小的元素,B原子最外层电子数是次外层的两倍。平面正六边形分子由A、B两种元素组成且原子个数比为1:1,该分子中含有___个σ键。
③利用CO可以合成化工原料COCl2,其中COCl2分子的结构式为
,COCl2分子内含有____(填标号);
A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3个σ键、1个π键
高二化学综合题中等难度题查看答案及解析
-
(5分)生物质能是一种洁净、可再生能源。生物质气(主要成分为 CO、CO2、H2 等)与 H2 混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有 Cu、Zn、Al 等元素。写出基态 Cu2+离子的核外电子排布式_______________________________________;
(2)根据等电子原理,写出 CO 分子的结构式______________________;
(3)甲醇催化氧化可得到甲醛,甲醛与新制 Cu(OH)2 的碱性溶液反应生成 Cu2O 沉淀。
①甲醛分子中碳原子轨道的杂化类型为_____________________;
②甲醛分子的空间构型是__________________;
③ 1 mol 甲醛分子中 σ 键的数目为__________________。
高二化学填空题简单题查看答案及解析
-
生物质能是一种洁净、可再生能源。生物质气(主要成分为 CO、CO2、H2 等)与 H2 混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有 Cu、Zn、Al 等元素。写出基态 Cu2+离子的核外电子排布式_________;
(2)根据等电子原理,写出 CO 分子的结构式______________________;
(3)甲醇催化氧化可得到甲醛,甲醛与新制 Cu(OH)2 的碱性溶液反应生成 Cu2O 沉淀。
①甲醛分子中碳原子轨道的杂化类型为_____________________;
②甲醛分子的空间构型是__________________;
③ 1 mol 甲醛分子中 σ 键的数目为__________________。
高二化学填空题困难题查看答案及解析
-
生物质能是一种洁净、可再生能源。生物质气(主要成分为 CO、CO2、H2等)与 H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有 Cu、Zn、Al 等元素。写出基态 Cu2+离子的核外电子排布式_______________________________________;
(2)根据等电子原理,写出 CO 分子的结构式______________________;
(3)甲醇催化氧化可得到甲醛,甲醛与新制 Cu(OH)2的碱性溶液反应生成 Cu2O 沉淀。
①甲醛分子中碳原子轨道的杂化类型为_____________________;
②甲醛分子的空间构型是__________________;
③ 1 mol 甲醛分子中 σ 键的数目为__________________。
高二化学填空题困难题查看答案及解析
-
(12分)生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式______________。
(2)根据等电子原理,写出CO分子的结构式________。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10—9 。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,若Na2CO3溶液的浓度为2×10—4mo1/L,现将等体积的CaCl2溶液与Na2CO3溶液混合,则生成沉淀所需CaCl2溶液的最小浓度为______mo1/ L。
(4)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是________;甲醛分子的空间构型是_____,中心碳原子的轨道杂化类型为_____。1 mol甲醛分子中σ键的数目为________。
②甲醇可制作燃料电池,以KOH溶液作电解质,向两极分别充入甲醇和空气,工作过程中,负极反应方程式为:___________________。
③已知在常温常压下:
CH3OH(l)+O2(g)= CO(g)+2H2O(g) △H= -359.8 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H= -556.0 kJ·mol-1
H2O(g)=H2O(l) △H= -44.0 kJ·mol-1
写出体现甲醇燃烧热的热化学方程式 。
高二化学填空题困难题查看答案及解析
-
(14分)生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1) 上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Cu原子的核外电子排布式_____
(2) 根据等电子原理,写出CO分子的结构式_______________。
(3) 甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
① 甲醇的沸点比甲醛的高,其主要原因是______________________;甲醛分子中碳原子轨道的杂化类型为________。
② 甲醛分子的空间构型是________;1 mol甲醛分子中σ键的数目为________。
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为________。
高二化学填空题中等难度题查看答案及解析
-
(8分)生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Al原子的价电子排布图________。
(2)根据等电子原理,写出CO分子结构式________。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是________;甲醛分子中碳原子轨道的杂化类型为________。
②甲醛分子的空间构型是________;1mol甲醛分子中σ键的数目为________。
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为________。

高二化学填空题简单题查看答案及解析
-
生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与 H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al 等元素。写出基态Zn原子的核外电子排布式________。
(2)根据等电子原理,写出CO分子的结构式________。
(3)甲醇催化氧化可得到甲醛(HCHO),甲醛与新制Cu(OH)2的碱性溶液反应生成 Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是________;甲醛分子中碳原子轨道的杂化类型为_____。
②甲醛分子的空间构型是________;1 mol甲醛分子中σ键的数目为_____。
高二化学填空题困难题查看答案及解析
-
生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式________。
(2)根据等电子原理,写出CO分子的结构式______。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是______________;甲醛分子中碳原子轨道的杂化类型为________。
②甲醛分子的空间构型是________;1 mol甲醛分子中σ键的数目为________。
高二化学填空题中等难度题查看答案及解析
-
生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式:________。
(2)根据等电子原理,写出CO分子的结构式__________。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醛分子中碳原子轨道的杂化类型为_______________。
②甲醛分子的空间构型是___________;1 mol甲醛分子中σ键的数目为______________。
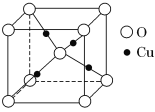
③在1个Cu2O晶胞(结构如图所示)中,所包含的Cu原子数目为______________。
高二化学综合题中等难度题查看答案及解析