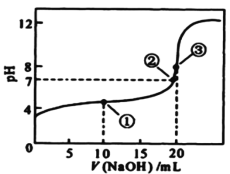
常温下,用 0.1000mol/L NaOH溶液滴定 20.00mL0.1000mol/L某一元酸HA溶液,滴定曲线如图。下列说法正确的是
A.该滴定过程既能用甲基橙又能用酚酞作指示剂
B.点①所示溶液中:c(A-) >c(Na+)>c(H+) >c(OH-)
C.点②所示溶液中:c(Na+) =c(HA) +c(A-)
D.水的电离程度随着NaOH溶液的滴入不断增大
高二化学单选题困难题
常温下,用 0.1000mol/L NaOH溶液滴定 20.00mL0.1000mol/L某一元酸HA溶液,滴定曲线如图。下列说法正确的是

A.该滴定过程既能用甲基橙又能用酚酞作指示剂
B.点①所示溶液中:c(A-) >c(Na+)>c(H+) >c(OH-)
C.点②所示溶液中:c(Na+) =c(HA) +c(A-)
D.水的电离程度随着NaOH溶液的滴入不断增大
高二化学单选题困难题
常温下,用 0.1000mol/L NaOH溶液滴定 20.00mL0.1000mol/L某一元酸HA溶液,滴定曲线如图。下列说法正确的是

A.该滴定过程既能用甲基橙又能用酚酞作指示剂
B.点①所示溶液中:c(A-) >c(Na+)>c(H+) >c(OH-)
C.点②所示溶液中:c(Na+) =c(HA) +c(A-)
D.水的电离程度随着NaOH溶液的滴入不断增大
高二化学单选题困难题查看答案及解析
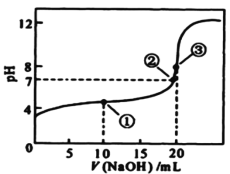
常温下,用 0.1000mol/L NaOH溶液滴定 20.00mL0.1000mol/L某一元酸HA溶液,滴定曲线如图。下列说法正确的是
A.该滴定过程既能用甲基橙又能用酚酞作指示剂
B.点①所示溶液中:c(A-) >c(Na+)>c(H+) >c(OH-)
C.点②所示溶液中:c(Na+) =c(HA) +c(A-)
D.水的电离程度随着NaOH溶液的滴入不断增大
高二化学单选题困难题查看答案及解析
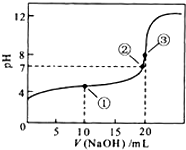
常温下,用 0.1000 mol·L-1NaOH溶液滴定 20.00mL0.1000 mol·L-1某一元弱酸HA溶液滴定曲线如图。下列说法正确的是

A. 点①所示溶液中:c(A-)+c(OH-) =c(HA) +c(H+)
B. 点②所示溶液中:c(Na+) = c(HA) +c(A-)
C. 点③所示溶液中:c(Na+) > c(A-)> c(OH-) > c(H+)
D. 滴定过程中可能出现:c(HA) > c(A-) > c(H+) > c(OH-)> c(Na+)
高二化学选择题中等难度题查看答案及解析
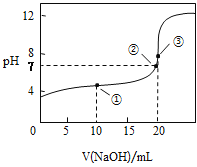
常温下,以酚酞溶液作指示剂,用0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1CH3COOH溶液所得滴定曲线如图:
(1)在整个实验过程中,不需要的仪器或用品是___(填序号)。
a.100mL容量瓶 b.锥形瓶 c.滴定管夹 d.漏斗 e.玻璃棒 f.滴定管
(2)到达滴定终点的标志是___。
(3)下列操作会导致测定结果偏高的是___。
A.碱式滴定管在装液前未用标准NaOH溶液润洗
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C.碱式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
(4)如图点①所示溶液中c(CH3COO-)+c(OH-)___c(CH3COOH)+c(H+)(填“>”“<”或“=”,下同),点②所示溶液中:c(Na+)___c(CH3COOH)+c(CH3COO-)。
高二化学实验题中等难度题查看答案及解析
常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1HA溶液所得滴定曲线如图。下列说法不正确的是
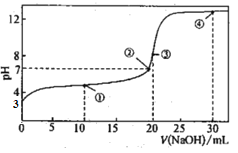
A.HA的电离平衡常数Ka=10-5
B.点①所示的溶液中:2c(Na+)=c(A-)+c(HA)
C.点③所示的溶液中:c(HA)>c(OH-)-c(H+)
D.点④所示的溶液中:2c(OH-)-2c(H+)=c(A-)+3c(HA)
高二化学单选题困难题查看答案及解析
常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1HA溶液所得滴定曲线如图。下列说法不正确的是

A.HA的电离平衡常数Ka=10-5
B.点①所示的溶液中:2c(Na+)=c(A-)+c(HA)
C.点③所示的溶液中:c(HA)>c(OH-)-c(H+)
D.点④所示的溶液中:2c(OH-)-2c(H+)=c(A-)+3c(HA)
高二化学单选题困难题查看答案及解析
常温下,用 0.1000 mol/L NaOH溶液滴定 20.00mL0.1000 mol/L CH3COOH溶液所得滴定曲线如图。下列说法正确的是

A. 点①所示溶液中:c(CH3COO-)+ c(OH-)=c(CH3COOH)+ c(H+)
B. 点②所示溶液中:c(Na+)=c(CH3COOH)+ c(CH3COO-)
C. 点③所示溶液中:c(Na+) >c(OH-) >c(CH3COO-) > c(H+)
D. 滴定过程中可能出现:c(CH3COOH) >c(CH3COO-) > c(H+)>c(Na+) >c(OH-)
高二化学选择题困难题查看答案及解析
高二化学选择题中等难度题查看答案及解析
常温下,用0.1000 mol·L-1 NaOH溶液分别滴定20.00 mL 0.1000 mol·L-1 HBr溶液和20.00 mL0.1000 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如图所示,下列说法不正确的是( )
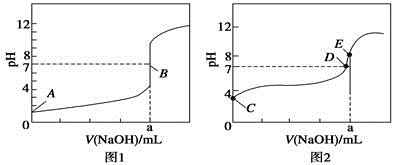
A. 根据图1和图2判断,滴定HBr溶液的曲线是图1
B. a=20.00 mL
C. c(Na+)=c(CH3COO-)的点是B点
D. E点对应溶液中离子浓度由大到小的顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
高二化学选择题困难题查看答案及解析
(14分)常温下,用 0.1000 mol·L-1NaOH溶液滴定 20.00mL0.1000 mol·L-1CH3COOH溶液,pH的变化如图1所示。
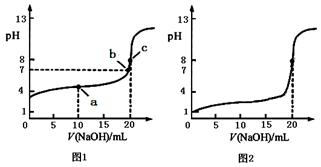
⑴根据图1,用化学符号表示滴定过程中溶液中微粒之间的关系
①点a处: c(CH3COO-)+c(CH3COOH) =________。
②点b处:溶液中离子浓度大小关系:________。
③点c处:c(CH3COOH)+c(H+) =________。
⑵甲同学也用0.1000 mol·L-1NaOH溶液滴定 20.00mL0.1000 mol·L-1CH3COOH溶液进行滴定实验,该同学所绘制的滴定曲线如图2所示。图2中有一处明显错误,请指出错误的原因:
________。
⑶乙同学设计了用0.1000 mol·L-1标准盐酸滴定20.00mL未知浓度氨水的中和滴定实验。
①0.1000 mol·L-1标准盐酸应盛放在________(填仪器名称)中。
②为减少实验误差,指示剂应选用:________。
③滴定过程中眼睛始终注视________。
④若实验中锥形瓶用待盛放的未知浓度氨水润洗,则测定结果将________。(选填“偏高”、“偏低”或“不影响”)
⑷实验室配制pH相等的CH3COONa溶液、NaOH溶液和Na2CO3溶液,三种溶液中溶质的物质的量浓度分别为c1、c2、c3,比较c1、c2、c3的大小关系:
________<________<________。
高二化学填空题中等难度题查看答案及解析