-
某兴趣小组查阅资料发现铁锈的成分除了含Fe2O3·xH2O外,还可能含有FeCO3。他们称取了10.60 g某干燥铁锈样品,粉碎后,进行了如下定量实验:①在氮气保护下充分加热,冷却后固体质量为8.56 g。②向所得固体中滴加5.00 mol·L-1硫酸直至残渣完全溶解,恰好用去硫酸30.00 mL。下列叙述正确的是( )
A. 该铁锈中不含碳酸亚铁
B. 充分加热后所得固体只有Fe3O4
C. 该铁锈中Fe2O3·xH2O的x=1
D. 该铁锈中n(Fe2O3·xH2O)∶n(FeCO3)=5∶4
高二化学单选题困难题查看答案及解析
-
某化学兴趣小组以菱铁矿(主要成分为FeCO3,含有SiO2、Al2O3等少量杂质)为原料制备氯化铁晶体(FeCl3·6H2O)的实验过程如下:
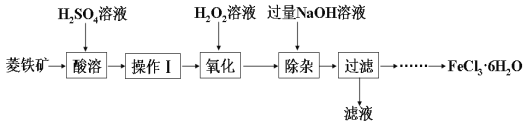
(1)酸溶及后续过程中均需保持酸过量,其目的除了提高铁元素的浸出率之外,还有___________。
(2)操作Ⅰ名称是___________。
(3)滴加H2O2溶液氧化时,发生主要反应的离子方程式为___________。
(4)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3−=Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4−= Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是___________。 (仅供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液、铁粉、KSCN溶液)
(5)加入过量NaOH溶液的目的是___________。
(6)请补充完整由过滤后得到的固体制备FeCl3·6H2O的实验方案:向过滤后所得固体,用水洗涤固体2-3次,低温干燥,得到FeCl3·6H2O。___________
高二化学综合题中等难度题查看答案及解析
-
某化学兴趣小组发现实验室有多件表面呈灰绿色的金属制品, 经了解其来源并查阅相关资料(如下表),初步确认为铜制品。
紫铜
青铜
铜绿
主要成分
纯铜
铜锡合金
Cu2(OH)2CO3
性质与用途
紫红色, 质软,导电性能良好;主要用作电线电缆。
多呈灰绿色, 熔点低、硬度大、 可塑性强;可铸造成各种器具。
不溶于水的灰绿色粉末,溶于酸, 加热易分解;可作颜料、杀虫剂。
针对铜制品表面的灰绿色物质究竟是什么,同学们提出了多种猜想并展开实验探究。
【猜想假设】
(1)小吴同学认为可能是纯铜制品表面涂上了灰绿色的油漆;
小周同学认为可能是青铜(铜锡合金),因为常见的青铜是灰绿色的;
小黄同学认为是纯铜制品,只是表面长出了铜绿[ Cu2(OH)2CO3 ];
除上述猜想外,其他合理的猜想是____________________(只写一个)。
【实验验证】三位同学为了验证各自上述的猜想,进行了以下探究:
(2)小吴刮下部分灰绿色物质放入燃烧匙中进行灼烧,发现该物质不能燃烧,证明灰绿色物质不是油漆。 其判断依据是________________________。
(3)小周刮下足量的灰绿色物质投入盐酸溶液中,观察到有气体产生,实验表明该气体不能燃烧。将表面刮净后的铜制品也投入盐酸中,并无气体产生。由此证明该铜制品不是青铜,理由是__________________。
(4)根据上述实验,小黄认为灰绿色物质可能是铜绿[ Cu2(OH)2CO3 ]。于是按图5所示装置进行实验。
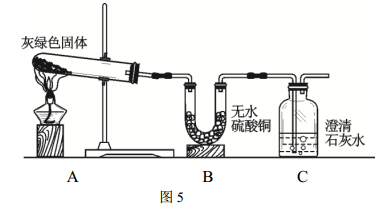
实验证明小黄的猜测是正确的,因为在A中观察到灰绿色物质变黑,B中观察到了___________的现象, C中观察到了_____________的现象。B中所发生反应的化学方程式为:__________________。
如果将实验装置中的B和C进行调换,将无法得出灰绿色物质是铜绿的结论,原因是______________。
【实验拓展】
(5)小黄同学还从网上找到了利用氨水擦拭去除铜绿的方法,其原理是氨水与碱式碳酸铜反应生成铜氨络离子[Cu(NH3)42+],其离子方程式可表示为:___________________________。
高二化学实验题极难题查看答案及解析
-
江苏省东海县矿产丰富,除了水晶制品名扬天下外,蛭石、蛇纹石等矿石储量大,品位高,其相关的耐火、保温隔热材料(主要成分为MgO、Al2O3)工业也较发达。某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究。
Ⅰ.相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成;
②氢氧化物开始沉淀及沉淀完全时的pH:
氢氧化物
Fe(OH)3
Mg(OH)2
Al(OH)3
沉淀的pH范围
1.5~4.1
9.4~12.4
3.3~5.2
Ⅱ.相关实验:
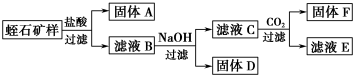
Ⅲ.实验数据:
①矿石样品质量为:8.22 g
②实验过程中得到固体的质量:A—2.40 g、D—2.14 g、F—1.56 g
③每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题:
(1)过滤操作需要的玻璃仪器有:_____________________________________。
(2)写出由D制一种红色颜料的化学方程式:_____________________________________。
(3)工业上的耐火材料通常由F及滤液E进一步转化而成,请你根据滤液E中可能含有的成分,设计一个从滤液E制取耐火材料的实验方法:__________________________。
(4)滤液B与NaOH溶液反应时,应控制溶液的pH在7~8之间,这是因为_______________________________________________________。
(5)通过计算,写出用氧化物的形式表示蛭石组成的化学式:___________________________。
高二化学填空题极难题查看答案及解析
-
某化学兴趣小组拟通过中和滴定实验验证某品牌陈醋的酸度。
(1)查阅资料:
①食醋组成极为复杂,除水以外的主要成分是醋酸CH3COOH,此外还有其他各种有机物和一些无机物等微量成分,醋酸的含量远远多于其他成分的含量。另外其中含一些色素成分,使食醋呈棕色(白醋除外)。
②0.1 mol·L-1醋酸与氢氧化钠恰好完全反应时的pH约为________。
A.5.6 B.7.0 C.8.8 D.13.0
③包装显示该陈醋的酸度约是3.6 g/100 mL。
(2)由以上资料,同学们认为:
①测量时可以忽略老陈醋其他成分特别是有机酸所带来的影响。
②根据陈醋的特点,只能选用________来指示滴定终点。
A.甲基橙 B.酚酞 C.石蕊
③为使滴定时溶液中的醋酸浓度接近0.1 mol·L-1,应将10 mL样品醋稀释至________。
A.36 mL B.60 mL C.360 mL D.600 mL
(3)配制标准氢氧化钠溶液
由于NaOH在称量过程中极易吸水,配好的溶液浓度往往比预期偏小。故实验小组先用0.101 0 mol·L-1的KHP标准溶液准确测定NaOH溶液的浓度(KHP与NaOH按物质的量比1∶1完全反应)。向锥形瓶中盛入20.00 mL NaOH溶液时,应用________量取。
A.20 mL的量筒 B.100 mL的容量瓶 C.碱式滴定管 D.酸式滴定管
(4)用标准氢氧化钠溶液测定醋酸的浓度,并换算为酸度。
V(NaOH)
V(KHP)平均
20.00 mL
18.00 mL
V(稀释后的醋)
V(NaOH)平均
18.00 mL
20.00 mL
计算得出该陈醋样品的酸度为________ g/100 mL。(计算结果保留4位有效数字)
高二化学综合题简单题查看答案及解析
-
(I)工业上过氧化氢是重要的氧化剂和还原剂。常用于消毒、杀菌、漂白等。某化学兴趣小组的同学围绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学习任务:
(1)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在水溶液中的电离方程式:____________________________。
(2)同学们用0.1000 mol /L -1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量,反应原理为2MnO4-+5H2O2 +6H+=2Mn2++8H2O+ 5O2↑。
①在该反应中,H2O2 被_________ (填“氧化”或“还原”)。
②滴定到达终点的现象是____________________________。
③用移液管吸取25.00 mL 试样置于锥形瓶中,重复滴定四次,每次消耗的酸性KMnO4标准溶液体积如下表所示:
第一次
第二次
第三次
第四次
体积(mL)
17.10
18.10
17.00
16.90
则试样中过氧化氢的浓度为__________mol/L-1。
(II)医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。测定含量如下:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀疏酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
(1)滴定时,用_____(填酸或碱)式滴定管装KMnO4溶液。
(2)下列操作会引起测定结果偏高的是______。
A.滴定管在盛装高锰酸钾前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.锥形瓶未用待测液润洗
高二化学综合题中等难度题查看答案及解析
-
工业上过氧化氢是重要的氧化剂和还原剂,常用于消毒、杀菌、漂白等。某化学兴趣小组的同学围绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学习任务:
(1)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在水溶液中的电离方程式:___。
(2)同学们用0.1000mol/L的酸性KMnO4标准溶液滴定某试样中过氧化氢的含量,反应原理为2MnO4-+5H2O2 +6H+=2Mn2++8H2O+5O2↑
①滴定达到终点的现象是___。
②用移液管吸取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗的酸性标准KMnO4溶液的体积如下表所示:
第一次
第二次
第三次
第四次
体积(mL)
17.10
18.10
17.00
16.90
则试样中过氧化氢的浓度为___mol/L。
(3)同学们通过继续查阅资料,发现医学上常用酸性KMnO4溶液和草酸溶液的反应来测定血钙的含量。测定方法如下:取2 mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后再用KMnO4溶液滴定。
①滴定时,用___(填“酸”或“碱”)式滴定管盛装KMnO4溶液。
②下列操作会引起测定结果偏高的是___(填字母代号)。
A.滴定管在盛装KMnO4溶液前未润洗
B.滴定过程中锥形瓶振荡得太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.锥形瓶未用待测液润洗
高二化学综合题中等难度题查看答案及解析
-
某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x的值。通过查阅资料该小组同学得知:草酸易溶于水,其水
溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O。该组同学利用该反应原理设计了滴定的方法测定x值。
① 称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③ 用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,实验记录有关数据如下:
滴定次数
待测草酸溶液体积(mL)
0.1000 mol/LKMnO4标准溶液体积(mL)
滴定前刻度
滴定后刻度
第一次
25.00
0.00
10.02
第二次
25.00
0.22
11.32
第三次
25.00
1.56
11.54

请回答:
(1)滴定时,将KMnO4标准液装在右图中的 (填“甲”或“乙”)滴定管中。
(2)本实验滴定达到终点的标志可以是 。
(3)通过上述数据,计算出x= 。
(4)①若滴定终点时俯视滴定管刻度,则由此测得的x值会 (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 。
高二化学填空题简单题查看答案及解析
-
某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x的值。通过查阅资料该小组同学得知:草酸易溶于水,其水溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O。该组同学利用该反应原理设计了滴定的方法测定x值。
① 称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③ 用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,实验记录有关数据如下:
滴定次数
待测草酸溶液体积(mL)
0.1000 mol/LKMnO4标准溶液体积(mL)
滴定前刻度
滴定后刻度
第一次
25.00
0.00
10.02
第二次
25.00
0.22
11.32
第三次
25.00
1.56
11.54

请回答:
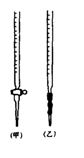
(1)滴定时,将KMnO4标准液装在右图中的________(填“甲”或“乙”)滴定管中。
(2)本实验滴定达到终点的标志可以是________。
(3)通过上述数据,计算出x=________。
(4)①若滴定终点时俯视滴定管刻度,则由此测得的x值会________(填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会________。
高二化学填空题简单题查看答案及解析
-
乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x值。通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O
该组同学设计了滴定的方法测定x值。
① 称取1.260 g纯草酸晶体,将其酸制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③ 用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL;
请回答:
⑴ 滴定时,将KMnO4标准液装在右图中的 (填“甲”或“乙”)滴定管中。
⑵ 本实验滴定达到终点的标志可以是 。
⑶ 通过上述数据,计算出x= 。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会 (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 。
高二化学实验题简单题查看答案及解析