-
硼氢化钠(NaBH4)是常用的还原剂,用途广泛。某探究小组采用偏硼酸钠(NaBO2)为主要原料制备NaBH4,其流程如下:
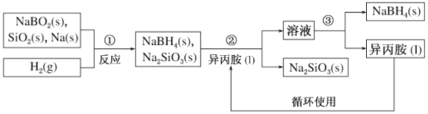
已知:NaBH4常温下易与水反应,可溶于异丙胺(沸点:33℃)
(1)在第①步反应加料之前,需要将反应器加热至 100 ℃以上并通入氩气 ,该操作的目的是______;第②步分离采用的方法是______;第③步分离NaBH4并回收溶剂,采用的方法是_____;
(2)NaBH4与水反应生成H2 : NaBH4 + 2H2O=NaBO2+4H2↑ (已知:HBO2是弱酸)。 实验测得,NaBH4每消耗一半所用的时间与溶液 pH、温度的关系如下表:
| pH | 8 | 10 | 12 | 1 4 |
| 温度/℃ | 25 | 25 | 25 | 25 |
| 时间/ min | 6. 2 ×10-1 | 6. 2 ×10 | 6. 2 ×103 | 6. 2 ×105 |
①NaBH4与水反应开始释放H2很快 ,经过一段时间后就缓慢下来 ,可能原因一是反应物浓度降低 ;二是________;
②为了加快制取的H2速率,常将一些促进剂投入水中,下列物质中可作为促进剂的是__;
a. 碳酸钾 b. 稀硝酸 c 硫酸氢钠 d. 氨水
(3)利用如图所示装置,可以测定NaBH4与水反应生成 H2的速率,在pH =10、25℃条件下,将恒压滴液漏斗中NaBH4滴加到含有催化剂的三颈烧瓶中。
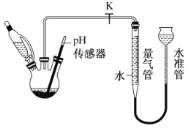
①实验中使用恒压滴液漏斗的原因为_________;
②气体生成结束后,水准管中的液面会高于量气管中的液面,此时量气管读数会_____( 填“偏大”或“偏小”)需要将水准管慢慢向下移动,则量气管中的液面会__________(填“上升”或“下降”);
③在此条件下,0. 38 g NaBH4开始反应至剩余 0. 19 g 时,实验测得量气管内气体体积为124mL,则这段时间内,生成H2的平均速率是_______mL·min-1。
-
(14分)硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠NaBO2为主要原料制备NaBH4,其流程如下:
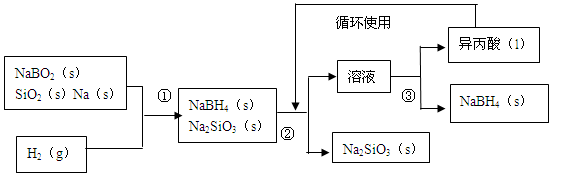
已知:NaBH4常温下能与水反应,可溶于异丙酸(沸点:13℃)。
(1)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是_____,原料中的金属钠通常保存在____中,实验室取用少量金属钠需要用到的实验用品有_____,_____,玻璃片和小刀等。
(2)请配平第①步反应的化学方程式:
□NaBO2+□SiO2+□Na+□H2==□NaBH4+□Na2SiO3
(3)第②步分离采用的方法是______;第③步分离(NaBH4)并回收溶剂,采用的方法是______。
(4)NaBH4(s)与水(l)反应生成NaBO2(s)和氢气(g),在25℃,101KPa下,已知每消耗3.8克NaBH4(s)放热21.6KJ,该反应的热化学方程式是_______。

-
硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠NaBO2为主要原料制备NaBH4,其流程如下:
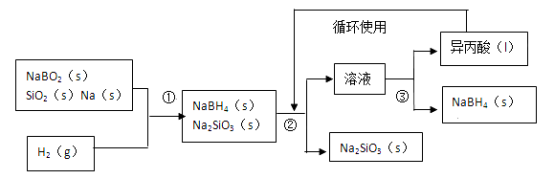
已知:NaBH4常温下能与水反应,可溶于异丙酸(沸点:13℃)。
(1)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是: 。
(2)请配平第①步反应的化学方程式:
NaBO2+ SiO2+ Na+ H2———— NaBH4+ Na2SiO3
(3)第②步操作需要的玻璃仪器有: ;第③步分离出NaBH4并回收溶剂,采用的操作方法是 。
(4)NaBH4与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为: ,反应消耗1molNaBH4时转移的电子数目为 。
-
硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠(NaBO2)为主要原料制备NaBH4,其流程如下:
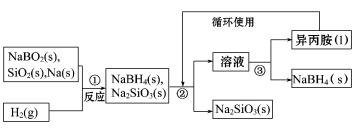
已知:NaBH4常温下能与水反应,可溶于异丙胺(沸点:33℃)。
(1)NaBH4中H元素的化合价为 。
请配平第①步反应的化学方程式,并用单线桥标出电子转移的方向和数目:
□NaBO2+□SiO2+□Na+□H2 □NaBH4+□Na2SiO3
□NaBH4+□Na2SiO3
(2) 实验室取用少量金属钠需要用到的实验用品有 、滤纸、玻璃片和小刀等。
在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是 。
(3)第②步分离采用的方法是 。
第③步分出NaBH4并回收溶剂,采用的方法是 。
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气(g),在25℃,101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是 。
-
硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠NaBO2为主要原料制备NaBH4,其流程如图:
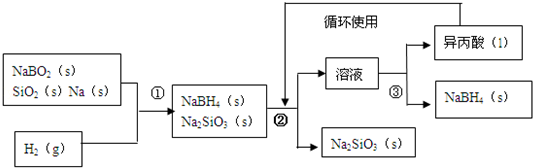
已知:NaBH4常温下能与水反应,可溶于异丙酸(沸点:13℃).
(1)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是: .
(2)请配平第①步反应的化学方程式:
NaBO2+ SiO2+ Na+ H2= NaBH4+ Na2SiO3
(3)第②步操作需要的玻璃仪器有: ;第③步分离出NaBH4并回收溶剂,采用的操作方法是 .
(4)NaBH4与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为: ,反应消耗1molNaBH4时转移的电子数目为 .
-
H·C·Brown和Schlesinger于1942年在芝加哥大学发现的硼氢化钠(NaBH4)是最常用的还原剂之一,反应常生成偏硼酸钠(NaBO2)。有关实验流程如图所示:

I.氢化钠的制备:
已知NaH能在潮湿的空气中自燃。甲同学用如图所示装置(每种装置只选一次)来制取NaH。
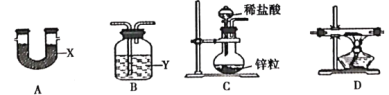
(1)装置的连接顺序是C→____________→D→__________,X、Y分别是__________、__________。
(2)通入H2,点燃装置D处酒精灯之前的实验操作是__________。若省略该操作,可能导致的后果是__________。
Ⅱ.硼氢化钠的制备及纯度测定:
将硼硅酸钠与氢化钠在450~500℃温度和(3.04~5.07)×105Pa压力下反应,生成硼氢化钠和硅酸钠。
(3)乙同学欲通过测定硼氢化钠与稀硫酸反应生成氢气的体积来确定硼氢化钠样品的纯度(杂质只有氢化钠),设计了以下4种装置,从易操作性、准确性角度考虑,宜选装置。__________
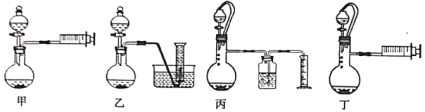
(4)称取4.04g样品(杂质只有氢化钠),重复实验操作三次,测得生成气体的平均体积为9.184L(已折算为标准状况),则样品中硼氢化钠的纯度为__________%(结果保留两位有效数字)。
Ⅲ.碉氢化钠的性质检验:
(5)碱性条件下,丙同学将NaBH4与CuSO4溶液反应可得到纳米铜和NaBO2,其离子方程式为__________。
-
完成下列填空:硼氧化钠(NaBH4)是合成中常用的还原剂。采用NaBO2为主要原料制备NaBH4(B元素化合价为+3)的反应为:NaBO2+SiO2+Na+H2 NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)
NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)
完成下列填空:
(1)上述反应中,原子最外层有两个未成对电子的元素是_____(填元素符号)。SiO2熔点高的原因是_____。
(2)上述反应中H2与Na的物质的量之比为_____。
(3)硅酸钠水溶液产生硅酸(H2SiO3),硬化粘结,且有碱性,其原因是_____(用离子方程式表示)。铸造工艺中可用氯化铵作为水玻璃的硬化剂。试用平衡原理加以解释_____。
(4)NaBH4可使许多金属离子还原成金属单质。例如它从含金离子(Au3+)的废液中提取Au.配平该反应的离子方程式:_____Au3++_____BH4﹣+_____OH-→_____Au+_____BO2﹣+_____H2O。
(5)最新研究发现以NaBH4和H2O2为原料,NaOH溶液作电解质溶液,可以设计成全液流电池,则每消耗1L6mol/L H2O2溶液,理论上流过电路中的电子数为_____。
-
硼氢化钠(NaBH4,硼为+3价)为白色粉末,在干燥空气中稳定,在潮湿空气中分解,是常用的还原剂。偏硼酸钠(NaBO2) 易溶于水,不溶于乙醇,易水解。目前有多种工艺制备NaBH4 。
(1)用硼精矿(含有一定量B2O3,及Al2O3、SiO2、Fe2O3等杂质)制取NaBH4的流程如下:
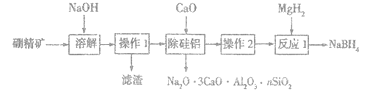
①“溶解”时,B2O3与NaOH反应生成了NaBO2,反应离子方程式为_____________。
②“除硅铝”步骤加入CaO,而不加入CaCl2的原因有:能将硅、铝以沉淀除去;尽量不带入杂质离子;__________。
③“操作2”是将滤液蒸发、结晶、洗涤,其中洗涤选用的试剂最好是___________。
④“反应1”是MgH2与NaBO2混合得到NaBH4和MgO,其化学方程式为_________。
(2)我国孙彦平采用耐腐蚀电极材料,以阳离子交换膜为隔离膜,电解偏硼酸钠的碱溶液,也可以高效制备NaBH4。该工艺阳极产物为______,阴极电极方程式为______________。
-
硼氢化钠(NaBH4)是应用广泛、性能较好的还原剂,以硼酸、甲醇和氢化钠(NaH)为原料可制得硼氢化钠。某学习小组的同学欲利用下图所示路线在实验室合成硼氢化钠。

I.氢化钠的制备
已知NaH的化学反应活性很高,在潮湿的空气中能自燃,与酸接触即放出热量和氢引发燃烧甚至爆炸。该小组的同学利用下图中的装置在实验室制取NaH。
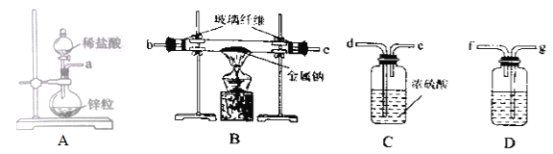
(1)NaH中氢元素的化合价为___________,NaH的电子式为___________。
(2)按气流方向连接各仪器接口,顺序为a→___________b→c(填接口字母);连接装置后进行实验,在给装置B加热前,必须进行的一步操作是___________。
(3)装置A中盛装稀盐酸的仪器名称为___________,装置D中应盛装的试剂是___________。
(4)经分析,该实验装置有一个明显的不足是____________,解决此不足的措施是__________。
Ⅱ.硼氢化钠的制备与纯度测定
在搅拌加热到220℃时,向盛装NaH的缩合反应罐中加入硼酸三甲酯[B(OCH3)3],升温到260℃,充分反应后,经过处理得到NaBH4和甲醇钠。
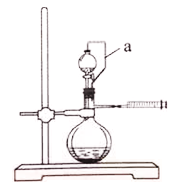
(5)某同学欲通过测定硼氢化钠与水反应生成氢气的体积来测定硼氢化钠产品的纯度。
已知:NaH+H2O=H2↑+NaOH。
①硼氢化钠与水反应可以产生大量氢气和偏硼酸钠,该反应方程式为___________。
②该同学用图装置测定硼氢化钠产品的纯度(杂质只有氢化钠)。装置中a的作用是_________;称取6.28g氢化钠样品,重复实验操作三次,测得生成气体的平均体积为13.44L(已折算为标准状况),则样品中硼氢化钠的纯度为___________%(结果保留两位有效数字)。
-
硼氢化钠(NaBH4)为白色粉末,容易吸水潮解,可溶于异丙胺(熔点:-101℃,沸点:33℃),在干空气中稳定,在湿空气中分解,是无机合成和有机合成中常用的选择性还原剂。某研究小组采用偏硼酸钠(NaBO2)为主要原料制备NaBH4,其流程如下:
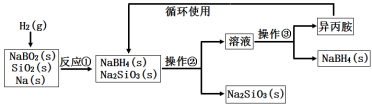
下列说法不正确的是
A.实验室中取用少量钠需要用到的实验用品有镊子、滤纸、玻璃片和小刀
B.操作②、操作③分别是过滤与蒸发结晶
C.反应①加料之前需将反应器加热至100℃以上并通入氩气
D.反应①中氧化剂与还原剂的物质的量之比为1∶2













