-
为了减少“84”消毒液对物品的腐蚀,天津一中高三师生给教室消毒使用的是二氧化氯泡腾片。二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体 ,其熔点为 -59℃,沸点为11.0℃,易溶于水。是目前国际上公认的新—代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面有广泛应用的高效安全消毒剂。与(Cl2)相比(ClO2)不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:
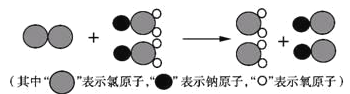
该反应的化学方程式为 ____________。
Ⅰ.ClO2是—种优良的消毒剂 ,浓度过高时易发生分解,为了运输和贮存便利常将其制成NaClO2固体 ,模拟工业上用过氧化氢法制备NaClO2固体的实验装置如图所示:
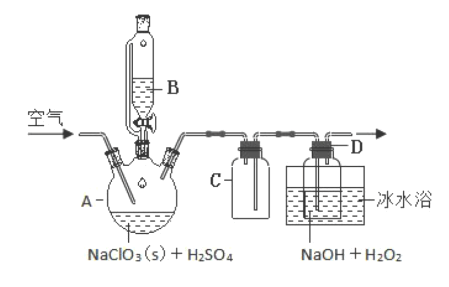
已知:H2O2沸点 150℃;A中的化学方程式:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
(2)NaClO3放入仪器 A中,仪器B中的药品是________(写化学式)。
(3)如果仪器B 改成分液漏斗,实验过程中可能会出现的实验现象_______。
(4)向 A 装詈中通入空气,其作用是赶出ClO2然后通过C 再到 D 中反应。通空气不能过快的,空气流速过快时ClO2不能被充分吸收;通空气也不能过慢,其原因是_________。
(5)冰水浴冷却的目的是_____。
a.降低NaClO2的溶解度 b.减少H2O2的分解
c.使ClO2变为液态 d. 加快反应速率
Ⅱ.“稳定性二氧化氯溶液”是淡黄色透明液体,广泛应用于食品卫生等领域的杀菌消毒。ClO2稳定性较差,“稳定性二氧化氯溶液”是以碳酸钠为稳定剂,有效成分为NaClO2。
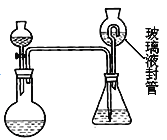
某合作学习小组的同学拟证实其中的有效成分并测定二氧化氯的含量(用样品和酸反应产生二氧化氯的质量与样品质量的比值来衡量)。请回答下列问题:
(6)为证实“稳定性二氧化氯溶液”中含有钠离子,方法是:______。
(7)为测定“稳定性二氧化氯溶液”中二氧化氯的含量,现进行以下操作:①取 mg(2g 左右)试样,置于烧瓶中,向分液漏斗中加入10mL盐酸溶液 ;②在锥形瓶中加入4g 碘化钾,用 100 mL水溶解后 ,再加 3 mL 硫酸溶液 ;③ 在玻璃液封管中加入水;④将分液漏斗中的盐酸溶液放入烧瓶中,关闭旋塞。缓慢加热烧瓶,使产生的二氧化氯气体全部通过导管在锥形瓶中被吸收;⑤将玻璃液封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmo l/L硫代硫酸钠标准溶液滴定至蓝色消失 ( ), 共用去VmL 硫代硫酸钠溶液。
), 共用去VmL 硫代硫酸钠溶液。
①NaClO2与盐酸反应生成ClO2(还原产物为Cl-)该反应的化学方程式为:_______;
②ClO2通入锥形瓶与酸性碘化钾溶液反应,二氧化氯被还原为氯离子,该反应的离子方程式为:_______。
③“稳定性二氧化氯溶液”中,ClO2的质量分数为_____(用m、c、V表示)。
-
(12分) ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒。但二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。
(1)欧洲国家主要采用氯酸钠氧化浓盐酸制备ClO2,缺点主要是产率低,产品难以分离,还产生毒副产品。该反应的化学反应方程式为: 。科学家又研究出了一 种新的制备ClO2的方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为 ,此法提高了生产及储存、运输的安全性,原因是 。
(2)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg/L之间。碘量法可以检测水中ClO2的浓度,步骤如下:
I.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2 S2 O3溶液.(已知:2S2O32-+I2=S4O62-+2I-)
III.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如下图所示。
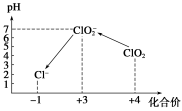
请回答:
①操作I中反应的离子方程式是 。
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式 是 。
是 。
③若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10一3mol/L的Na2S2O3溶液10 mL,则水样中ClO2的浓度是 mg/L。
-
化学与科技、生产、生活密切相关,下列说法正确的是( )
A.使用含有CaCl2的融雪剂会加速对桥梁的腐蚀
B.二氧化氯(ClO2)具有还原性,故可用作自来水的杀菌消毒
C.碳酸氢钠(NaHCO3)是一种抗酸药,服用时喝些醋能提高药效
D.“华为麒麟980”手机中芯片的主要成分是二氧化硅
-
化学与科技、生产、生活密切相关,下列说法正确的是
A. 使用含有CaCl2的融雪剂会加速对桥梁的腐蚀
B. 二氧化氯(ClO2)具有还原性,故可用作自来水的杀菌消毒
C. 碳酸氢钠(NaHCO3)是一种抗酸药,服用时喝些醋能提高药效
D. C919 大型客机使用的碳纤维材料属于有机高分子材料
-
二氧化氯是一种黄绿色具有刺激性气味的气体,常用于自来水消毒和果蔬保鲜等方面。氯酸钠还原法是目前使用较为广泛的ClO2制备方法,其中一种是用NaClO3与CH3OH在催化剂、60℃时,发生反应得到ClO2,如图装置(夹持装置略)对其制备、吸收、释放进行了研究。
已知:
①ClO2的浓度较大时易分解,实验室用稳定剂吸收ClO2,生成NaClO2,使用时加酸只释放出ClO2一种气体;
②ClO2与KI反应的离子方程式为:2ClO2+10I−+8H+=2Cl−+5I2+4H2O。
③
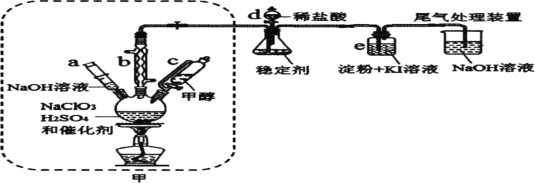
请回答:
(1)比较仪器c和d,实验中c的优点是___。
(2)制备装置甲中需改进的一项措施是___。
(3)反应中甲醇被氧化为甲酸,写出制备ClO2的化学方程式:___;该制备法可选用不同的还原性物质作为还原剂,例如草酸,相比甲醇法,草酸法的优点是___。
(4)下列有关说法正确的是___。
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的ClO2
B.装置e主要用于检验是否有Cl2生成
C.在ClO2释放实验中,发生的离子反应方程式是:4H++5ClO2-=Cl−+4ClO2↑+2H2O
D.ClO2和Cl2都为强氧化剂,在相同条件下,等物质的量时,ClO2的氧化能力是Cl2的2.5倍
(5)自来水厂用碘量法检测水中ClO2的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用0.1000mol·L−1Na2S2O3标准溶液滴定碘单质(I2+2S2O32-=2I−+S4O62-),达到滴定终点时用去20.00mLNa2S2O3标准溶液,测得该水样中ClO2的含量为___mg·L−1。
-
二氧化氯是一种黄绿色具有刺激性气味的气体,常用于自来水消毒和果蔬保鲜等方面。氯酸钠还原法是目前使用较为广泛的ClO2制备方法,其中一种是用NaClO3与CH3OH在催化剂、60℃时,发生反应得到ClO2,如图装置(夹持装置略)对其制备、吸收、释放进行了研究。
已知:
①ClO2的浓度较大时易分解,实验室用稳定剂吸收ClO2,生成NaClO2,使用时加酸只释放出ClO2一种气体;
②ClO2与KI反应的离子方程式为:2ClO2+10I−+8H+=2Cl−+5I2+4H2O。
③
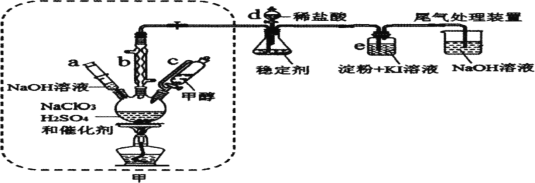
请回答:
(1)比较仪器c和d,实验中c的优点是___。
(2)制备装置甲中需改进的一项措施是___。
(3)反应中甲醇被氧化为甲酸,写出制备ClO2的化学方程式:___;该制备法可选用不同的还原性物质作为还原剂,例如草酸,相比甲醇法,草酸法的优点是___。
(4)下列有关说法正确的是___。
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的ClO2
B.装置e主要用于检验是否有Cl2生成
C.在ClO2释放实验中,发生的离子反应方程式是:4H++5ClO2-=Cl−+4ClO2↑+2H2O
D.ClO2和Cl2都为强氧化剂,在相同条件下,等物质的量时,ClO2的氧化能力是Cl2的2.5倍
(5)自来水厂用碘量法检测水中ClO2的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用0.1000mol·L−1Na2S2O3标准溶液滴定碘单质(I2+2S2O32-=2I−+S4O62-),达到滴定终点时用去20.00mLNa2S2O3标准溶液,测得该水样中ClO2的含量为___mg·L−1。
-
化学与人类生活密切相关。下列说法不正确的是
A. 光导纤维是由高纯度的硅单质制得,遇强碱会“断路”
B. 二氧化氯(ClO2)是新型水处理剂,具有消毒杀菌作用
C. 使用太阳能代替化石能源,可以减少温室气体排放
D. “光化学烟雾”、“硝酸酸雨”的形成都与氮氧化物有关
-
在抗击“2019新型冠状病毒”的过程中,大量防护和消毒用品投入使用。下列有关说法正确的是
A.二氧化氯泡腾片和酒精均可杀灭新型冠状病毒,二者的消毒原理相同
B.聚丙烯和聚四氟乙烯为生产防护服的主要原料,二者均属于有机高分子材料
C.真丝织品和棉纺织品可代替无纺布生产防护口罩,二者均可防止病毒渗透
D.保持空气湿度和适当降温可减少新型冠状病毒传染,二者均可防止病毒滋生
-
二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问題:
(1)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式 。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2: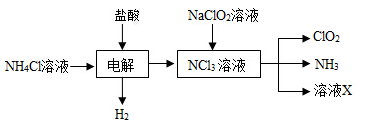
①电解时发生反应的化学方程式为 。
②溶液X中大量存在的阴离子有__________。
③除去ClO2中的NH3可选用的试剂是 (填标号)。
a.水 b.碱石灰 C.浓硫酸 d.饱和食盐水
(3)用下图装置可以测定混合气中ClO2的含量:
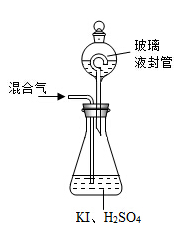
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入 3 mL稀硫酸:
Ⅱ.在玻璃液封装置中加入水.使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液
(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为 。
②玻璃液封装置的作用是 。
③V中滴定至终点的现象是 。
④测得混合气中ClO2的质量为 g.。
-
70年代开始发现氯气应用水消毒会产生具有致癌作用的卤代甲烷类化合物。氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广泛消毒剂,是一种黄绿色的气体,易溶于水。我国从2000年起已逐步用消毒剂ClO2代替氯气对饮用水进行消毒。
(1)ClO2消毒水时,可将Fe2+、Mn2+转化成Fe(OH)3、MnO2难溶物除去,用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子ClO2-。2001年我国卫生部规定,饮用水的ClO-2含量应不超过0.2mg/L。若饮用水中ClO2-的含量超标,可向其中加入适量的某还原剂,该反应的氧化产物是_____________(填化学式)。
ClO2在杀菌消毒的同时,可将剧毒氰化物中碳、氮元素氧化成无毒气体而除去,写出用ClO2氧化除去NaCN的化学方程式___________________________________。
(2)①工业上制备ClO2,可以通过NaClO3在H2SO4存在的条件下与Na2SO3反应制得。
请写出该反应的离子方程式:_________________________________________。
②实验室制备ClO2,可以用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料在一定条件下制得,只是制得的ClO2中混有NH3除去ClO2中的NH3可选用的试剂是____;(填序号)
A.浓硫酸 B.饱和食盐水
C.碱石灰 D.水
(3)测定ClO2(如图)的过程如下:在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定(I2+2S2O32-===2I—+S4O62—),共用去V ml硫代硫酸钠溶液。
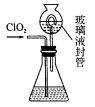
①装置中玻璃液封管的作用是__________________;
②滴定终点的现象是:_________________________。




), 共用去VmL 硫代硫酸钠溶液。







