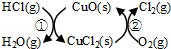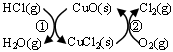-
用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.

(1)反应A的热化学方程式是 。
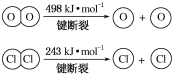
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”) 。
-
用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.

(1)反应A的热化学方程式是____。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为____kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”)____。
-
(8分)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,1 mol HCl被氧化,放出28.9 kJ的热量。
ⅱ.

(1)反应A的热化学方程式是 。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”) 。
(3)大气中的部分碘源于O3对海水中I-的氧化。O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g) IO-(aq)+O2(g) ΔH1
IO-(aq)+O2(g) ΔH1
②IO-(aq)+H+(aq) HIO(aq) ΔH2
HIO(aq) ΔH2
③HIO(aq)+I-(aq)+H+(aq) I2(aq)+H2O(l) ΔH3
I2(aq)+H2O(l) ΔH3
总反应的化学方程式为 ,其反应热ΔH= 。
-
I 用Cl2生产某些含氯有机物时会产生副产物HCl,利用反应A可实现氯的循环利用。反应A:4HCl+O2 2Cl2+2H2O。
2Cl2+2H2O。
已知:ⅰ反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.
(1)H2O的电子式是______________________。
(2)反应A的热化学方程式是_________________________________________________。
(3)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为________ kJ,H2O中H—O键比HCl中H—Cl键________(填“强”或“弱”)。
II 在一定条件下,可逆反应A2(g) + B2(g)  2C(g)达到平衡时,各物质的平衡浓度c(A2)=0.5 mol·L-1、c(B2)=0.1 mol·L-1、c(C)=1.6 mol·L-1,若用a、b、c分别表示A2、B2、C的初始浓度(mol·L-1),则:
2C(g)达到平衡时,各物质的平衡浓度c(A2)=0.5 mol·L-1、c(B2)=0.1 mol·L-1、c(C)=1.6 mol·L-1,若用a、b、c分别表示A2、B2、C的初始浓度(mol·L-1),则:
(1)a、b应满足的关系是________________________________;
(2)a的取值范围是________________________________。
-
(1)用Cl2生产某些含氯有机物时会产生副产物HCl。
利用反应A可实现氯的循环利用。反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.此条件下反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.

①写出此条件下,反应A的热化学方程式 。
②断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ。
(2)氢气用于工业合成氨 N2(g) + 3H2(g)  2NH3(g);ΔH = -92.2 kJ·mol-1。
2NH3(g);ΔH = -92.2 kJ·mol-1。
①一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,正逆反应速率与时间的关系如下图所示,其中t4 ﹑t5 ﹑t7时刻对应的实验条件改变分别是t4 ;t5 ;t7 。

②温度为T℃时,将2nmolH2和nmolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则n= 。
(3)科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4。
①写出铜电极表面的电极反应式 。
②为提高该人工光合系统的工作效率,可向装置中加入少量 (选填“氢氧化钠”或“硫酸”)。
(4)传统制备肼的方法是以NaClO氧化NH3,制得肼(N2H4)的稀 溶液。该反应的
溶液。该反应的 离子方程式是 。
离子方程式是 。
-
用Cl2生产某些含氯有机物时会产生副产物HC1。利用 反应A,可实现氯的循环利用。
反应A,可实现氯的循环利用。
反应A:4HCl+O22Cl2+2H2O
(1)已知:Ⅰ、反应A中, 4mol HCl被氧化,放出115.6kJ的热量。
4mol HCl被氧化,放出115.6kJ的热量。
Ⅱ、
①反应A的热化学方程式是________________________。
②断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为__________kJ,H2O中H—0 键比HCl中H—Cl键(填“强”或“弱”)_______________。
(2)合成氨工厂常通过测定反应前后混合气体的密度来确定氨的转化率。某工厂测得合成塔中N2、H2混合气体的密度为0.5536g/L(标准状况),从合成塔中出来的混合气体在相同条件下密度为0.693g/L(标准状况)。该合成氨厂N2的转化率为___________。
-
用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应A,可实现氯的循环利用。反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
(1)已知:Ⅰ反应A中, 4mol HCI被氧化,放出115.6kJ的热量。
Ⅱ
H2O的电子式是_______________.
②反应A的热化学方程式是_______________。
③断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为__________KJ,H2O中H—O 键比HCl中H—Cl键(填“强”或“若”)_______________。
(2)对于反应A,下图是4种投料比[n(HCl):n(O2),分别为1:1、2:1、4:1、6:1、]下,反应温度对HCl平衡转化率影响的曲线。

①曲线b对应的投料比是______________.
②当曲线b, c, d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度与投料比的关系是_________________.
③投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是_______________.
-
用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A可实现氯的循环利用.反应A:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g).
2Cl2(g)+2H2O(g).
(1)研究表明反应A通过如图所示的催化剂循环实现.
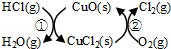
反应①为:2HCl(g)+CuO(s) H2O(g)+CuCl2(s)△H1
H2O(g)+CuCl2(s)△H1
反应②生成1 mol Cl2(g)的反应热为△H2,则A反应的△H表示为 ,
(用△H1和△H2表示).
(2)反应A中4mol HCl被氧化生成Cl2和水蒸气,放出115.6kJ的热量,且部分化学键断裂示意图如下:

①H2O的电子式是 ,反应A的热化学方程式是 .
②断开1mol H﹣O键与断开 1mol H﹣Cl 键所需能量相差约为 kJ,
H2O中H﹣O 键比HCl中H﹣Cl键 (填“强”或“弱”).
(3)“嫦娥二号”于2010年10月1日18时59分57秒在西昌卫星发射中心发射升空,并获得了圆满成功.发射“嫦娥二号”的长三丙火箭的第三级使用的推进剂是液氢和液氧.已知下列热化学方程式:
①H2(g)+ O2(g)═H2O(l)△H1=﹣285.8kJ/mol
O2(g)═H2O(l)△H1=﹣285.8kJ/mol
②H2(g)═H2(l)△H2=﹣0.92kJ/mol
③O2(g)═O2(l)△H3=﹣6.84kJ/mol
④H2O(l)═H2O(g)△H4=+44.0kJ/mol
则反应H2(l)+ O2(l)═H2O(g)的反应热△H为 .
O2(l)═H2O(g)的反应热△H为 .
-
用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl(g)+O2(g)  2Cl2(g)+2H2O(g)。
2Cl2(g)+2H2O(g)。
(1)研究表明反应A通过如下图所示的催化剂循环实现。
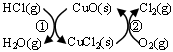
反应①为:2HCl(g)+CuO(s) H2O(g)+CuCl2(g) ΔH1
H2O(g)+CuCl2(g) ΔH1
反应②生成1 mol Cl2(g)的反应热为ΔH2,则A反应的反应热表示为 。(用ΔH1和ΔH2表示)。
(2)反应A中,4mol HCl被氧化,放出115.6kJ的热量,且部分化学键断裂示意图如下:
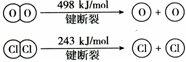
①H2O的电子式是 ,反应A的热化学方程式是 。
②断开1 mol H—O键与断开 1 mol H—Cl 键所需能量相差约为 kJ,H2O中H—O 键比HCl中H—Cl键 (填“强”或“弱”)。
(3)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性。
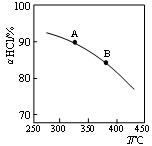
实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的ɑHCl—T曲线如上图所示,若压缩体积使压强增大,画出相应ɑHCl—T曲线的示意图,并简要说明理由 。
-
用Cl2生产某些含氯有机物时会产生副产物HCl,利用如下反应,可实现氯的循环利用:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g)△H=﹣115.6kJ/mol
2Cl2(g)+2H2O(g)△H=﹣115.6kJ/mol

下列说法正确的是
A. 该反应的活化能为115.6kJ/mol
B. 加入催化剂,能使该反应的焓变增大
C. 该反应的正反应活化能比逆反应活化能大
D. 断裂H2O(g)中1molH-O键比断裂HCl(g)中1molH-Cl键所需能量高
 2Cl2+2H2O
2Cl2+2H2O
IO-(aq)+O2(g) ΔH1
HIO(aq) ΔH2
I2(aq)+H2O(l) ΔH3
 2Cl2+2H2O
2Cl2+2H2O
 2Cl2+2H2O
2Cl2+2H2O